Enlace covalente es un tipo de interacción entre átomos que tienen un alto electronegatividad, es decir, alta tendencia a recibir electrones. Los elementos químicos comúnmente involucrados en este tipo de enlace son:
Hidrógeno (H)
Berilio (Be)
Boro (B)
Carbono (C)
Nitrógeno (N)
Fósforo (P)
Oxígeno (O)
Azufre (S)
Flúor (F)
Cloro (Cl)
Bromo (Br)
Yodo (I)
a) Naturaleza de los elementos involucrados
Los elementos químicos que tienen alta electronegatividad y, en consecuencia, realizan enlaces covalentes son:
Hidrógeno
Ametals
b) Aparición del enlace covalente
Dependiendo de la naturaleza de los elementos químicos involucrados en el enlace covalente, puede ocurrir de la siguiente manera:
Entre dos átomos de hidrógeno;
Entre un átomo no metálico y el hidrógeno;
Entre átomos del mismo elemento químico (no metal);
Entre átomos de diferentes elementos químicos (ambos no metales).
c) Número de electrones que debe recibir cada átomo
El número de electrones que recibe cada átomo de hidrógeno o no metal en un enlace está relacionado con la Regla del octeto.
Según la regla del octeto, un átomo es estable cuando adquiere ocho o dos electrones (solo en el caso del hidrógeno) en la capa de valencia. Si un átomo tiene cinco electrones en su capa de valencia, por ejemplo, debe recibir tres electrones para lograr la estabilidad.
NOTA: El berilio y el boro son excepciones a la regla del octeto, a medida que se estabilizan, respectivamente, con 4 y 6 electrones en la capa de valencia.
El número de electrones en la capa de valencia se puede determinar fácilmente analizando la familia de elementos químicos. En la siguiente tabla, tenemos el número de electrones en la capa de valencia que se refiere a la familia a la que pertenece el elemento y el número de electrones que necesita recibir para lograr la estabilidad:

d) Principio de enlace covalente
Como en el enlace covalente, todos los átomos involucrados tienen tendencia a recibir electrones, obligatoriamente, habrá un intercambio entre ellos de los electrones presentes en la capa de valencia (el nivel más alejado del núcleo).
El intercambio ocurre cuando un electrón de la capa de valencia de un átomo se convierte en parte de la misma nube electrónica que rodea a otro electrón de la capa de valencia de otro átomo.
Cada átomo de hidrógeno, por ejemplo, tiene un electrón en la capa de valencia. Cuando dos electrones pasan a formar parte de la misma nube, cada Hidrógeno empieza a tener dos electrones de valencia, es decir, se estabiliza.
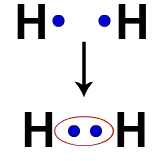
Electrones de dos átomos de hidrógeno que ocupan la misma nube de electrones
e) Fórmulas utilizadas en la unión covalente
1ª) fórmula molecular
Es la indicación del número de átomos de cada elemento que forman la molécula originada a partir de enlaces covalentes.
Ejemplo: H2O
En la molécula de agua, tenemos 2 átomos de hidrógeno y 1 átomo de oxígeno.
2ª) fórmula estructural
La fórmula estructural es la demostración de la organización de la molécula, es decir, demuestra los enlaces entre átomos. Para ello se utilizan guiones que representan el enlace de cada átomo:
Simple (?): Indica que el átomo compartió solo un electrón de su capa de valencia con otro átomo y viceversa;
Doble (?): Indica que el átomo compartió dos electrones de su capa de valencia con el otro átomo y viceversa;
Triple (≡): indica que el átomo ha compartido tres electrones de su capa de valencia con otro átomo y viceversa.
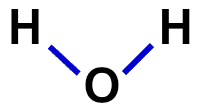
Fórmula estructural del agua
3ª) Fórmula electrónica de Lewis
La fórmula electrónica de Lewis también representa la organización de la molécula (fórmula electrónica), pero tiene como objetivo demostrar el intercambio de electrones en los átomos.
Para construirlo, basta con respetar la organización propuesta en una fórmula estructural y sustituir cada trazo de los enlaces (simple, doble o triple) por “dos bolas”, que representan los electrones.
En la fórmula estructural del agua, por ejemplo, tenemos dos enlaces simples entre Hidrógenos y Oxígeno. Así, entre ellos, solo tendremos dos bolas, delimitadas por una elipse (que representa la nube electrónica).
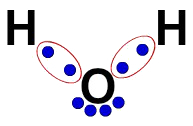
Fórmula electrónica del agua de Lewis
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-covalente.htm

