La descomposición o análisis es un tipo de reacción inorgánica en la que un reactivo se descompone en dos o más sustancias.
Estas sustancias formadas pueden ser simples (compuestas por un solo tipo de elemento químico) o compuestas (compuestas por átomos de diferentes tipos de elementos químicos).
Genéricamente, esto se puede representar por:
A → B + C
Se muestra un ejemplo en el texto. Reacción de airbag y descomposición. O bolsa de aire de automóviles tiene una bolsabolso en inglés) que contiene azida de sodio, que es la siguiente sal: Yaya3 (s). Cuando el automóvil tiene una colisión, los sensores del parachoques transmiten un impulso eléctrico (chispa) que hace que la sustancia se descomponga rápidamente. Vea esta reacción a continuación:
2 NaN3 (s) → 3 N2 (g) + 2 adentro (s)
No pares ahora... Hay más después de la publicidad;)
Tenga en cuenta que la azida de sodio se ha descompuesto en dos sustancias simples, gas nitrógeno, que hace que la bolsa se infle, y sodio metálico, que reacciona con otro compuesto en la bolsa (KNO3) y produce más nitrógeno gaseoso.
En este caso, la descomposición se produjo gracias a la chispa. Pero este tipo de reacción puede iniciarse no solo por la acción del calor, sino también por la acción de la luz o la electricidad. En cada uno de estos casos, la reacción de descomposición recibe un nombre específico, que la caracteriza. Anote cada uno de estos nombres en la siguiente tabla:

Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Reacción de descomposición inorgánica"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/reacao-inorganica-decomposicao.htm. Consultado el 27 de junio de 2021.
Química
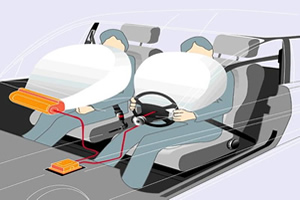
Funcionamiento del airbag, dispositivo diseñado para proteger a los conductores, impulso eléctrico, reacción de descomposición química, colisión, mezcla química de azida de sodio, sensores ubicados en el parachoques del automóvil, silicato alcalino, gas nitrógeno.