capa de valencia es la capa (o nivel) más externa (más alejada del núcleo) de un átomo, es decir, la más alejada del núcleo. Por lo tanto, tiene los llamados electrones más externos o electrones de valencia.
El número de niveles que puede tener un átomo varía de 1 a 7, que tienen los siguientes subniveles (en amarillo):
nivel K (1a capa): subnivel s
nivel L (segunda capa): subniveles s y PAG
nivel M (3a capa): subniveles s, PAG y D
nivel N (4a capa): subniveles s, PAG, D y F
nivel O (quinto nivel): subniveles s, PAG, D y F
Nivel P (sexto nivel): subniveles s, PAG y D
nivel Q (1a capa): subniveles s y PAG
Cada uno de los subniveles contiene un número diferente de electrones. Vea:
el subnivel s contiene un máximo de 2 electrones;
el subnivel p contiene un máximo de 6 electrones;
el subnivel d contiene un máximo de 10 electrones;
el subnivel f contiene un máximo de 14 electrones.
Por tanto, si la capa de valencia de un determinado átomo es M, el número máximo de electrones que puede estar presentes en él son 18 (2 electrones del subnivel s + 6 electrones del subnivel p + 10 electrones del subnivel d).
Para determinar la capa de valencia de un átomo y cuántos electrones tiene, hay dos formas, a saber:
→ Determinación de la capa de valencia y su número de electrones a partir de la distribución electrónica.
Las distribuciones electrónicas siempre se realizan a través del Diagrama de Linus Pauling, representado a continuación:

Representación de un diagrama de Linus Pauling
Ordinario número atómico (que indica el número de electrones en un átomo), hacemos la distribución electrónica. Por ejemplo, un átomo de número atómico 50:

Distribución electrónica del átomo de número atómico igual a 50
Analizando la distribución anterior, tenemos que el nivel más alejado del núcleo es el 5º (nivel N), en el que tenemos la presencia de 4 electrones (dos en el subnivel s y 2 en el subnivel p).
→ Determinación de la capa de valencia y su número de electrones de la tabla periódica
La tabla está organizada en puntos (columnas horizontales), que indican el número de niveles de un átomo y grupos o familias (columnas verticales). El período se utiliza para determinar el capa de valencia, y las familias se utilizan para determinar el número de electrones.
a) Conocer el período del elemento químico
La tabla periódica presenta un total de siete períodos, cuyo número está relacionado con el número de niveles presentes en el diagrama de Linus Pauling. Entonces, si conocemos el período en el que elemento químico está en la tabla, automáticamente, sabemos cuántos niveles tienen sus átomos, siendo la capa de valencia el nivel más alejado del núcleo.
1er Ejemplo: elemento químico Potasio
El potasio se coloca en el cuarto período de la tabla periódica, por lo que su átomo tiene cuatro niveles, siendo el cuarto nivel la capa de valencia, que se confirma a través de su distribución electrónica.
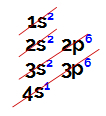
Distribución electrónica del elemento potasio.
2do Ejemplo: elemento químico Flúor
El flúor se coloca en el segundo período de la tabla periódica, por lo que su átomo tiene dos niveles, siendo el segundo nivel la capa de valencia, que se confirma a través de su distribución electrónica.

Distribución electrónica del elemento flúor
3er Ejemplo: elemento químico indio
El indio se posiciona en el quinto período de la tabla periódica, por lo que su átomo tiene cinco niveles, siendo el quinto nivel la capa de valencia, que se confirma a través de su distribución electrónica.

Distribución electrónica del elemento indio
b) Conocer la familia o grupo del elemento químico
Al conocer la familia o grupo en el que se posiciona el elemento, también conocemos el número de electrones presentes en la capa de valencia de ese elemento.
Elementos de la familia A
Los elementos de las familias A se colocan en las columnas 1, 2, 13 a 18 de la tabla periódica. Cada una de estas columnas recibe un número (1 a 8, número romano), que indica exactamente el número de electrones en la capa de valencia de estos elementos:
Columna 1 - Familia IA = todos tienen 1 electrón en la capa de valencia;
Columna 2 - familia IIA = todos tienen 2 electrones en la capa de valencia;
Columna 3 - familia IIIA = todos tienen 3 electrones en la capa de valencia;
Columna 4 - Familia IVA = todos tienen 4 electrones en la capa de valencia;
Columna 5 - Familia VA = todos tienen 5 electrones en la capa de valencia;
Columna 6 - Familia VIA = todos tienen 6 electrones en la capa de valencia;
Columna 7 - familia VIIA = todos tienen 7 electrones en la capa de valencia;
Columna 8 - familia VIIIA = todos tienen 8 electrones en la capa de valencia.
Vea algunos ejemplos de la determinación del número de electrones de valencia de algunos elementos de la familia A:
Ejemplo 1: elemento químico bario
El bario se encuentra en la familia IIA, por lo que tiene dos electrones en la capa de valencia, lo que se confirma por su distribución electrónica:

Distribución electrónica del elemento bario
Ejemplo 2: Elemento químico antimonio
El antimonio se encuentra en la familia VA, por lo que tiene cinco electrones en la capa de valencia, lo que se confirma por su distribución electrónica:

Distribución electrónica del elemento antimonio
Ejemplo 3: Elemento químico xenón
El xenón pertenece a la familia VIIIA, por lo que tiene ocho electrones en la capa de valencia, lo que se confirma por su distribución electrónica.

Distribución electrónica del elemento Xenon
NOTA: el único elemento químico perteneciente a la familia A que no cumple con la regla propuesta es el Helio. Pertenece a la familia VIIIA, pero solo tiene dos electrones en la capa de valencia. Esto se debe a que su número atómico es 2, por lo que es imposible que tenga 8 electrones en la capa de valencia como los otros elementos de la familia.
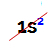
Distribución electrónica de un átomo de helio
Elementos de la familia B
Los elementos de las familias B se colocan en las columnas 3 a 12 de la tabla periódica. Además de las familias A, también hay ocho familias B, que están representadas por números romanos. A diferencia de las familias A, el número de la familia B no determina el número de electrones en la capa de valencia.
El número de electrones en la capa de valencia de un elemento de la familia B es siempre igual a 2, independientemente del número atómico y la posición en la tabla. Las distribuciones electrónicas de californio (98Cf) y hassius (108hs) prueba esto:
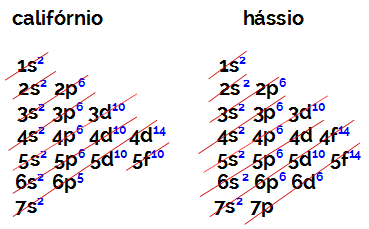
La distribución electrónica de californio tiene como subnivel más energético el 5f10, y la o de hassius es 6d6. En ambos casos, el subnivel más alejado del núcleo es el séptimo nivel, y ambos tienen dos electrones distribuidos.
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-camada-valencia.htm