Η θεωρία υβριδισμού εμφανίστηκε ως συμπλήρωμα του Θεωρία Octet, καταφέρνοντας να εξηγήσουμε τη δομή ενός μεγαλύτερου αριθμού μορίων, συμπεριλαμβανομένων των μορίων που σχηματίζονται από το βόριο (Β).
Αυτό το στοιχείο έχει πέντε ηλεκτρόνια κατάστασης γείωσης, με την ακόλουθη ηλεκτρονική διαμόρφωση:
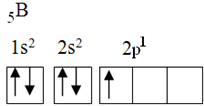
Σύμφωνα με τη θεωρία των οκτάδων, το βόριο μπορούσε να δημιουργήσει μόνο έναν ομοιοπολικό δεσμό, καθώς έχει μόνο έναν ατελή ατομικό τροχιακό. Ωστόσο, πειραματικά, σημειώνεται ότι αυτό το στοιχείο σχηματίζει ενώσεις στις οποίες εκτελεί περισσότερους από έναν δεσμούς.
Ένα παράδειγμα είναι το τριφθοριούχο βόριο (BF3). Όπως φαίνεται παρακάτω, το βόριο δημιουργεί τρεις ομοιοπολικούς δεσμούς με φθόριο, μοιράζοντας τρία ζεύγη ηλεκτρόνια και με έξι ηλεκτρόνια στο τελευταίο του κέλυφος (στρώμα σθένους), δηλαδή, εξαίρεση από τον κανόνα του οκταφωνία.
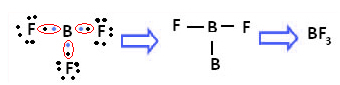
Αυτό εξηγείται από το φαινόμενο υβριδοποίησης που συμβαίνει με το βόριο. Αποδεικνύεται ότι ένα ηλεκτρόνιο από το sublevel 2s απορροφά ενέργεια και πηγαίνει στη διεγερμένη κατάσταση, στην οποία πηδά σε ένα κενό τροχιακό του sublevel 2p. Με αυτόν τον τρόπο, σχηματίζονται τρία ελλιπή τροχιακά, τα οποία μπορούν τώρα να δημιουργήσουν τρεις ομοιοπολικούς δεσμούς:
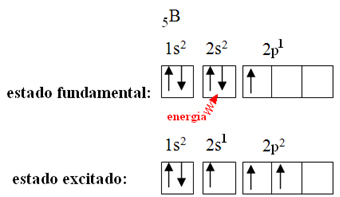
Ωστόσο, οι δεσμοί που σχηματίζονται στο τριφθοριούχο βόριο είναι όλοι οι ίδιοι, αλλά αν κοιτάξουμε παραπάνω, υπάρχουν δύο δεσμοί διαφορετικό, δεδομένου ότι ένα από αυτά θα γινόταν με τροχιακό s και το άλλο με τροχιακό τύπο. πληκτρολογήστε p. Εδώ συμβαίνει ο υβριδισμός, δηλαδή, οι ελλιπείς τροχιές συγχωνεύονται, δημιουργώντας τρεις υβριδικά τροχιακά ή υβριδισμένος, που είναι πανομοιότυπα και διαφορετικά από τα πρωτότυπα:
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση;)
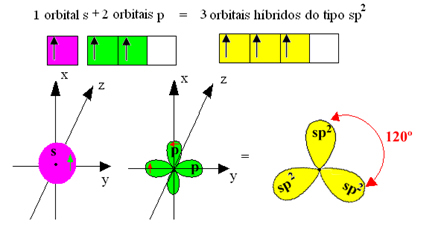
Δεδομένου ότι αυτά τα υβριδικά τροχιακά αποτελούνται από ένα τροχιακό ενός s και δύο p τροχιακά, αυτή η υβριδοποίηση ονομάζεται υβριδοποίηση sp2.
Το φθόριο που συνδέεται με το βόριο έχει εννέα ηλεκτρόνια. Η ηλεκτρονική διανομή και τα τροχιακά του φαίνονται παρακάτω:
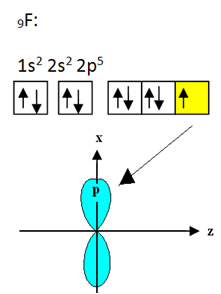
Σημειώστε ότι κάθε άτομο φθορίου μπορεί να δημιουργήσει μόνο έναν ομοιοπολικό δεσμό και ότι το τροχιακό που δημιουργεί αυτόν τον δεσμό είναι τύπου p. Λοιπόν, παρατηρήστε παρακάτω πώς σχηματίζονται τα τροχιακά όταν κάνετε τις συνδέσεις που σχηματίζουν το BF3 και δείτε πώς οι σύνδεσμοι είναι ίδιοι, όπως σp-sp2:
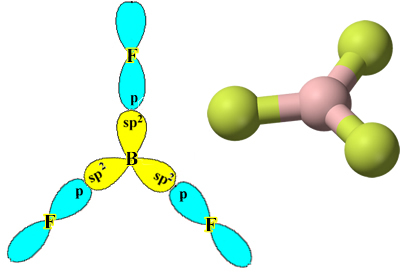
Αυτό συμβαίνει επίσης με άλλα στοιχεία, δείτε, για παράδειγμα, το κείμενο "Υβριδοποίηση βηρυλλίου”.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Υβριδοποίηση βορίου". Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm. Πρόσβαση στις 28 Ιουνίου 2021.