Αμερικανός χημικός Gilbert N. Ο Lewis (1875-1946) πρότεινε τον κανόνα οκτάδας, ο οποίος λέει:
"Άτομα διαφορετικών στοιχείων δημιουργούν χημικούς δεσμούς, δωρίζουν, λαμβάνουν ή μοιράζονται ηλεκτρόνια, προκειμένου να αποκτήσουν την ηλεκτρονική διαμόρφωση του ευγενές αέριο, δηλαδή, με 8 ηλεκτρόνια στο τελευταίο κέλυφος (ή με 2 ηλεκτρόνια στην περίπτωση εκείνων των ατόμων που έχουν μόνο ένα κέλυφος ηλεκτρονίων, όπως συμβαίνει με το υδρογόνο)."
Το 1916, ο Lewis πρότεινε να παραμείνει σταθερός, φτάνοντας στο οκτάτο ή στο ντουέτο, τα στοιχεία που απαρτίζουν το μοριακές ουσίες εκτελέστε κοινή χρήση ζευγών ηλεκτρονίων. Αυτές οι ουσίες σχηματίζονται μόνο από άτομα υδρογόνο, μη μέταλλα και ημι μέταλλα, όλα με το τάση λήψης ηλεκτρονίων. Επομένως, δεν υπάρχει τρόπος για κανέναν από αυτούς να δωρίσει οποιοδήποτε ηλεκτρόνιο (όπως συμβαίνει με μέταλλα σε ιοντικούς δεσμούς), αλλά ο καθένας πρέπει να λάβει, έτσι μοιράζονται τα ηλεκτρόνια τους μέσω ενός ομοιοπολικού δεσμού ή μοριακός.
Έτσι, ο Gilbert Lewis πρότεινε έναν τρόπο αναπαράστασης του ομοιοπολικού ή μοριακού δεσμού, ο οποίος έγινε γνωστός ως
Τύπος Lewis. Λέγεται επίσης ηλεκτρονικός τύπος ή ακόμα, Η ηλεκτρονική φόρμουλα του Lewis, επειδή το κύριο χαρακτηριστικό του είναι ότι είναι δείχνει τα ηλεκτρόνια στο κέλυφος σθένους κάθε ατόμου και τον σχηματισμό ηλεκτρονικών ζευγών.Κάθε ηλεκτρόνιο αντιπροσωπεύεται από μια τελεία., που περιβάλλει το σύμβολο του αντίστοιχου χημικού στοιχείου. Μόνο τα ηλεκτρόνια κελύφους σθένους βρίσκονται γύρω από το στοιχείο.
Όπως φαίνεται στον παρακάτω πίνακα, για να γνωρίζετε την ποσότητα ηλεκτρονίων στο κέλυφος σθένους, απλώς γνωρίζετε την οικογένεια Περιοδικού Πίνακα:
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση;)

Στη φόρμουλα Lewis, κάθε κοινό ζεύγος ηλεκτρονίων αντιπροσωπεύει έναν χημικό (ομοιοπολικό) δεσμό, όπου τα ηλεκτρόνια συναντώνται στην περιοχή της ηλεκτροσφαίρας που είναι κοινό σε κάθε ζεύγος ατόμων που συνδέονται μεταξύ τους. Επομένως, στην αναπαράσταση, τοποθετούνται δίπλα-δίπλα.
Για παράδειγμα, ας μάθουμε ποιος είναι ο τύπος Lewis για το αέριο υδρογόνο, του οποίου ο μοριακός τύπος είναι: H2.
Κάθε άτομο υδρογόνου έχει μόνο ένα ηλεκτρόνιο στο κέλυφος σθένους, καθώς αυτό το στοιχείο ανήκει στην οικογένεια 1 του Περιοδικού Πίνακα. Ο καθένας πρέπει να λάβει ένα ακόμη ηλεκτρόνιο, ώστε να είναι σταθερό, με δύο ηλεκτρόνια στο κέλυφος ηλεκτρονίων Κ. Έτσι μοιράζονται τα ηλεκτρόνια τους και οι δύο παίρνουν δύο. Κοίτα:
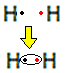
Αυτός είναι ο τύπος Lewis για το μόριο αερίου υδρογόνου.
Το οξυγόνο έχει έξι ηλεκτρόνια στο κέλυφος ηλεκτρονίων του, οπότε το καθένα πρέπει να λάβει δύο ακόμη ηλεκτρόνια για να είναι σταθερό, με οκτώ ηλεκτρόνια. Επομένως, ο τύπος Lewis για το μόριο αερίου οξυγόνου είναι:

Δείτε ότι υπάρχουν δύο σύνδεσμοι, καθώς υπάρχουν δύο κοινόχρηστα ζεύγη.
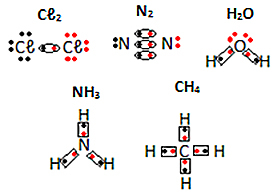
Δείτε άλλα παραδείγματα ηλεκτρονικών τύπων μοριακών ουσιών παρακάτω:
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Ηλεκτρονική φόρμουλα Lewis". Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/formula-eletronica-lewis.htm. Πρόσβαση στις 28 Ιουνίου 2021.
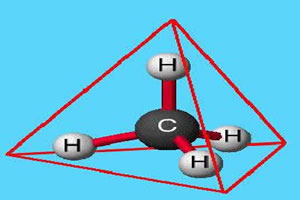
Χωρικός τύπος άνθρακα, Ηλεκτρονικός τύπος Lewis, δομή επιπέδου, ηλεκτρονικά ζεύγη, δεσμός ομοιοπολικό, στρώμα σθένους, εξέλιξη του ατομικού μοντέλου, μοριακός τύπος, δομικός τύπος, τύποι τρισδιάστατο.
Χημικοί τύποι, επίπεδος δομικός τύπος, συντακτικός τύπος Couper, τριπλός δεσμός, αέριο άζωτο, ηλεκτρονικός τύπος, τύπος Lewis, μοριακός τύπος, μονός δεσμός, διπλός δεσμός, αέριο ανθρακικός.
Χημεία
Μοριακές ουσίες, θερμοκρασία βρασμού, επιφάνεια επαφής, σημείο βρασμού, διαμοριακές δυνάμεις έλξης, χημικός δεσμός, μοριακές ενώσεις, ομοιοπολικοί χημικοί δεσμοί, ιοντικοί δεσμοί, μεταλλικοί δεσμοί, φυσικές καταστάσεις κακό


