Μία από τις μεγαλύτερες προκλήσεις για όσους μαθαίνουν Χημεία ονομάζεται ηλεκτρονική διανομή. Αυτό που πρόκειται να παρουσιάσουμε σε αυτό το πλαίσιο μπορεί να διευκολύνει σε μεγάλο βαθμό τις μελέτες σας σχετικά με τη διαμόρφωση ηλεκτρονίων που πρότεινε ο επιστήμονας Linus Pauling.
Ο μέγιστος αριθμός ηλεκτρονίων που ταιριάζει σε κάθε επίπεδο ή επίπεδο ενέργειας δίνεται μέσω του πίνακα:
Μέγιστος αριθμός επιπέδων ενεργειακού επιπέδου
1ο Κ 2
2ο L 8
3ο Μ 18
4ο Ν 32
5 ° Ο 32
6ο P 18
7ο Ε 8
Η αυξανόμενη τάξη ενέργειας των επιπέδων είναι η σειρά στην ακολουθία των διαγώνων. Το διάγραμμα Linus Pauling φαίνεται παρακάτω:
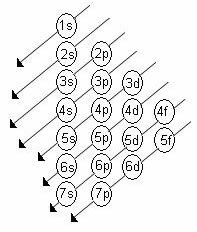
Βασικοί κανόνες:
1. Ο ατομικός αριθμός (Z) του στοιχείου, στην ουδέτερη κατάσταση, δείχνει τον αριθμό των ηλεκτρονίων που θα διανεμηθούν. Αυτός ο αριθμός αντιπροσωπεύεται στο κάτω αριστερό μέρος του συμβόλου στοιχείου.
2. Χρησιμοποιώντας το διάγραμμα Pauling, ξεκινήστε να διανέμετε τα ηλεκτρόνια από πάνω προς τα κάτω, λαμβάνοντας υπόψη την αυξανόμενη σειρά ενέργειας (προσανατολισμένη από την κατεύθυνση των βελών).
3. Γεμίστε τα επίπεδα με τη μέγιστη στάθμη ηλεκτρονίων. Εάν ένα δεδομένο επίπεδο έχει μόνο 6 ηλεκτρόνια, μην υπερβαίνετε αυτό το ποσό.
4. Ελέγξτε τον αριθμό των ηλεκτρονίων προσθέτοντάς τα σε κάθε επίπεδο.
Ας το εφαρμόσουμε;
Κατανομή των ηλεκτρονίων του ατόμου σιδήρου (Z = 26).
Εάν ο ατομικός αριθμός είναι 26, αυτό σημαίνει ότι στο κανονικό άτομο σιδήρου υπάρχουν 26 ηλεκτρόνια. Εφαρμόζοντας το διάγραμμα Pauling, θα έχουμε:
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση;)

Από τη Lria Alves
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Κανόνες ηλεκτρονικής διανομής" · Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm. Πρόσβαση στις 27 Ιουνίου 2021.
