Στο οργανικές αντιδράσεις αποβολής είναι εκείνα στα οποία άτομα ή ομάδες ατόμων ενός μορίου απομακρύνονται ή εξαλείφονται από αυτό, δημιουργώντας μια νέα οργανική ένωση, εκτός από μια ανόργανη ένωση που σχηματίζεται από το μέρος που ήταν διαγράφηκε.
Ένας τύπος αντίδρασης αποβολής είναι το αφυδάτωση, στο οποίο το μόριο που χάνεται είναι νερό. Η αφυδάτωση των αλκοολών (ενώσεις που έχουν την ομάδα ΟΗ συνδεδεμένη με έναν κορεσμένο άνθρακα σε ανοιχτή αλυσίδα) μπορεί να λάβει χώρα με δύο τρόπους: ενδομοριακό και διαμοριακό.
"Intra" σημαίνει "εσωτερικό", επομένως, η ενδομοριακή αφυδάτωση των αλκοολών συμβαίνει όταν ένα μόριο νερού εξέρχεται από «μέσα» το ίδιο το μόριο αλκοόλης. Σε αυτήν την περίπτωση, το οργανικό προϊόν που σχηματίζεται θα είναι αλκένιο.
Αυτή η αντίδραση λαμβάνει χώρα μόνο παρουσία ενός καταλύτη που δρα ως ξηραντικό, και τις περισσότερες φορές είναι συμπυκνωμένο θειικό οξύ (H2ΜΟΝΟ4) και η θερμοκρασία πρέπει να είναι περίπου 170ºC.
Παράδειγμα:
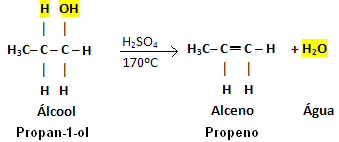
Σημειώστε ότι η ομάδα OH έφυγε και το υδρογόνο άφησε τον γειτονικό άνθρακα, δημιουργώντας νερό. Επιπλέον, δημιουργήθηκε ο διπλός δεσμός που προκάλεσε το αλκένιο.
Η εγκατάσταση για αφυδάτωση ακολουθεί την ακόλουθη φθίνουσα σειρά:
Τριτογενείς αλκοόλες> Δευτερεύουσες αλκοόλες> Πρωτογενείς αλκοόλες
Τι γίνεται όμως όταν η ομάδα OH έρχεται στη μέση της αλυσίδας άνθρακα; Το άτομο υδρογόνου από το οποίο θα απελευθερωθεί το γειτονικό άτομο άνθρακα και θα σχηματίσει το μόριο του νερού;
Για παράδειγμα, το επόμενο είναι 2-μεθυλοπενταν-3-όλη. Σημειώστε ότι το ένα γειτονικό άτομο άνθρακα είναι τριτογενές (επισημαίνεται με κόκκινο χρώμα), ενώ το άλλο είναι δευτερεύον (επισημαίνεται με μπλε χρώμα):
Ω Ω Χ
│ │ │
Η3Γ─ ΝΤΟ ─ ΝΤΟ ─ ΝΤΟ ─ CH3
│ │ │
Χ Χ CH3
Το υδρογόνο που συνδέεται με το άτομο τριτοταγούς άνθρακα θα είναι ευκολότερο να αφεθεί, επειδή ο ηλεκτροαρνητικός χαρακτήρας του είναι ίσος με+1Έτσι, όσο λιγότερο αρνητικός είναι ο χαρακτήρας του άνθρακα, τόσο ασθενέστερος είναι ο δεσμός μεταξύ τους και τόσο πιο εύκολο θα είναι να σπάσει ο δεσμός τους.
Σε τέτοιες περιπτώσεις, σχηματίζονται όλες οι πιθανές ενώσεις, ωστόσο, η επικράτηση θα δοθεί με τη σειρά: Τριτογενείς αλκοόλες> Δευτερεύουσες αλκοόλες> Πρωτογενείς αλκοόλες.
Έτσι έχουμε:
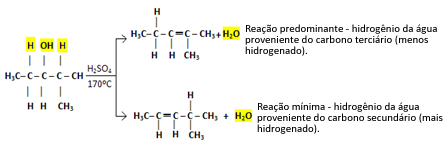
Αυτός ο τύπος αντίδρασης υπακούει στο Ο κανόνας του Saytzef, που το λέει αυτό θα υπάρχει μεγαλύτερη τάση για το υδρογόνο να αφήνει άνθρακα λιγότερο υδρογονωμένο. Αυτός ο κανόνας είναι ακριβώς το αντίθετο Ο κανόνας του Μάρκοβνικοφ χρησιμοποιείται για αντιδράσεις προσθήκης.
Για να συμπληρώσετε τις γνώσεις σας σχετικά με αυτό το θέμα, διαβάστε επίσης το κείμενο "Διαμοριακή αφυδάτωση αλκοολών”.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/desidratacao-intramolecular-dos-Alcoois.htm

