Ο στερεοισομερεία, επίσης γνωστός ως Διαστημικός ισομερισμός, είναι ένας τύπος ισομερισμού στον οποίο τα ισομερή του διαφοροποιούνται από τους δεσμούς μεταξύ των ατόμων τους που τακτοποιούνται διαφορετικά στο διάστημα.
Υπάρχουν δύο τύποι στερεοϊσομερών, το διαστερεοϊσομερή και το εναντιομερή. Τα διαστερεοϊσομερή είναι γεωμετρικά ισομερή τύπου cis-trans, τα οποία δεν είναι καθρέφτες μεταξύ τους, ενώ τα εναντιομερή είναι οπτικά ισομερή που είναι καθρέφτες μεταξύ τους.
Μιλώντας λίγο για το cis-trans διαστερεοϊσομερές, εμφανίζεται μόνο σε ενώσεις που είναι ακόρεστες ή κυκλικές. Γιατί δεν συμβαίνει σε κορεσμένες αλυσίδες ενώσεις, δηλαδή που έχουν μόνο μεμονωμένους δεσμούς μεταξύ των ανθράκων;
Μπορεί να γίνει σύγχυση, πιστεύοντας ότι ορισμένες κορεσμένες ενώσεις είναι διαστερεοϊσομερή, ενώ στην πραγματικότητα αντιπροσωπεύουν την ίδια ένωση. Για παράδειγμα, παρακάτω, έχουμε τρεις χωρικές διαμορφώσεις των ατόμων του 1,2-διχλωροαιθανίου:
Η Χ Υ Η Η Κλ
│ │ │ │ │ │
Η — ΝΤΟ — ΝΤΟ — Χ Χ — ΝΤΟ — ΝΤΟ — ClH — ΝΤΟ — ΝΤΟ — Η
│ │ │ │ │ │
Κλ ΚλΚλ Η Κλ Η
Είναι αυτά τα τρία διαστερεοϊσομερή; Μην. Πράγματι, τα τρία μόρια είναι της ίδιας ένωσης. Αυτό που συμβαίνει είναι ότι οι απλοί δεσμοί ή το σίγμα (σ) μεταξύ των ανθράκων μπορούν να υποστούν περιστροφές, με αποτέλεσμα διαφορετικές ατομικές διευθετήσεις.
Δείτε πώς συμβαίνει αυτό στο σχήμα παρακάτω με αιθάνιο:

Αυτές οι ενώσεις, οι οποίες στην πραγματικότητα είναι η ίδια ένωση, δεν εκτελούν γεωμετρικό ισομερισμό cis-trans, αλλά ονομάζονται διαμορφωτικά ισομερή, καθώς διαφέρουν μόνο στη διαμόρφωση των ατόμων τους που προκαλούνται από περιστροφή γύρω από τον απλό δεσμό.
Ένας από τους τρόπους για την αναπαράσταση αυτών των μορίων για την εύκολη απεικόνιση της περιστροφής του άξονα σύνδεσης είναι μέσω του Η προβολή του Newman, στο οποίο θεωρείται ότι το επίπεδο όρασης ήταν ακριβώς στον άξονα του δεσμού μεταξύ των ανθράκων και αντιπροσωπεύονται από έναν κεντρικό κύκλο. Δείτε την προβολή του Newman για το αιθάνιο:

Μπορούμε επίσης να αναπαραστήσουμε αυτές τις διαφορετικές διαμορφώσεις μέσω του τύπος στα καβαλέτα:
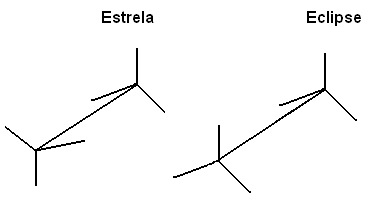
Αυτή η ελεύθερη περιστροφή του άξονα σύνδεσης δεν συμβαίνει πλέον σε ακόρεστες ενώσεις ή σε κυκλικές ενώσεις. Για παράδειγμα, φανταστείτε ότι χτίζουμε ένα απλό μοντέλο, που αντιπροσωπεύει δύο άνθρακες από δύο μπάλες Styrofoam που συνδέονται με μια οδοντογλυφίδα κολλημένη σε αυτά.
Όταν έχουμε μία μόνο οδοντογλυφίδα και κρατάμε μία από τις μπάλες, η άλλη μπορεί εύκολα να περιστρέφεται γύρω από τον άξονά της, όπως συμβαίνει με την απλή δέσμευση.

Ωστόσο, εάν τοποθετήσουμε μία ακόμη οδοντογλυφίδα που συνδέει τις δύο σφαίρες, δεν θα είμαστε σε θέση να κρατήσουμε τη μία σφαίρα και να περιστρέψουμε την άλλη. Αν το κάνουμε αυτό, οι οδοντογλυφίδες θα σπάσουν. Ομοίως, όταν υπάρχει ένας δεσμός pi και ένα σίγμα (διπλός δεσμός) υπάρχει ένα εμπόδιο στην περιστροφή των ανθράκων.
Επομένως, στην παρακάτω περίπτωση, στην οποία έχουμε διπλό δεσμό μεταξύ των άνθρακα, δεν πρόκειται για δύο ισομερή διαμόρφωσης, δηλαδή δύο διαμορφώσεις για το ίδιο μόριο. στην πραγματικότητα έχουμε δύο διαστερεοϊσομερή cis-trans:
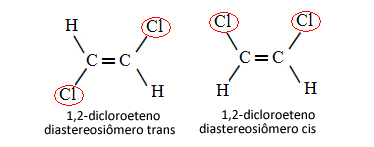
Δείτε περισσότερα για αυτόν τον τύπο ισομερισμού στο κείμενο Γεωμετρικά ή cis-trans ισομερή.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/isomeria-conformacional.htm
