Στο οικογένειες περιοδικού πίνακα είναι οι κάθετες ακολουθίες του πίνακα και συγκεντρώνονται χημικά στοιχεία με παρόμοιες χημικές ιδιότητες. Τέτοιες ομοιότητες οφείλονται στην παρουσία ίσων ποσοτήτων ηλεκτρονίων σθένους για τα στοιχεία που ομαδοποιούνται στην ίδια οικογένεια. Οι οικογένειες φιλοξενούν τα αντιπροσωπευτικά στοιχεία στις ομάδες 1 και 2, από 13 έως 18 και τα μεταβατικά στοιχεία στις ομάδες 1 έως 12.
Διαβάστε επίσης:Υπερουρανικά στοιχεία — τα τεχνητά χημικά στοιχεία που έρχονται μετά το ουράνιο στον Περιοδικό Πίνακα
Περίληψη Οικογενειών Περιοδικού Πίνακα
Οι οικογένειες αντιστοιχούν στις κάθετες γραμμές του Περιοδικός Πίνακας.
Γνωστές και ως ομάδες, οι οικογένειες στον Περιοδικό Πίνακα αριθμούνται από το 1 έως το 18.
Τα χημικά στοιχεία της ίδιας οικογένειας έχουν παρόμοιες χημικές ιδιότητες.
Η εξοικείωση ενός συνόλου στοιχείων εξηγείται από την ύπαρξη ίσου αριθμού ηλεκτρονίων σθένους.
Τα αντιπροσωπευτικά στοιχεία χωρίζονται στις ομάδες 1, 2, 13, 14, 15, 16, 17 και 18. Κάθε μία από αυτές τις οικογένειες έχει συγκεκριμένα ονόματα.
Τα μεταβατικά στοιχεία σχηματίζουν μια ενιαία οικογένεια που χωρίζεται σε ομάδες 3, 4, 5, 6, 7, 8, 9, 10, 11 και 12.
Οργάνωση οικογενειών του Περιοδικού Πίνακα
Οικογένειες στον περιοδικό πίνακα είναι οι κάθετες ακολουθίες του πίνακα, δηλαδή τις στήλες. Γνωστές και ως ομάδες, οι οικογένειες του Περιοδικού Πίνακα αριθμούνται από το 1 έως το 18, από αριστερά προς τα δεξιά.
Τα χημικά στοιχεία που καταλαμβάνουν την ίδια στήλη θεωρούνται ότι ανήκουν στην ίδια οικογένεια., λόγω της ομοιότητας μεταξύ των χημικών τους ιδιοτήτων, η οποία οφείλεται στο γεγονός ότι έχουν τον ίδιο αριθμό από ηλεκτρόνια στο κέλυφος σθένους. Για παράδειγμα, όλα τα χημικά στοιχεία της οικογένειας 18 έχουν οκτώ ηλεκτρόνια στο φλοιό σθένους (πλήρης φλοιό) και σπάνια συμμετέχουν σε χημικοί δεσμοί.
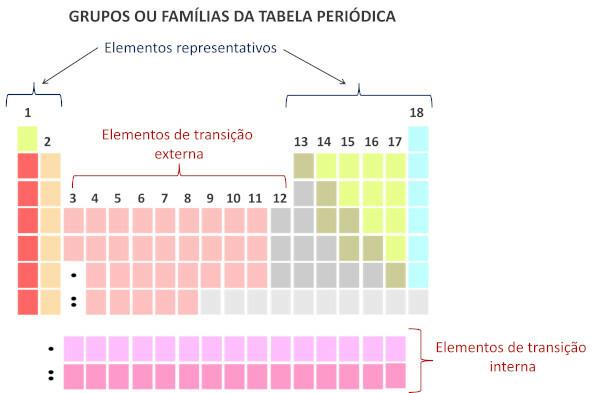
Σύμφωνα με το σύγχρονο σύστημα των Διεθνής Ένωση Καθαρής και Εφαρμοσμένης Χημείας (Iupac), κάθε ομάδα ή οικογένεια προσδιορίζεται με έναν αριθμό από το 1 έως το 18, ξεκινώντας από τα αριστερά προς τα δεξιά στον Περιοδικό Πίνακα.
Είναι σημαντικό να τονιστεί ότι το παλιό σύστημα IUPAC υιοθέτησε ένα αλφαριθμητικό σύστημα, με τα γράμματα Α και Β να αναφέρονται στα αντιπροσωπευτικά και μεταβατικά στοιχεία, αντίστοιχα. Επί του παρόντος, αυτός ο τύπος ονοματολογίας δεν χρησιμοποιείται πλέον.
Ονοματολογία οικογενειών του Περιοδικού Πίνακα
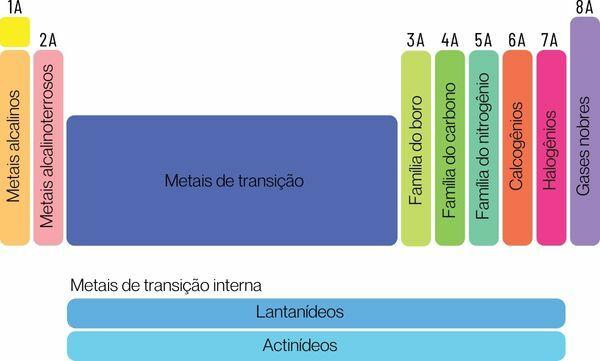
Τα χημικά στοιχεία μπορούν να ταξινομηθούν σε δύο μεγάλες οικογένειες: αντιπροσωπευτικά στοιχεία και μεταβατικά στοιχεία.
→ Αντιπροσωπευτικά στοιχεία του Περιοδικού Πίνακα
Τα αντιπροσωπευτικά στοιχεία χωρίζονται στις ομάδες 1, 2, 13, 14, 15, 16, 17 και 18. Κάθε μία από αυτές τις ομάδες έχει ένα συγκεκριμένο όνομα, με το οποίο μπορεί επίσης να είναι γνωστή. Κοίτα:
Ομάδα 1: οικογένεια των μέταλλα αλκαλική.
Ομάδα 2: οικογένεια των μέταλλα αλκαλικών γαιών.
Ομάδα 13: οικογένεια μετάλλων βορίου ή γαιών.
Ομάδα 14: οικογένεια άνθρακα.
Ομάδα 15: Οικογένεια αζώτου ή Pnicogens.
Ομάδα 16: οικογένεια οξυγόνου ή χαλκογόνων.
Ομάδα 17: οικογένεια των αλογόνα.
Ομάδα 18: οικογένεια των ευγενή αέρια.
→ Στοιχεία μετάβασης Περιοδικού Πίνακα
Εσείς μεταβατικά στοιχείασχηματίζουν μια ενιαία οικογένεια χωρισμένη σε ομάδες 3, 4, 5, 6, 7, 8, 9, 10, 11 και 12. Οι σειρές λανθανιδίων και ακτινιδών αποτελούν επίσης μέρος των μεταβατικών στοιχείων.
Τα μεταβατικά στοιχεία είναι όλα μεταλλικά και έχουν παρόμοιες χημικές ιδιότητες, ακόμη και έχοντας διαφορετικά ηλεκτρόνια στο κέλυφος σθένους και, ως εκ τούτου, θα σχημάτιζε μια ενιαία και μεγάλη οικογένεια μετάλλων μετάπτωσης.
Χημικά στοιχεία από τις οικογένειες του Περιοδικού Πίνακα
Κάθε οικογένεια ή ομάδα αποτελείται από ένα σύνολο χημικών στοιχείων. Δείτε την περιγραφή των χημικών στοιχείων που απαρτίζουν κάθε οικογένεια:
Ομάδα 1:λίθιο, νάτριο, κάλιο, ρουβίνιο, καίσιο, φράγκιο.
Ομάδα 2:βηρύλλιο, μαγνήσιο, ασβέστιο, στρόντιο, βάριο, ραδιόφωνο.
Ομάδα 3:σκάνδιο, ύττριο, σειρά λανθανιδών και σειρά ακτινιδών.
Ομάδα 4: τιτάνιο, ζιρκονίαΟ, άφνιο είναι rutherfordium.
Ομάδα 5:βανάδιο, νιόβιο, ταντάλιο είναι dubnium.
Ομάδα 6:χρώμιο, μολυβδαίνιο, βολφράμιο είναι seaborgium.
Ομάδα 7:μαγγάνιο, τεχνήτιο, ρήνιο είναι bohrio.
Ομάδα 8: σίδερο, ρουθήνιο, ωσμίο είναι χασσίου.
Ομάδα 9:κοβάλτιο, ρόδιο, ιρίδιο και μεϊνέριο.
Ομάδα 10:νικέλιο, παλλάδιο, πλατίνα και darmstadtio.
Ομάδα 11: χαλκός, ασήμι, χρυσός και ρεντγένιο.
Ομάδα 12:ψευδάργυρος, κάδμιο, Ερμής και Κοπέρνικος.
Ομάδα 13: βόριο, αλουμίνιο, γάλλιο, ίνδιο και θάλλιο.
Ομάδα 14: άνθρακας, πυρίτιο, γερμάνιο, κασσίτερος, οδηγω και φλερόβιο.
Ομάδα 15:άζωτο, φώσφορο, αρσενικό, αντιμόνιο είναι βισμούθιο.
Ομάδα 16:οξυγόνο, θείο, σελήνιο, τελλούριο, πολώνιο και λιβερμόριο.
Ομάδα 17: φθόριο, χλώριο, βρώμιο, ιώδιο και αστάτινος.
Ομάδα 18:ήλιο, νέο, αργόν, κρυπτόν, ξένο είναι ραδόνιο.
Σπουδαίος: το χημικό στοιχείο υδρογόνο είναι μια ιδιαίτερη περίπτωση, γιατί παρόλο που βρίσκεται δίπλα στην ομάδα 1, δεν ανήκει στην οικογένεια των αλκαλιμετάλλων, καθώς δεν έχει παρόμοιες χημικές ιδιότητες.
Μάθετε περισσότερα: Ποια είναι τα ραδιενεργά στοιχεία στον Περιοδικό Πίνακα;
Κύρια χαρακτηριστικά των οικογενειών του Περιοδικού Πίνακα
→ Ομάδα 1 ή οικογένεια αλκαλικών μετάλλων
Είναι μεταλλικά στερεά, γυαλιστερά και λεία.
Έχουν υψηλή θερμική αγωγιμότητα και υψηλή Ηλεκτρική αγωγιμότητα.
έχω θερμοκρασίες σχετικά χαμηλή τήξη.
Είναι εξαιρετικά αντιδραστικά με νερό.
Τάση σχηματισμού μονοσθενών κατιόντων (φόρτιση +1).
→ Ομάδα 2 ή οικογένεια μετάλλων αλκαλικών γαιών
Είναι μεταλλικά στερεά, γυαλιστερά και πιο σκληρά σε σύγκριση με τα αλκαλικά μέταλλα.
Οξειδώνονται εύκολα.
Έχουν υψηλή θερμική αγωγιμότητα και υψηλή ηλεκτρική αγωγιμότητα.
Έχουν ελαφρώς υψηλότερες θερμοκρασίες τήξης σε σύγκριση με τα αλκαλικά μέταλλα.
Αντιδρούν με το νερό.
Τάση σχηματισμού δισθενών κατιόντων (φόρτιση +2).
→ Ομάδες 3 έως 12 ή οικογένεια μετάλλων μετάπτωσης
Είναι η μεγαλύτερη οικογένεια στον Περιοδικό Πίνακα.
Σκληρά, γυαλιστερά μεταλλικά στερεά.
Έχουν υψηλή θερμική αγωγιμότητα και υψηλή ηλεκτρική αγωγιμότητα.
Πυκνός.
Υψηλές θερμοκρασίες τήξης.
μπορεί να παρουσιάζονται διαφορετικά καταστάσεις οξείδωσης.
→ Ομάδα 13 ή οικογένεια βορίου
Έχουν ενδιάμεσες ιδιότητες μεταξύ των ιδιοτήτων των μετάλλων και όχι μέταλλα.
Είναι στερεά υπό συνθήκες περιβάλλοντος.
Τάση σχηματισμού τρισθενών κατιόντων (φόρτιση +3).
→ Ομάδα 14 ή οικογένεια άνθρακα
Έχουν ενδιάμεσες ιδιότητες μεταξύ των ιδιοτήτων των μετάλλων και των μη μετάλλων.
Είναι στερεά υπό συνθήκες περιβάλλοντος.
Τάση σχηματισμού τεσσάρων δεσμών.
Είναι στερεά υπό συνθήκες περιβάλλοντος.
Ο άνθρακας και το πυρίτιο μπορούν να σχηματίσουν δεσμούς αλυσίδας.
→ Ομάδα 15 ή οικογένεια αζώτου
Έχουν ενδιάμεσες ιδιότητες μεταξύ των ιδιοτήτων των μετάλλων και των μη μετάλλων.
Στερεά υπό συνθήκες περιβάλλοντος, με εξαίρεση το άζωτο, που είναι αέριο.
Το άζωτο και ο φώσφορος είναι θεμελιώδεις για τους ζωντανούς οργανισμούς.
Το αρσενικό είναι πολύ τοξικό.
→ Ομάδα 16 ή οικογένεια οξυγόνου (χαλκογόνα)
Έχουν διαφορετικές ιδιότητες, αλλάζουν από μη μεταλλικό σε μεταλλικό στοιχείο καθώς πηγαίνετε κάτω από την οικογένεια.
Στερεά υπό συνθήκες περιβάλλοντος, με εξαίρεση το οξυγόνο, που είναι αέριο.
Τάση σχηματισμού δισθενών ανιόντων (φόρτιση -2).
→ Ομάδα 17 ή οικογένεια αλογόνων
Είναι αμέταλλα.
Αρκετά αντιδραστικό.
Κακοί θερμικοί και ηλεκτρικοί αγωγοί.
Υπό συνθήκες περιβάλλοντος, το φθόριο και το χλώριο υπάρχουν ως αέρια, το βρώμιο είναι υγρό και το ιώδιο στερεό.
Τάση σχηματισμού μονοσθενών ανιόντων (φόρτιση -1).
→ Ομάδα 18 ή οικογένεια ευγενών αερίων
Είναι αμέταλλα.
Πολύ λίγο αντιδραστικά, επομένως μπορούν να ονομαστούν αδρανή αέρια.
Υπάρχουν με τη μορφή αερίων.
Δεν έχουν τάση σχηματισμού ιόντων.
Περιοδικός Πίνακας και ηλεκτρονική διανομή
Τα χημικά στοιχεία που ανήκουν στην ίδια οικογένεια ή ομάδα έχουν παρόμοιες χημικές ιδιότητες επειδή έχουν ίσος αριθμός ηλεκτρονίων στο φλοιό σθένους.
Ο αριθμός των ηλεκτρονίων στο φλοιό σθένους είναι σχετικός, καθώς καθορίζει την τάση για σχηματισμό κατιόντων ή ανιόντα, τον τύπο του χημικού δεσμού που θα σχηματιστεί, την ενέργεια που εμπλέκεται στις χημικές αντιδράσεις, μεταξύ άλλων Χαρακτηριστικά. Για να βρείτε τον αριθμό των ηλεκτρονίων σθένους, είναι απαραίτητο να γνωρίζουμε το ατομικός αριθμός του στοιχείου και εκτελέστε σας ηλεκτρονική διανομή.
→ Ηλεκτρονική κατανομή αντιπροσωπευτικών στοιχείων
Τα αντιπροσωπευτικά στοιχεία έχουν τα πιο ενεργητικά ηλεκτρόνια τους σε υποεπίπεδα μικρό είναι Π του ηλεκτρονικού στρώματος (n). Ο παρακάτω πίνακας συγκεντρώνει τις ηλεκτρονικές διαμορφώσεις που σχετίζονται με κάθε οικογένεια αντιπροσωπευτικών στοιχείων. ο όρος n κυμαίνεται από 1 έως 7 και αντιπροσωπεύει το επίπεδο ενέργειας που καταλαμβάνουν τα ηλεκτρόνια σθένους, που ισοδυναμεί με την περίοδο (οριζόντια γραμμή) του Περιοδικού Πίνακα στην οποία βρίσκεται το στοιχείο.
Ηλεκτρονική διανομή αντιπροσωπευτικών στοιχείων | ||
οικογένεια ή ομάδα |
Ηλεκτρονική διανομή |
Παράδειγμα |
1 |
μας1 |
Li (Z=3): 1 δευτ2 2s1 |
2 |
μας2 |
Be (Z=4): 1s2 2s2 |
13 |
μας2 np1 |
Β (Ζ=5): 1δ2 2s22π1 |
14 |
μας2 np2 |
C (Z=6): 1s2 2s22π2 |
15 |
μας2 np3 |
Ν (Ζ=7): 1δ2 2s22π3 |
16 |
μας2 np4 |
O (Z=8): 1s2 2s22π4 |
17 |
μας2 np5 |
F (Z=9): 1s2 2s22π5 |
18 |
μας2 np6 |
Νε (Ζ=10): 1δ2 2s22π6 |
→ Ηλεκτρονική κατανομή μεταβατικών στοιχείων
Τα μεταβατικά στοιχεία κατανέμονται μεταξύ των ομάδων 3 και 12 και έχουν τα υποεπίπεδα ρε είναι φά καταλαμβάνεται από ηλεκτρόνια σθένους:
Εξωτερικά μεταβατικά στοιχεία: κρατήστε τα ηλεκτρόνια σθένους στο υποεπίπεδο ρε, διατηρώντας τη διαμόρφωση ηλεκτρονίων ίση με μας2 (n-1)d(1 έως 8). Για παράδειγμα, το στοιχείο νικέλιο (Z = 28) ανήκει στην ομάδα 10 και η διαμόρφωσή του είναι 1s2 2s2 2π6 3s2 3π6 4s2 3d8.
Εσωτερικά μεταβατικά στοιχεία: αποτελούν μέρος της ομάδας 3, αλλά είναι «εσωτερικά» στον Περιοδικό Πίνακα, επεκτείνοντας κάτω από αυτόν, στις περιόδους 6 (λανθανίδες) και 7 (ακτινίδες). Αυτά τα στοιχεία έχουν ηλεκτρόνια σθένους που καταλαμβάνουν το υποκέλυφος φά και γενική ηλεκτρονική διαμόρφωση του μας2 (n-2)f(1 έως 13). Για παράδειγμα, το στοιχείο λανθάνιο (Z = 57) είναι το πρώτο στοιχείο στη σειρά των λανθανιδών και η διαμόρφωση ηλεκτρονίων του είναι 1s2 2s2 2π6 3s2 3π6 4s2 3d10 4σ6 5s2 4δ10 5π6 6 δευτ2 4στ1.
Γνωρίστε επίσης:Ποια είναι η προέλευση του Περιοδικού Πίνακα;
Λυμένες ασκήσεις για τις οικογένειες του Περιοδικού Πίνακα
ερώτηση 1
(UFC — προσαρμοσμένο) Όσον αφορά τη σύγχρονη περιοδική ταξινόμηση στοιχείων, σημειώστε την αληθινή δήλωση:
Α) Στον Περιοδικό Πίνακα, οι οικογένειες ή οι ομάδες αντιστοιχούν σε οριζόντιες γραμμές.
Β) Τα στοιχεία μιας οικογένειας έχουν πολύ διαφορετικές χημικές ιδιότητες.
Γ) Σε μια οικογένεια, τα στοιχεία έχουν γενικά τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο κέλυφος.
Δ) Σε μια περίοδο, τα στοιχεία έχουν παρόμοιες χημικές ιδιότητες.
Ε) Τα αντιπροσωπευτικά στοιχεία κατανέμονται στις ομάδες 3 έως 12.
Ανάλυση:
Εναλλακτική Γ
Το στοιχείο Α είναι λάθος: οι οικογένειες ή οι ομάδες είναι οι στήλες (κάθετες γραμμές) του Περιοδικού Πίνακα.
Εσφαλμένο στοιχείο Β και Δ: Σε μια οικογένεια, τα στοιχεία έχουν παρόμοιες χημικές ιδιότητες. Σε περιόδους, τα στοιχεία έχουν το ίδιο κέλυφος ηλεκτρονίων που καταλαμβάνεται από ηλεκτρόνια σθένους.
Σωστό στοιχείο Γ: Σε μια οικογένεια, τα στοιχεία έχουν τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο φλοιό.
Στοιχείο Ε λάθος: αντιπροσωπευτικά στοιχεία είναι οι ομάδες 1, 2, 13, 14, 15, 16, 17 και 18. Τα μεταβατικά στοιχεία κατανέμονται στις ομάδες 3 έως 12.
Ερώτηση 2
(EAM) Τα στοιχεία A, B και C έχουν τις ακόλουθες διαμορφώσεις ηλεκτρονίων στα κελύφη σθένους τους:
Α: 3 δευτ1
Β: 4 δευτ2 4σ4
Γ: 3 δευτ2
Με βάση αυτές τις πληροφορίες, επιλέξτε τη σωστή επιλογή.
Α) Το στοιχείο Α είναι αλκαλικό μέταλλο.
Β) Το στοιχείο Β είναι αλογόνο.
Γ) Το στοιχείο Γ είναι ένα χαλκογόνο.
Δ) Τα στοιχεία Α και Β ανήκουν στην τρίτη περίοδο του Περιοδικού Πίνακα.
Ε) Τα τρία στοιχεία ανήκουν στην ίδια ομάδα του Περιοδικού Πίνακα.
Ανάλυση:
Εναλλακτική Α
Σωστό στοιχείο Α: το στοιχείο Α έχει ηλεκτρονική κατανομή που περιέχει μόνο ένα ηλεκτρόνιο σθένους, επομένως ανήκει στην ομάδα 1 του Περιοδικού Πίνακα.
Λανθασμένο στοιχείο Β: το στοιχείο Β έχει διαμόρφωση ηλεκτρονίων 4s2 4σ4, υποδεικνύοντας ότι υπάρχουν 6 ηλεκτρόνια στο τελευταίο κέλυφος και ότι αυτό το στοιχείο ανήκει στην ομάδα 16 (χαλκογόνα).
Λανθασμένο στοιχείο Γ: το στοιχείο Γ έχει ηλεκτρονική διαμόρφωση με 2 ηλεκτρόνια στο τελευταίο φλοιό, επομένως είναι στοιχείο της ομάδας 2 του πίνακα.
Λανθασμένο στοιχείο Δ: το στοιχείο Α ανήκει στην τρίτη περίοδο (n = 3) και το στοιχείο Β ανήκει στην τέταρτη περίοδο (n = 4).
Λανθασμένο στοιχείο Ε: τα τρία στοιχεία έχουν διαφορετικές ποσότητες ηλεκτρονίων στο τελευταίο κέλυφος, επομένως δεν μπορούν να ανήκουν στην ίδια οικογένεια.
Της Ana Luiza Lorenzen Lima
Καθηγητής Χημείας
Πηγή: Σχολείο Βραζιλίας - https://brasilescola.uol.com.br/quimica/familias-da-tabela-periodica.htm
