Πολυμερισμός είναι το όνομα της χημικής διαδικασίας που έχει ως αποτέλεσμα το σχηματισμό μακρομορίων (μεγάλων μορίων) που ονομάζονται πολυμερή, μέσω του συνδυασμού μικρότερων μορίων, των μονομερών.
η αντίδραση του πολυμερισμός είναι πολύ κοινό στη φύση, όπως μπορούμε να δούμε στους υδατάνθρακες (όπως το άμυλο) και τις πρωτεΐνες (όπως η καζεΐνη στο γάλα). Εμφανίζεται επίσης συνθετικά, καθώς η συντριπτική πλειονότητα των πολυμερών που χρησιμοποιούνται από τον άνθρωπο στην καθημερινή του ζωή είναι κατασκευασμένα τεχνητά.
Το πρώτο πολυμερές που παράγεται από πολυμερισμός συνθετικός ήταν ο βακελίτης, το 1909, από τον Βέλγο χημικό Leo Hendrik Baekeland.
Γενικά, για να συνδυαστεί ένα μονομερές με ένα άλλο (είτε είναι ίδιο είτε διαφορετικό) σε μια αντίδραση πολυμερισμός, είναι απαραίτητη η ύπαρξη ελεύθερου σθένους (να εκτελεστεί χημικός δεσμός) και στα δύο μονομερή.
Αυτά τα σθένη προκύπτουν ως αποτέλεσμα της θραύσης των δεσμών, μέσω της χρήσης καταλυτών (όπως το νικέλιο), εξωτερικές συνθήκες όπως το φως και η θερμότητα ή από το φαινόμενο του συντονισμού στη δομή (μετατόπιση ηλεκτρονίων).
Στον σχηματισμό πολυπροπυλενίου (πολυμερές PP), για παράδειγμα, που χρησιμοποιείται σε οικιακά σκεύη και παιχνίδια, σύνδεσμος pi (π) σε κάθε μόριο αναλύεται ως εξής:
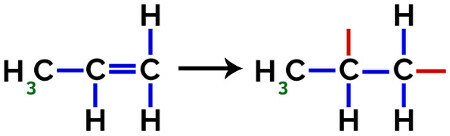
Σπάσιμο του δεσμού pi στο προπυλένιο
Έτσι, κάθε μονομερές προπυλενίου μπορεί να συνδεθεί με δύο άλλα μονομερή προπυλενίου και να σχηματίσει το πολυμερές PP ή πολυπροπυλένιο (το πρόθεμα πολυ υποδεικνύει πολλές μονομερείς μονάδες). Ο πιο συχνός τρόπος αναπαράστασης ενός πολυμερούς έχει το μονομερές ανάμεσα στις παρενθέσεις και, εξωτερικά, το γράμμα n, το οποίο υποδεικνύει πολλά μονομερή, όπως μπορούμε να δούμε στην περίπτωση του πολυμερούς PP:
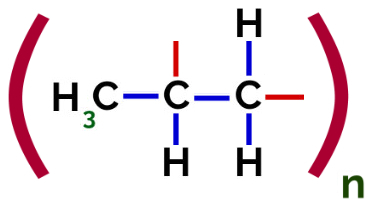
Αναπαράσταση πολυμερούς ΡΡ
η αντίδραση του πολυμερισμός μπορεί να γίνει με διάφορους τρόπους, όπως θα δούμε παρακάτω:
α) Αντίδραση του πολυμερισμός προσθήκης
Σε αυτό πολυμερισμός, υπάρχει πάντα μια θραύση ενός δεσμού pi στο μονομερές, που προκαλεί την εμφάνιση δύο ελεύθερων σθένων στη δομή, όπως στο σχηματισμό του πολυαιθυλένιο, πολυμερές που χρησιμοποιείται ευρέως στις φαρμακευτικές συσκευασίες.
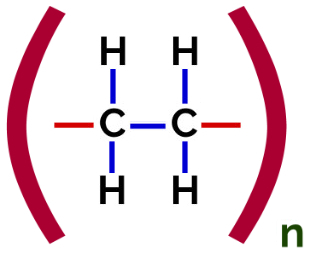
Δομικός τύπος πολυμερούς προσθήκης πολυαιθυλενίου
Στο πολυμερισμός του πολυαιθυλενίου, μόρια αιθυλενίου (αιθενίου), τα οποία έχουν δεσμό pi μεταξύ των δύο ατόμων άνθρακα, χρησιμοποιούνται ως μονομερές. Όταν αυτός ο δεσμός σπάσει, εμφανίζονται δύο ελεύθερα σθένη, ένα σε κάθε άτομο άνθρακα που εμπλέκεται στον δεσμό pi. Τα μονομερή ενώνονται ακριβώς σε καθένα από αυτά τα σθένη, δηλαδή το σθένος του ενός συνδέεται με το σθένος του άλλου κ.ο.κ.
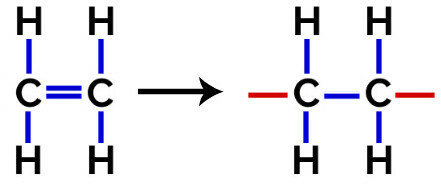
Εξίσωση Σχηματισμού Πολυαιθυλενίου
β) Αντίδραση πολυμερισμού προσθήκης 1.4
Σε αυτόν τον πολυμερισμό, τα μονομερή παρουσιάζουν δύο εναλλασσόμενους διπλούς δεσμούς (ένας pi και ένα σίγμα), γεγονός που ευνοεί το φαινόμενο συντονισμού (εναλλαγή της θέσης των ηλεκτρονίων pi του δεσμού pi), όπως στο σχηματισμό συνθετικού καουτσούκ (πολυβουταδιένιο)

Δομικός τύπος πολυβουταδιενίου
Η μονομερής μονάδα αυτού του πολυμερούς είναι το βουταδιένιο, το οποίο έχει δύο εναλλασσόμενους διπλούς δεσμούς. Με συντονισμό, η δομή έχει διπλό δεσμό μεταξύ των ανθράκων 2 και 3 και δύο ελεύθερα σθένη στους άνθρακες 1 και 4. Ακριβώς σε αυτά τα ελεύθερα σθένη των ανθράκων 1 και 4 συνδυάζονται τα μονομερή.

Συντονισμός βουταδιενίου
γ) Αντίδραση του πολυμερισμός συμπύκνωσης ή εξάλειψη
Είναι μια αντίδραση του πολυμερισμός στην οποία, υποχρεωτικά, δύο μονομερή (ίδια ή διαφορετικά) χάνουν ταυτόχρονα άτομα ή ομάδες, με αποτέλεσμα δύο ελεύθερα σθένη σε καθένα από αυτά. Με αυτόν τον τρόπο, υπάρχει πάντα η απομάκρυνση του υδρογόνου από ένα μονομερές, το οποίο στη συνέχεια ενώνεται με ένα αλογόνο (F, Cl, Br, I), OH, NH2ή στο CN του άλλου μονομερούς.
Έτσι, στο πολυμερισμός με την αποβολή, υπάρχει πάντα ο σχηματισμός νερού, αλογονωμένου οξέος (HCl, HI, HF, HBr), αμμωνίας (NH3) ή υδροκυανικό οξύ (HCN) επιπλέον του πολυμερούς. Δείτε, για παράδειγμα, την αναπαράσταση του σχηματισμού πολυεστέρα, ενός υλικού που χρησιμοποιείται ως ύφασμα:

Εξίσωση Σχηματισμού Πολυεστέρα
Τα μονομερή που σχηματίζουν πολυεστέρα είναι το π-βενζολοδιοϊκό οξύ και η αιθανο-1,2-διόλη. Μπορούμε να το παρατηρήσουμε σε αυτό πολυμερισμός γίνεται η αποβολή των μορίων του νερού, αφού τα δύο μονομερή έχουν δύο υδροξύλια. Σε αυτή τη διαδικασία, το οξύ χάνει τα δύο υδροξύλια και η διαλκοόλη χάνει μόνο το υδρογόνο από τα υδροξύλια της:

Πολυεστερική δομή
Τα πολυεστερικά μονομερή ενώνονται με το οξυγόνο στην αλκοόλη και τον άνθρακα στο καρβοξυλικό οξύ.
Από εμένα Diogo Lopes Dias
Πηγή: Σχολείο Βραζιλίας - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm

