Εξάτμιση είναι η μετάβαση από την υγρή κατάσταση στην αέρια κατάσταση. Εμφανίζεται στην ελεύθερη επιφάνεια των υγρών, αργά και σταδιακά, σε οποιαδήποτε θερμοκρασία.
Όταν μια ουσία βρίσκεται σε υγρή κατάσταση, έχει χαμηλότερη συνεκτική δύναμη μεταξύ των ατόμων της από ό, τι όταν βρίσκεται σε στερεά κατάσταση.
Σε αυτήν την κατάσταση, τα μόρια διαχωρίζονται περαιτέρω, σε συνεχή ανάδευση και κινούνται μέσα στο υγρό με διαφορετικές ταχύτητες.
Με αυτόν τον τρόπο, τα σωματίδια με μεγαλύτερη ταχύτητα, όταν φτάσουν στην ελεύθερη επιφάνεια του υγρού, καταφέρνουν να διαφύγουν, περνώντας στην αέρια κατάσταση.

Ταχύτητα εξάτμισης
Υπάρχουν παράγοντες που επηρεάζουν την ταχύτητα με την οποία συμβαίνει η εξάτμιση, είναι:
- Θερμοκρασία: όσο υψηλότερη είναι η θερμοκρασία, τόσο πιο γρήγορη είναι η ταχύτητα εξάτμισης. Επειδή όσο υψηλότερη είναι η θερμοκρασία, τόσο υψηλότερη κινητική ενέργεια των σωματιδίων. Με αυτόν τον τρόπο, περισσότερα σωματίδια θα ξεφύγουν από την επιφάνεια του υγρού.
- Φύση του υγρού: υπάρχουν ουσίες που εξατμίζονται πιο εύκολα, ονομάζονται πτητικές ουσίες. Ο αιθέρας, το αλκοόλ και η ακετόνη είναι παραδείγματα πτητικών ουσιών.
- ελεύθερη επιφάνεια: καθώς η εξάτμιση πραγματοποιείται στην ελεύθερη επιφάνεια υγρών, όσο μεγαλύτερη είναι η επιφάνεια, τόσο μεγαλύτερη είναι η ποσότητα σωματιδίων που θα αφήσουν το υγρό.
- Συγκέντρωση ατμών σε υγρό: όσο μεγαλύτερη είναι η ποσότητα ατμού, τόσο χαμηλότερος είναι ο ρυθμός εξάτμισης.
- Πίεση στο υγρό: όσο υψηλότερη είναι η πίεση, τόσο χαμηλότερη είναι η ταχύτητα εξάτμισης.
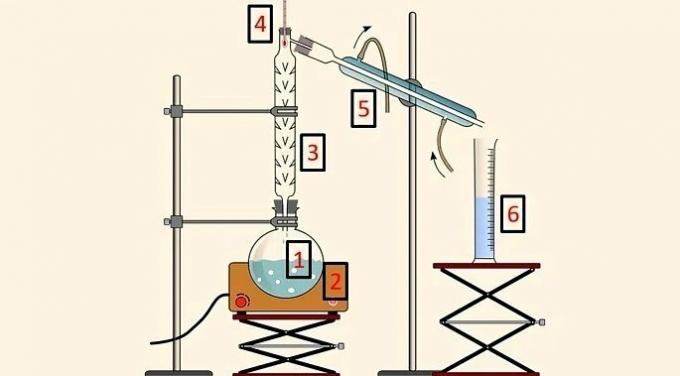
Διαφορά μεταξύ εξάτμισης και βρασμού
Και η εξάτμιση και βρασμός αντιπροσωπεύουν την αλλαγή από την υγρή κατάσταση στην αέρια κατάσταση. Ωστόσο, ενώ η εξάτμιση γίνεται σταδιακά, ο βρασμός συμβαίνει γρήγορα.
Για να συμβεί βρασμός, είναι απαραίτητο το υγρό να φτάσει, για μια δεδομένη πίεση, σε μια συγκεκριμένη θερμοκρασία, που ονομάζεται σημείο βρασμού. Η εξάτμιση μπορεί να συμβεί σε οποιαδήποτε θερμοκρασία.
Διαχωρισμός μιγμάτων
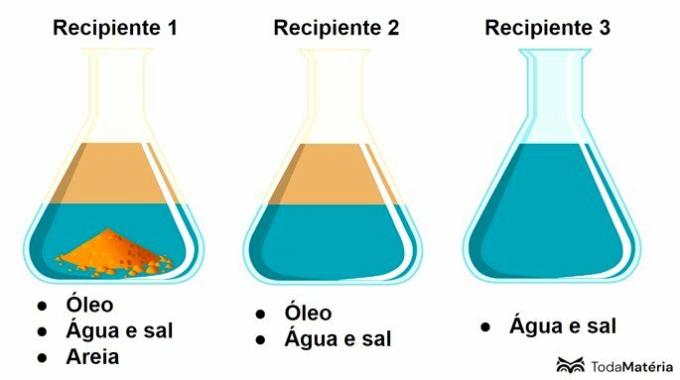
Η κλασματική κρυστάλλωση είναι μια διαδικασία διαχωρισμού ετερογενών μιγμάτων. Χρησιμοποιείται όταν οι ουσίες που συνθέτουν το μείγμα βρίσκονται σε στερεά κατάσταση.
Σε αυτήν τη διαδικασία, ένα μείγμα που διαλύει όλα τα στερεά συστατικά προστίθεται στο μείγμα. Τα συστατικά στη συνέχεια κρυσταλλώνονται ξεχωριστά μετά την εξάτμιση του διαλύματος.
Αυτή η διαδικασία χρησιμοποιείται, για παράδειγμα, σε κατσαρόλες με αλάτι για να ληφθούν άλατα από θαλασσινό νερό.

Εξάτμιση και κύκλος νερού
Η εξάτμιση είναι μία από τις διαδικασίες που αποτελούν το ο κύκλος του νερού. Η ενέργεια από τον Ήλιο θερμαίνει την ελεύθερη επιφάνεια λιμνών, ποταμών, θάλασσας και ωκεανών.
Αυτή η θέρμανση αναγκάζει μέρος του νερού να εξατμιστεί σε κατάσταση ατμού. Αυτό, όταν φτάσει στα υψηλότερα στρώματα της ατμόσφαιρας, ψύχει και συμπυκνώνει σχηματίζοντας σύννεφα.
Όταν συμβαίνει καθίζηση, το νερό επιστρέφει στην επιφάνεια σε υγρή μορφή, διεισδύοντας στο έδαφος και σχηματίζοντας υπόγεια φύλλα.
Μέρος αυτού του νερού απορροφάται από φυτά, τα οποία επιστρέφουν τους υδρατμούς στην ατμόσφαιρα με διαπνοή.
αλλαγές φάσης
Η αλλαγή από υγρό σε αέρια κατάσταση ονομάζεται γενικά εξάτμιση, καθώς περιλαμβάνει, εκτός από την εξάτμιση, δύο άλλες διαδικασίες: βρασμό και θέρμανση.
Υπάρχουν ακόμα άλλες διαδικασίες αλλαγής της κατάστασης. Είναι αυτοί:
- Σύντηξη
- Στερεοποίηση
- Ρευστοποίηση ή συμπύκνωση
- Εξάχνιση
Στο παρακάτω διάγραμμα αντιπροσωπεύουμε τα τρία φυσικές καταστάσεις της ύλης και τις αντίστοιχες αλλαγές κατάστασης:
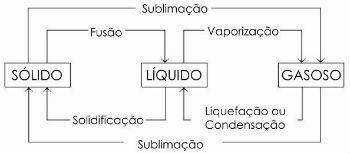
Μάθετε περισσότερα στο: Αλλαγές φυσικής κατάστασης.