Ο οζονόλυση Είναι ένας τύπος αποτελεσματικής αντίδρασης για την οξείδωση μιας ακόρεστης ένωσης με τη διάσπαση του διπλού δεσμού της. Είναι εκεί εκεί συμβαίνει μεταξύ a αλκένιο (αλκένιο) και όζον (O3), ως οξειδωτικό μέσο. Στη συνέχεια, εμφανίζεται υδρόλυση όταν αντιδρά με το νερό (H2O) παρουσία σκόνης ψευδαργύρου ή αρχειοθέτησης ψευδαργύρου (Zn) ως καταλύτες, σχηματίζοντας τα κύρια προϊόντα: αλδεΰδες και / ή κετόνες, εκτός από το υπεροξείδιο του υδρογόνου (H2O2).
Με απλοποιημένο τρόπο μπορούμε να το πούμε αυτό η οζονόλυση είναι μια αντίδραση με το όζον που ακολουθείται από υδρόλυση. Η χημική της εξίσωση γράφεται ως εξής, λαμβάνοντας υπόψη ένα γενικό αλκένιο:
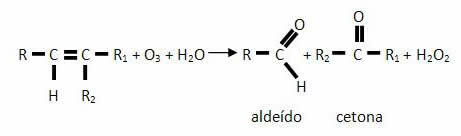
Ακριβώς λόγω του σχηματισμού υπεροξειδίου του υδρογόνου εισάγεται σκόνη ψευδαργύρου, καθώς καταστρέφει το νερό Σχηματίζεται οξυγόνο, εμποδίζοντας το οξυγόνο που μπορεί να παραχθεί από την αποσύνθεσή του να οξειδώσει την αλδεΰδη σε οξύ καρβοξυλικό οξύ.
Αυτή η αντίδραση σχηματίζει πρώτα μια σταθερή ενδιάμεση ένωση που ονομάζεται α όζο ή οζονίδιο
ή ακόμα όζο. Αυτό είναι προϊόν της σύνδεσης ατόμων οξυγόνου στο όζον με τους άνθρακες που σχηματίζουν τον διπλό δεσμό του αλκενίου. Το όζον είναι μια ασταθής και εκρηκτική ένωση.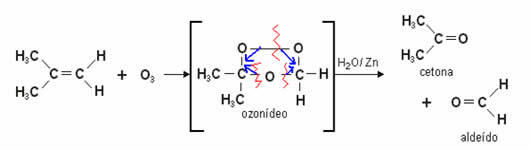
Παρατηρούμε ότι ο διπλός δεσμός άνθρακα-άνθρακα (C = C) έχει σπάσει και αρχίζουν να συμμετέχουν του διπλού δεσμού με οξυγόνο (C = O) στις νεοσυσταθείσες ουσίες που μπορεί να είναι αλδεΰδες ή κετόνες.
Το να γνωρίζουμε αν θα συμβεί ο σχηματισμός αλδεϋδών ή κετονών εξαρτάται από το αρχικό μόριο αλκενίου, δηλαδή, εξαρτάται από τη θέση του διπλού στο αλκένιο και από το αν ο άνθρακας που συνδέεται με τον διπλό δεσμό είναι πρωτογενής, δευτερεύων ή τριτογενής. Επιπλέον, η άγνωστη δομή του αλκενίου μπορεί επίσης να προσδιοριστεί από τα προϊόντα που σχηματίζονται. Έχουμε λοιπόν τον ακόλουθο κανόνα:
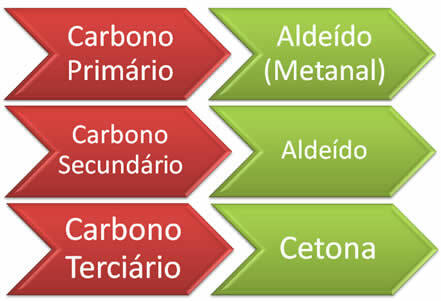
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Σχολική ομάδα της Βραζιλίας
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/ozonolise-alcenos.htm
