Ένας από τους τρόπους οργάνωσης των χημικών στοιχείων είναι μέσω οικογενειών, που αντιστοιχούν στις κάθετες ακολουθίες του περιοδικού πίνακα.
Στο 18 στήλες του πίνακα ομαδοποιεί τα στοιχεία σύμφωνα με ομοιότητες στις χημικές ιδιότητες.
Η οργάνωση χημικών στοιχείων σε οικογένειες ήταν ένας πρακτικός τρόπος δομής των διαφόρων πληροφοριών που βρέθηκαν και παρουσίασής τους με απλό τρόπο.
Για να διευκολυνθεί η θέση ενός χημικού στοιχείου, οι οικογένειες ορίστηκαν σε αριθμούς από 1 έως 18 ως εξής:
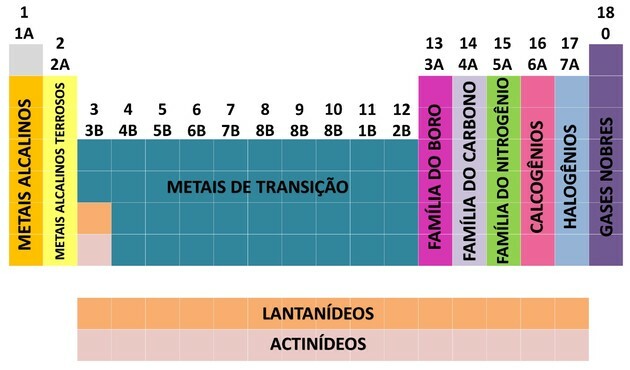
Μέσω της συμβολής πολλών επιστημόνων και διαφόρων προσπαθειών για την τακτοποίηση των δεδομένων, ο περιοδικός πίνακας εξελίχθηκε, δημιουργώντας μια σειρά για την οργάνωση των στοιχείων.
Ονοματολογία των οικογενειών
- Οι οικογένειες στον πίνακα χωρίστηκαν σε Α (εκπρόσωπος) και Β (μετάβαση), προσδιοριζόμενες με γράμματα και αριθμούς.
- Εσείς αντιπροσωπευτικά στοιχεία Οι οικογένειες 0, 1A, 2A, 3A, 4A, 5A, 6A και 7A αντιστοιχούν.
- Εσείς μεταβατικά στοιχεία Οι οικογένειες 1B, 2B, 3B, 4B, 5B, 6B, 7B και 8B αντιστοιχούν.
- Με τον προσδιορισμό της Διεθνούς Ένωσης Καθαρής και Εφαρμοσμένης Χημείας (IUPAC), οι οικογένειες εντοπίστηκαν στο ομάδες από 1 έως 18.
Περιοδικός πίνακας και ηλεκτρονική διανομή
Οι ομοιότητες μεταξύ των στοιχείων της ίδιας οικογένειας συμβαίνουν επειδή ο αριθμός των ηλεκτρονίων σθένους του ατόμου στην κατάσταση γείωσης είναι ο ίδιος για τα μέλη μιας συγκεκριμένης ομάδας.
Για παράδειγμα:
| Ομάδα 1 | Ηλεκτρονική διανομή |
|---|---|
| 3ανάγνωση | 2-1 |
| 11Στο | 2-8-1 |
| 19κ | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Πρ | 2-8-18-32-18-8-1 |
Τα άτομα της ομάδας 1 έχουν τα ηλεκτρόνια τους κατανεμημένα σε περισσότερα από ένα επίπεδα ενέργειας, αλλά όλα έχουν ένα ηλεκτρόνιο σθένους.
Με αυτό, παρατηρούμε ότι κάνοντας το ηλεκτρονική διανομή του ατόμου στην κατάσταση του εδάφους, βρίσκουμε τη θέση του στον περιοδικό πίνακα.
αντιπροσωπευτικά στοιχεία
Τα αντιπροσωπευτικά στοιχεία εμφανίζουν σχετικά λιγότερο περίπλοκη χημική συμπεριφορά από τα μεταβατικά στοιχεία και σχηματίζουν τις περισσότερες ουσίες γύρω μας.
Ορισμένες από τις αντιπροσωπευτικές οικογένειες στοιχείων έχουν ειδικά ονόματα, όπως φαίνεται παρακάτω:
Ομάδα |
Οικογένεια | συγκεκριμένο όνομα | Προέλευση ονόματος | Στοιχεία | ηλεκτρονική διαμόρφωση |
|---|---|---|---|---|---|
| 1 | 1Α | αλκαλι μέταλλα | από λατινικά αλκαλίο, που σημαίνει "γκρι φυτών". | Li, Na, K, Rb, Cs και Fr | μας1 |
| 2 | 2Α | μέταλλα αλκαλικών γαιών | Ο όρος "γήινος" αναφέρεται στο "υπάρχον στη γη". | Be, Mg, Ca, Sr, Ba και Ra | μας2 |
| 13 | 3Α | οικογένεια βορίου | Όνομα του πρώτου στοιχείου της οικογένειας. | B, Al, Ga, In, Tl και Nh. | μας2np1 |
| 14 | 4Α | οικογένεια άνθρακα | Όνομα του πρώτου στοιχείου της οικογένειας. | C, Si, Ge, Sn, Pb και Fl. | μας2np2 |
| 15 | 5Α | Οικογένεια αζώτου | Όνομα του πρώτου στοιχείου της οικογένειας. | N, P, As, Sb, Bi και Mc. | μας2np3 |
| 16 | 6Α | Χαλκογόνα | από τα ελληνικά χαλκ, καθώς είναι στοιχεία που βρίσκονται στα μεταλλεύματα χαλκού. | O, S, Se, Te, Po και Lv. | μας2np4 |
| 17 | 7Α | Αλογόνα | Ελληνική έκφραση που σημαίνει σχηματιστές αλατιού. | F, Cl, Br, I, At και Ts. | μας2np5 |
| 18 | 0 | Ευγενή αέρια | Θεωρήθηκε ότι δεν αντιδρά με άλλες ουσίες. | Αυτός, Ne, Ar, Kr, Xe, Re και Og. | 1δ2 (Αυτός) ή εμάς2np6 |
Μέσω του πίνακα, μπορούμε να δούμε ότι:
- Τα στοιχεία που παρουσιάζονται παραπάνω ταξινομούνται ως αντιπροσωπευτικά επειδή έχουν το πιο ενεργητικό ηλεκτρόνιο σε ένα δευτερεύον επίπεδο s ή p.
- Τα ηλεκτρόνια κατανέμονται σε επίπεδα ενέργειας και το n αντιπροσωπεύει το εξόχως επίπεδο του ατόμου στην κατάσταση του εδάφους.
- Τα αντιπροσωπευτικά στοιχεία, σύμφωνα με τη σύσταση του IUPAC, ανήκουν στις ομάδες ή τις οικογένειες 1,2,13,14,15,16,17 και 18.
Ο υδρογόνο ταξινομείται εκτός από τα άλλα στοιχεία. Ακόμη και με ηλεκτρονική διαμόρφωση 1s1, δεν ανήκει στην ομάδα 1 για παρουσίαση μιας μοναδικής συμπεριφοράς
μεταβατικά στοιχεία
Τα μεταβατικά στοιχεία αντιστοιχούν στις ομάδες 3 έως 12. Λαμβάνουν αυτό το όνομα επειδή έχουν ενδιάμεσα χαρακτηριστικά μεταξύ των ομάδων 1 και 2 και των αντιπροσωπευτικών μη μεταλλικών στοιχείων.
Εσείς μέταλλα μετάβασης ορίζονται από το IUPAC ως:
Ένα μεταβατικό στοιχείο έχει ένα ημιτελές d sublevel ή μπορεί να σχηματίσει κατιόντα με ένα ατελές d sublevel.
Όταν το πιο ενεργητικό ηλεκτρόνιο του ατόμου κατάστασης εδάφους βρίσκεται σε ένα ατελές υπόστρωμα d, χαρακτηρίζεται ως εξωτερική μετάβαση.
Οι λανθανίδες και τα ακτινίδια είναι στοιχεία εσωτερικής μετάβασης καθώς έχουν τουλάχιστον ένα ελλιπές επίπεδο.
Όταν τα στοιχεία έχουν ηλεκτρόνια που γεμίζουν τα τροχιακά d ή f, παρουσιάζουν παρόμοιες ιδιότητες και μπορούν να ταξινομηθούν σε τροχιακά στοιχεία d ή f. εξωτερική ή εσωτερική μετάβαση.
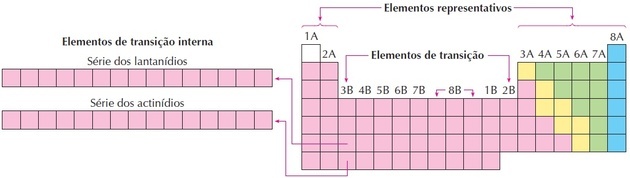
Όπως μπορούμε να δούμε στην εικόνα, η οικογένεια 8Β αντιστοιχεί σε 3 στήλες, είναι ομάδες 8, 9 και 10, οι οποίες ομαδοποιήθηκαν έτσι επειδή έχουν παρόμοια χαρακτηριστικά.
Κύρια χαρακτηριστικά των οικογενειών
Ο παρακάτω πίνακας δείχνει τις κύριες ιδιότητες των ομάδων στον περιοδικό πίνακα:
| Ομάδα | Χαρακτηριστικά | σύνθετες ουσίες πιο συχνό |
περιστατικά |
|---|---|---|---|
| 1 | Στερεό και γυαλιστερό σε συνθήκες περιβάλλοντος. Πολύ αντιδραστικοί, μαλακοί και καλοί αγωγοί ηλεκτρικής ενέργειας. | Άλατα, υδροξείδια και οξείδια |
Αντιδράστε με αλογόνα και σχηματίζετε άλατα. |
| 2 | Λιγότερο αντιδραστικό και πιο δύσκολο από την ομάδα 1. Ασημένια στερεά με καλή αγωγιμότητα. | Άλατα, υδροξείδια και οξείδια |
Σχηματίζοντας άλατα και οξείδια. |
| 3 έως 12 | Σχηματίζουν συγκροτήματα. Είναι μεταλλικά στερεά, σκληρά και εύθραυστα, με εξαίρεση τον υδράργυρο, που είναι υγρό. | Άλατα, οξείδια και σύμπλοκα. Π.χ.: AgNO3, TiO και [Cr (OH)3(Η2Ο)3] |
Στα ορυκτά με τη μορφή οξειδίων. |
| 13 | Στερεά σε συνθήκες περιβάλλοντος, ασήμι, εκτός από το βόριο. | Οξείδια Π.χ.: Β2Ο3 |
Στα ορυκτά με τη μορφή οξειδίων. |
| 14 | Στερεά σε συνθήκες περιβάλλοντος. | Τα άτομα των C και Si μπορούν να τακτοποιηθούν σε αλυσίδες και να παράγουν μια τεράστια ποικιλία ουσιών. | Σε ζωντανούς οργανισμούς και με τη μορφή πυριτικών ή οξειδίων. |
| 15 | Στερεά, εκτός από το άζωτο, το οποίο είναι αέριο υπό συνθήκες περιβάλλοντος. | Οξείδια και οξέα Π.χ.: ΟΧΙ2 και Η3ΣΚΟΝΗ4 |
Ατμόσφαιρα, ζωντανοί οργανισμοί και μέταλλα. |
| 16 | Στερεά, εκτός από το οξυγόνο, το οποίο είναι αέριο υπό συνθήκες περιβάλλοντος. | Σουλφίδια και οξείδια Π.χ.: ZnS και SiO2 |
Ατμόσφαιρα, ζωντανοί οργανισμοί και μέταλλα. |
| 17 | Σχηματίζουν διατομικά μόρια και είναι πολύ αντιδραστικά. Είναι κακοί αγωγοί ηλεκτρισμού και θερμότητας. Είναι επιθετικοί στα ζωντανά όντα και στο περιβάλλον. | Οξέα και άλατα. Π.χ.: HCl και KBr |
Υπάρχουν σε ουσίες οργανικά και μεταλλικά. |
| 18 | Είναι πολύ σταθερά και βρίσκονται με τη μορφή αερίων. | Δεν σχηματίζουν σύνθετες ουσίες. | Αέρια στην ατμόσφαιρα. |
Οι χημικές και φυσικές ιδιότητες διακρίνουν τη μια οικογένεια από την άλλη. Όπως έχουμε δει, οι χημικές ιδιότητες σχετίζονται με ηλεκτρόνια του σθένους, και μέσω αυτών, ένα άτομο αλληλεπιδρά με ένα άλλο, είναι υπεύθυνο για τη χημική συμπεριφορά και χημικοί δεσμοί σχηματίστηκε.
Οι φυσικές ιδιότητες των στοιχείων στην ίδια ομάδα μπορούν να ποικίλουν ανάλογα με τον ατομικό αριθμό και τη μάζα.
Γυμνάσια
Τώρα που γνωρίζετε περισσότερα για τις οικογένειες Περιοδικού Πίνακα, δοκιμάστε τις γνώσεις σας και δείτε τι έχετε μάθει.
1) Εξετάστε το ακόλουθο απόσπασμα από τον Περιοδικό Πίνακα.
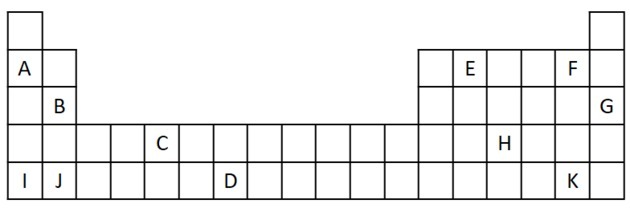
α) Ονομάστε δύο στοιχεία που έχουν δύο ηλεκτρόνια σθένους.
β) Υποδείξτε ένα στοιχείο που αντιδρά βίαια με νερό, παράγοντας ένα μεταλλικό υδροξείδιο.
γ) Υποδείξτε ένα μη αντιδραστικό στοιχείο.
δ) Αναφέρετε δύο στοιχεία που συνδυάζονται με αλκαλικά μέταλλα για να σχηματίσουν άλατα.
Απάντηση:
α) B και J
Δύο ηλεκτρόνια σθένους αντιστοιχούν στην ομάδα 2, η οποία έχει μια διαμόρφωση ηλεκτρονίων ns2 και εκπροσωπούνται στην άσκηση από τους B και J.
β) A, B, I ή J.
A και I αντιπροσωπεύουν στοιχεία της οικογένειας 1. Οι B και J είναι από την οικογένεια 2. Όπως είδαμε στον πίνακα ιδιοτήτων, τα στοιχεία της ομάδας 1 και 2 είναι πολύ αντιδραστικά και μπορούν να σχηματίσουν υδροξείδια, όπως στα παραδείγματα που δίνονται: KOH και Mg (OH)2.
γ) Ζ
Τα ευγενή αέρια είναι πολύ σταθερά και επομένως δεν είναι πολύ αντιδραστικά. Το γράμμα G εισάγεται στον πίνακα ως στοιχείο αυτής της οικογένειας.
δ) F και Κ
Τα αλογόνα αντιδρούν με αλκαλικά μέταλλα για να σχηματίσουν άλατα. Το πιο συνηθισμένο παράδειγμα είναι το επιτραπέζιο αλάτι, το NaCl.
2) Το παρακάτω σχήμα δείχνει τρία χημικά στοιχεία, από αριστερά προς τα δεξιά, λίθιο, νάτριο και κάλιο.

Ορίστε την επιλογή που συμπληρώνει σωστά καθεμία από τις ακόλουθες δηλώσεις.
1.1) "Μπορούμε να πούμε ότι το λίθιο, το νάτριο και το κάλιο ...
(Α)… ανήκουν στην ίδια περίοδο. "
(B)… έχει τον ίδιο ατομικό αριθμό. "
(Γ)... ανήκουν στην ίδια ομάδα. "
(D)... έχει τον ίδιο αριθμό μάζας. "
1.2) "Τα στοιχεία λιθίου, νατρίου και καλίου ...
(Α)... έχει πολύ παρόμοιες χημικές ιδιότητες. "
(B)… έχει πολύ διαφορετικές χημικές ιδιότητες. "
(C)... είναι μη μέταλλα. "
(Δ)… αντιδρά με νερό για να σχηματίσουν όξινα διαλύματα.
Απαντήσεις:
1.1) (C) ανήκουν στην ίδια ομάδα.
1.2) (Α) έχει πολύ παρόμοιες χημικές ιδιότητες.
Μπορούμε να λάβουμε αυτές τις πληροφορίες συμβουλευόμενοι τον περιοδικό πίνακα ή κάνοντας την ηλεκτρονική διανομή των στοιχείων λιθίου, νατρίου και καλίου. Θα δούμε ότι οι τρεις έχουν ένα ηλεκτρόνιο στο κέλυφος σθένους και επειδή είναι μέρος της ίδιας ομάδας, οι χημικές ιδιότητες είναι πολύ παρόμοιες.
3) Σκεφτείτε τον παρακάτω πίνακα, όπου αναπαριστώνται οι ατομικοί αριθμοί και οι ηλεκτρονικές κατανομές ορισμένων χημικών στοιχείων.
| Στοιχείο | χημικό σύμβολο | ατομικός αριθμός | Ηλεκτρονική διανομή |
|---|---|---|---|
| Λίθιο | ανάγνωση | 3 | 2,1 |
| Βηρύλλιο | είναι | 4 | 2,2 |
| Φθόριο | φά | 9 | 2,7 |
| νέο | Ναι | 10 | 2,8 |
| χλώριο | Κλ | 17 | 2,8,7 |
| αργόν | Αέρας | 18 | 2,8,8 |
| Κάλιο | κ | 19 | 2,8,8,1 |
| Ασβέστιο | Εδώ | 20 | 2,8,8,2 |
Υποδείξτε την ομάδα κάθε στοιχείου.
Απάντηση:
Λιθίου και καλίου: ομάδα 1. (Έχουν ένα ηλεκτρόνιο στο κέλυφος σθένους).
Βηρύλλιο και ασβέστιο: ομάδα 2. (Έχουν δύο ηλεκτρόνια στο κέλυφος σθένους).
Φθόριο και χλώριο: ομάδα 17. (Έχουν επτά ηλεκτρόνια στο κέλυφος σθένους).
Νέον και αργόν: ομάδα 18. (Έχουν οκτώ ηλεκτρόνια στο κέλυφος σθένους).
Ελέγξτε τις ερωτήσεις για τις εισαγωγικές εξετάσεις με ένα σχόλιο στο Ασκήσεις στον περιοδικό πίνακα και αδημοσίευτες ερωτήσεις σχετικά με το θέμα στο Ασκήσεις για την οργάνωση του περιοδικού πίνακα.


