Μπορούμε να το σημειώσουμε Κάθε φορά που αυξάνουμε τη συγκέντρωση ενός ή όλων των αντιδρώντων που συμμετέχουν σε μια χημική αντίδραση, υπάρχει μια αύξηση στον ρυθμό ανάπτυξής της, δηλαδή στην ταχύτητα της αντίδρασης.
Το αντίθετο ισχύει επίσης. Για παράδειγμα, συνιστάται να χρησιμοποιούμε τζελ αλκοόλης αντί για κανονικό αλκοόλ, καθώς υπάρχει λιγότερος κίνδυνος καύσης και αποφεύγοντας έτσι ατυχήματα. Η συνηθισμένη υγρή αλκοόλη είναι στην πραγματικότητα ένα μείγμα αλκοόλης και νερού, με αλκοόλη γέλης που περιέχει μικρότερη ποσότητα αλκοόλ. Επομένως, όταν η συγκέντρωση ενός από τα αντιδραστήρια καύσης μειώνεται, στην περίπτωση αλκοόλης, η αντίδραση προχωρά πιο αργά. Από την άλλη πλευρά, όσο πιο καθαρό είναι το αλκοόλ, τόσο πιο γρήγορη είναι η αντίδραση καύσης.

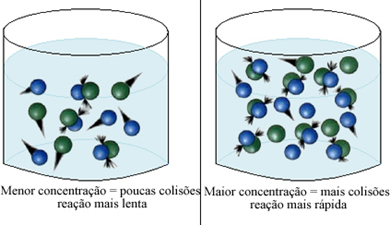
Όπως αναφέρεται στο κείμενο Όροι για την εμφάνιση χημικών αντιδράσεων, μία από τις προϋποθέσεις για να λάβει χώρα μια αντίδραση είναι η αποτελεσματική σύγκρουση μεταξύ των σωματιδίων. Ετσι, Η αύξηση της συγκέντρωσης των αντιδραστηρίων καθιστά δυνατή την περιορισμένη μεγαλύτερη ποσότητα σωματιδίων ή μορίων στον ίδιο χώρο. Αυτό αυξάνει την ποσότητα των συγκρούσεων μεταξύ τους και επίσης αυξάνει την πιθανότητα να συμβούν αποτελεσματικές συγκρούσεις που θα έχουν ως αποτέλεσμα την αντίδραση. Το αποτέλεσμα είναι ότι η αντίδραση λαμβάνει χώρα πιο γρήγορα.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση;)
Για να το δείτε αυτό, σκεφτείτε το ακόλουθο παράδειγμα: όταν έχουμε καύση χορταριού και θέλουμε αυτή η καύση να επεξεργαστεί γρηγορότερα, ρίχνουμε ή ανεβάζουμε τη χήνα; Γιατί λειτουργεί αυτό;
Λοιπόν, ένα από τα αντιδραστήρια σε αυτήν την αντίδραση καύσης είναι το οξυγόνο στον αέρα. Όταν ανακινείται, το ρεύμα αέρα αφαιρεί την τέφρα που σχηματίζεται κατά τη διάρκεια της καύσης και αυτό διευκολύνει την επαφή του οξυγόνου με τη χόβολη. Με αυτόν τον τρόπο, αυξάνουμε την επαφή μεταξύ των αντιδρώντων και επιταχύνουμε την αντίδραση καύσης.
Εν συντομία, έχουμε:

Όταν εργάζεστε με αέρια, ένας τρόπος για να αυξήσετε τη συγκέντρωση των αντιδραστηρίων είναι χαμηλώστε την πίεση. Όταν το κάνουμε αυτό, μειώνουμε τον όγκο και, κατά συνέπεια, υπάρχει αύξηση στις συγκεντρώσεις αντιδραστηρίων.

Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Συγκέντρωση αντιδραστηρίων και ταχύτητα αντιδράσεων" · Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm. Πρόσβαση στις 27 Ιουνίου 2021.
