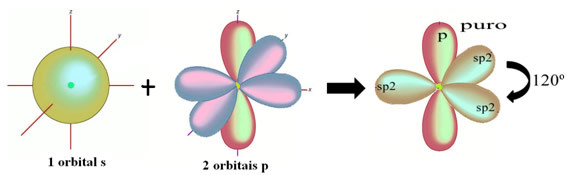
Στο μόρια Είναι δομές που έχουν καθορισμένη γραμμομοριακή μάζα και σχετικά μικρό και ακριβή αριθμό ατόμων που συνδέονται μεταξύ τους ομοιοπολικά, δηλαδή μέσω της κατανομής ηλεκτρονίων.
Δείτε τρία παραδείγματα:
- Αέριο οξυγόνου: Τα μόρια του σχηματίζονται το καθένα από έναν διπλό δεσμό, δηλαδή με την κατανομή δύο ζευγών ηλεκτρονίων μεταξύ δύο ατόμων οξυγόνου (O2);
- Νερό: σχηματίζεται από μόρια Η2Ο. Αυτό σημαίνει ότι κάθε μόριο έχει δύο άτομα υδρογόνου που μοιράζονται ένα ζευγάρι ηλεκτρονίων το καθένα με ένα άτομο οξυγόνου.
- Μεθάνιο: αυτή η ένωση σχηματίζεται από μόρια CH4, στο οποίο τέσσερα άτομα υδρογόνου συνδέονται ομοιοπολικά με ένα άτομο άνθρακα.
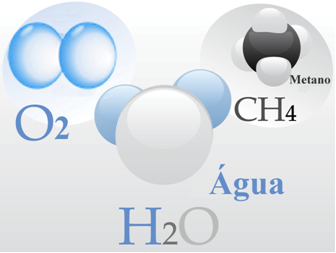
Οι μοριακές ουσίες έχουν ορισμένες χαρακτηριστικές ιδιότητες, όπως:
- Ποικίλη διαλυτότητα στο νερό και άλλους διαλύτες.
- Μπορούν να παρουσιαστούν στις τρεις φυσικές καταστάσεις.
- Σε γενικές γραμμές, είναι ηλεκτρικοί μονωτές, τόσο στερεοί όσο και υγροί.
Όλα τα μόρια σχηματίζονται από μη μεταλλικά στοιχεία, δηλαδή περιλαμβάνουν μόνο υδρογόνο, μη μέταλλα και ημι μέταλλα. Αλλά αυτά τα στοιχεία μπορούν επίσης να σχηματίσουν ουσίες που υπάρχουν μόνο σε στερεά κατάσταση και που έχουν ιδιότητες πολύ διαφορετικές από αυτές των μορίων. αυτά είναι τα
μακρομόρια.Μακρομόρια, επίσης γνωστά ως ομοιοπολικά στερεά ή ομοιοπολικά στερεά δικτύου,Είναι δομές με πολύ υψηλή και ανακριβή μοριακή μάζα, εκτός από το ότι σχηματίζονται από μια μεγάλη και απροσδιόριστη ποσότητα ατόμων που συνδέονται ομοιοπολικά με σχηματισμό τρισδιάστατων πλεγμάτων. Τα μακρομόρια σχηματίζουν το ομοιοπολικοί κρύσταλλοι ή ατομικοί κρύσταλλοι.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
Για παράδειγμα, τα άτομα άνθρακα μπορούν να μοιράζονται ηλεκτρόνια με πολλούς τρόπους και να σχηματίζουν πολλές διαφορετικές απλές ουσίες. Σε αυτήν την ιδιότητα που έχει το ίδιο χημικό στοιχείο για να σχηματίσει δύο ή περισσότερες διαφορετικές απλές ουσίες έχει το όνομα αλλοτροπία.
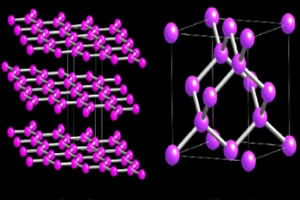
Δύο αλλοτροπικές ποικιλίες άνθρακα που σχηματίζουν μακρομόρια είναι οι Διαμάντι και το γραφίτης. Στις παρακάτω εικόνες μπορείτε να δείτε ότι, στην περίπτωση του διαμαντιού, κάθε άτομο άνθρακα συνδέεται με τέσσερα άλλα άτομα άνθρακα και δημιουργεί ένα μακρομόριο με τετραεδρική δομή.

Εν τω μεταξύ, η δομή του γραφίτη σχηματίζεται από εξαγωνικούς δακτυλίους που περιέχονται στο ίδιο επίπεδο. Τα άτομα άνθρακα δημιουργούν έναν διπλό και δύο μονό δεσμούς.

Αλλά τα μακρομόρια δεν αποτελούνται απλώς από έναν μόνο τύπο στοιχείου. Μπορούν επίσης να σχηματιστούν από άτομα διαφορετικών χημικών στοιχείων.
Ένα παράδειγμα είναι το διοξείδιο του πυριτίου (χαλαζία), του οποίου τα μακρομόρια έχουν κάθε άτομο πυριτίου που περιβάλλεται από τέσσερα άτομα άνθρακα και κάθε άτομο οξυγόνου συνδέεται με δύο άτομα πυριτίου.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Μόρια και μακρομόρια" · Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/moleculas-macromoleculas.htm. Πρόσβαση στις 28 Ιουνίου 2021.
Χημεία
Τι είναι αλλοτροπία, απλές ουσίες, αέριο οξυγόνο, όζον, αλλοτροπικές μορφές, χημικό στοιχείο οξυγόνο, υπεριώδεις ακτίνες από τον ήλιο, διαμάντι, γραφίτης, ατομικότητα, λευκός φωσφόρος.
Χωρικός τύπος Carbon, ηλεκτρονικός τύπος Lewis, δομή επιπέδου, ηλεκτρονικά ζεύγη, δεσμός ομοιοπολικό, στρώμα σθένους, εξέλιξη του ατομικού μοντέλου, μοριακός τύπος, δομικός τύπος, τύποι τρισδιάστατο.
Χημικοί τύποι, επίπεδος δομικός τύπος, συντακτικός τύπος Couper, τριπλός δεσμός, αέριο άζωτο, ηλεκτρονικός τύπος, τύπος Lewis, μοριακός τύπος, μονός δεσμός, διπλός δεσμός, αέριο ανθρακικός.