Υβριδισμός άνθρακα τύπου sp2 Εμφανίζεται όταν έχει έναν διπλό δεσμό και δύο απλούς δεσμούς ή έναν δεσμό pi (π) και τρεις δεσμούς σίγμα (σ). Στην πραγματικότητα, η υβριδοποίηση sp2 προκαλείται μεταξύ των ατόμων που δημιουργούν τον διπλό δεσμό.
Ένα παράδειγμα ενός τέτοιου μορίου είναι η φορμαλδεΰδη (CH2Ο). Σημειώστε τη δομή του παρακάτω:
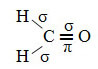
Όπως φαίνεται στο κείμενο "υβριδοποίηση τύπου sp3", Ο υβριδισμός του άνθρακα συμβαίνει όταν ένα ηλεκτρόνιο από το δευτερεύον επίπεδο 2s λαμβάνει ενέργεια και" μεταφέρεται "στο 2p sublevel και, ως εκ τούτου, προέρχονται 4 υβριδισμένα τροχιακά από το "μείγμα" ατομικών τροχιακών ΚΑΘΑΡΟΣ.
Στην περίπτωση της φορμαλδεΰδης, γνωρίζουμε ότι θα υπάρχει ένας δεσμός pi, οπότε ένα από αυτά τα υβριδοποιημένα τροχιακά προορίζεται για αυτόν τον δεσμό, ενώ τα άλλα τρία φέρουν τους δεσμούς σίγμα:
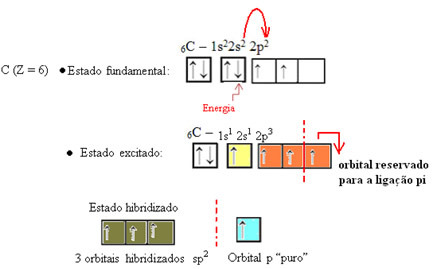
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
Τα άτομα υδρογόνου που κάνουν τον μοναδικό δεσμό με άνθρακα, το κάνουν με την τροχιά τους:
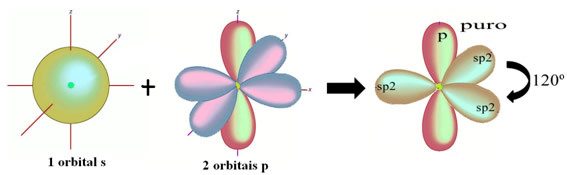
Το υπόλοιπο "καθαρό" τροχιακό p διπλώνει το άτομο οξυγόνου και το μόριο φορμαλδεΰδης έχει την ακόλουθη δομή:
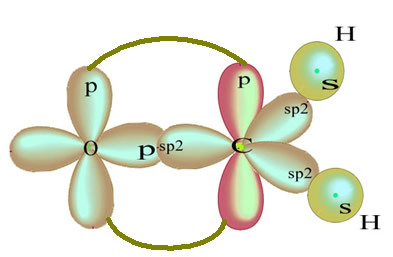
Όσον αφορά τον τύπο ομολόγων που υπάρχουν σε αυτήν τη δομή φορμαλδεΰδης, έχουμε:

Συνδέσεις: 1 = 2 = σs-sp2
3 = σp-sp2
4 =ππ-π
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Υβριδοποίηση τύπου Sp2"; Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm. Πρόσβαση στις 28 Ιουνίου 2021.
