Μερικές φορές μπορεί να συμβεί ελάχιστος τύπος να είναι το ίδιο με τον μοριακό τύπο της ένωσης · Ωστόσο, αυτό δεν ισχύει πάντα.
Για παράδειγμα, η εμπειρική ή ελάχιστη φόρμουλα για το νερό είναι H2Ο, υποδεικνύοντας ότι υπάρχει αναλογία 2: 1 μεταξύ των στοιχείων που απαρτίζουν τα μόρια του νερού. Και, συμπτωματικά, αυτός είναι και ο μοριακός τύπος για το νερό. Ωστόσο, για να δείτε ότι αυτό δεν συμβαίνει πάντα, δείτε τα δύο παρακάτω παραδείγματα:
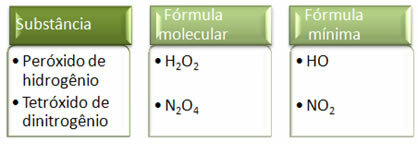
Δεδομένου ότι ο ελάχιστος τύπος είναι μόνο ο λόγος των ατόμων κάθε στοιχείου και όχι η πραγματική ποσότητα αυτών στον μοριακό τύπο, μπορεί να συμβεί διαφορετικών ενώσεων που έχουν τον ίδιο εμπειρικό τύπο και ακόμη και τον ελάχιστο τύπο μιας ένωσης μπορεί να είναι ο ίδιος με τον μοριακό τύπο του άλλα. Σημειώστε, στο παρακάτω παράδειγμα, πώς μπορεί να συμβεί αυτό:
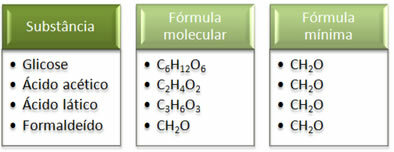
Δείτε ότι ο ελάχιστος τύπος CH2Το ίδιο ισχύει για όλες τις ουσίες, δηλαδή, αυτός ο ελάχιστος τύπος εκφράζει ότι, σε όλες τις περιπτώσεις, το άτομα άνθρακα, υδρογόνου και οξυγόνου υπάρχουν σε μοριακούς τύπους σε αναλογία 1:2:1. Επιπλέον, το μόνο που έχει τον ίδιο μοριακό τύπο με τον εμπειρικό τύπο είναι η φορμαλδεΰδη.
- Υπολογισμός του ελάχιστου ή εμπειρικού τύπου:
Για να προσδιοριστεί ο εμπειρικός τύπος μιας ένωσης, είναι πρώτα απαραίτητο να γνωρίζουμε ποιο είναι το ποσοστό ή το εγγύς τύπο του. Αυτό μπορεί να γίνει μετρώντας τη μάζα κάθε στοιχείου σε 100 g δείγματος. Το κείμενο "Ποσοστό ή εκατοστιαίο τύπο"Διευκρινίζει αυτό το θέμα καλύτερα.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
Για παράδειγμα, ας υποθέσουμε ότι η εγγύς σύνθεση μιας δεδομένης ένωσης δίνεται από: 40,00% C, 6,67% H και 53,33% O. Μεταβιβάζουμε αυτές τις τιμές σε γραμμάρια, λαμβάνοντας υπόψη μια μάζα 100 g σύνθετου δείγματος. Έτσι, έχουμε: 40 g C, 6,67 g H και 53,33 g O.
Τώρα είναι απαραίτητο να περάσετε αυτές τις τιμές στην ποσότητα της ύλης (mol). Αυτό το κάνουμε διαιρώντας κάθε μία από τις τιμές που βρέθηκαν από τις αντίστοιχες μοριακές μάζες τους:
C: 40/12 = 3,33
Η: 6,67 / 1 = 6,67
Ο: 53,33 / 16 = 3,33
Δεδομένου ότι οι τιμές δεν είναι ακέραιοι, χρησιμοποιούμε την ακόλουθη συσκευή: διαιρούμε όλες τις τιμές με τις μικρότερες από αυτές, έτσι ώστε η αναλογία μεταξύ τους να μην αλλάζει.
Σε αυτήν την περίπτωση, η μικρότερη τιμή είναι 3,33, οπότε το αποτέλεσμα θα είναι:
C: 3,33 / 3,33 = 1
Η: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Έτσι, ο ελάχιστος τύπος αυτής της άγνωστης ουσίας ισούται με: ΝΤΟ1Η2Ο1 ή Χ.Χ.2Ο.
Εν συντομία, τα βήματα που απαιτούνται για την εύρεση του εμπειρικού ή ελάχιστου τύπου μιας ουσίας είναι:

Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Ελάχιστος ή εμπειρικός τύπος". Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Πρόσβαση στις 28 Ιουνίου 2021.