Ο αρχή του Le Chatelier μας λέει ότι όταν μια διαταραχή προκαλείται σε ένα σύστημα ισορροπίας, θα μετατοπιστεί προς την κατεύθυνση που ελαχιστοποιεί τις δυνάμεις που δημιουργούνται από αυτή τη διαταραχή και αποκαθιστά μια νέα χημική ισορροπία.
Μία από αυτές τις διαταραχές είναι η διακύμανση θερμοκρασίας. Αυτή η διακύμανση είναι σημαντική επειδή, εκτός από την πρόκληση μετατόπισης ισορροπίας, θα αλλάξει επίσης την τιμή της σταθεράς ισορροπίας, Kντο.
Για να καταλάβετε καλύτερα πώς συμβαίνει αυτό, ας δούμε ένα παράδειγμα:
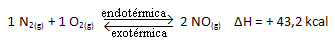
κντο = _[ ΣΤΟ]2___
[Ν2]. [Ο2]
Η παραπάνω αντίδραση εμφανίζεται στην άμεση κατεύθυνση με απορρόφηση ενέργειας, είναι ενδοθερμική. Η αντίστροφη διαδικασία, από την άλλη πλευρά, συμβαίνει με την απελευθέρωση ενέργειας, ως εξώθερμη αντίδραση.
Έτσι, εάν αυξήσουμε τη θερμοκρασία του συστήματος, η χημική ισορροπία θα μετατοπιστεί προς την ενδοθερμική αντίδραση, η οποία σε αυτήν την αντίδραση είναι προς τα δεξιά. Αυτό γίνεται έτσι ώστε η θερμότητα να απορροφάται και να ανακτάται η ισορροπία.
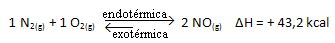
Το αντίθετο ισχύει επίσης. Αν μειώσουμε τη θερμοκρασία αυτού του συστήματος, η αντίδραση θα μετατοπιστεί προς την κατεύθυνση που θα απελευθερώσει θερμότητα, επειδή η συνολική ενέργεια της αντίδρασης θα μειωθεί. Αυτό σημαίνει ότι η ισορροπία θα μετακινηθεί προς την εξώθερμη αντίδραση, η οποία στην περίπτωση αυτή είναι προς τα αριστερά:
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
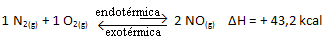
Εν συντομία:

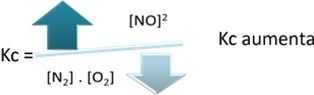
Σε σχέση με τη σταθερά ισορροπίας (Κντο), όταν η θερμοκρασία αυξάνεται, ευνοεί την ενδοθερμική αντίδραση και περισσότερο ΟΧΙ(σολ) σχηματίζεται, αυξάνοντας τη συγκέντρωσή του και μειώνοντας τη συγκέντρωση των αντιδρώντων. Σημειώστε στον παρακάτω τύπο ότι η συγκέντρωση ΝΟ(σολ) είναι άμεσα ανάλογη με τη σταθερά Κντο, συνεπώς, αυξάνει επίσης:
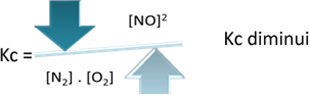
Αλλά αν μειώσουμε τη θερμοκρασία, μετατοπίζοντας την αντίδραση προς την εξώθερμη αντίδραση, η συγκέντρωση του προϊόντος ΝΟ θα μειωθεί και οι συγκεντρώσεις των αντιδρώντων θα αυξηθούν. Δεδομένου ότι οι συγκεντρώσεις των αντιδρώντων είναι αντιστρόφως ανάλογες με το σταθερό Kc, τότε θα μειωθεί:
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Μεταβολή θερμοκρασίας και μετατόπιση χημικής ισορροπίας". Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/variacao-temperatura-deslocamento-equilibrio-quimico.htm. Πρόσβαση στις 28 Ιουνίου 2021.
Χημεία

Δοκιμάστε τις γνώσεις σας και μάθετε περισσότερα με αυτόν τον κατάλογο λύσεων για χημικές ισορροπίες. Μέσω αυτού του υλικού, θα είστε σε θέση να κατανοήσετε καλύτερα πώς να εργάζεστε σταθερές ισορροπίας (Kp, Kc και Ki), μετατόπιση ισορροπίας, pH και pOH, καθώς και ισορροπία σε λεγόμενες ρυθμιστικές λύσεις.