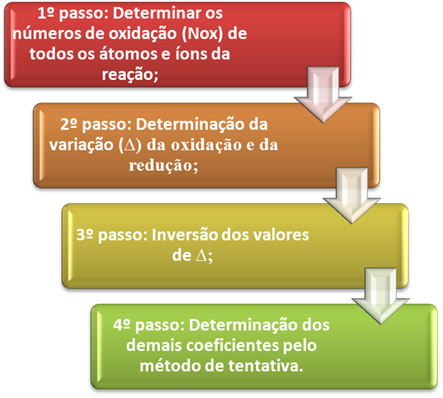
Το ρΗ αντιστοιχεί στο υδρογονικό δυναμικό ενός διαλύματος. Προσδιορίζεται από τη συγκέντρωση ιόντων υδρογόνου (Η+) και χρησιμεύει για τη μέτρηση του βαθμού οξύτητας, ουδετερότητας ή αλκαλικότητας ενός δεδομένου διαλύματος.
Εκτός από το pH, υπάρχει επίσης μια άλλη ποσότητα που καθορίζει την οξύτητα και τη βασικότητα ενός υδατικού συστήματος: το pOH (υδροξυλονικό δυναμικό). Αυτή η κλίμακα έχει την ίδια λειτουργία με το pH, αν και χρησιμοποιείται λιγότερο.
κλίμακα pH
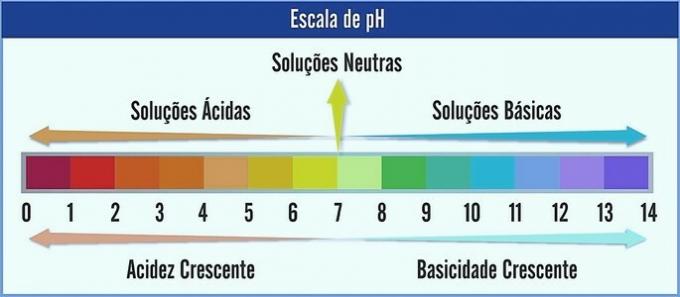
Το pH αντιπροσωπεύεται σε κλίμακα που κυμαίνεται από 0 έως 14. Μετρά την οξύτητα και τη βασικότητα μιας λύσης.
Επομένως, το ρΗ 7 αντιπροσωπεύει ένα ουδέτερο διάλυμα (π.χ. καθαρό νερό). Αυτά πριν από αυτό θεωρούνται όξινα διαλύματα (όξινο pH), και αυτά μετά το 7 είναι τα βασικά διαλύματα (αλκαλικό pH).
Με αυτήν την παρατήρηση, ο όξινος χαρακτήρας αυξάνεται από δεξιά προς αριστερά. Ο βασικός χαρακτήρας, από αριστερά προς τα δεξιά. Σημειώστε ότι όσο χαμηλότερη είναι η τιμή του pH, τόσο πιο όξινο θα είναι το διάλυμα.
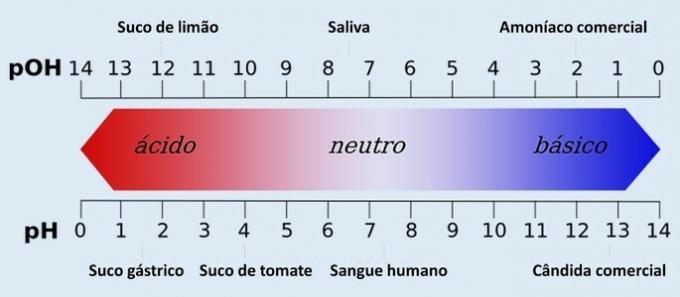
Μάθετε περισσότερα στο:
- Ρυθμιστικό διάλυμα
- Ογκομετρική ανάλυση
- Αντίδραση εξουδετέρωσης
Παραδείγματα
Διαλύματα οξέος
| Λύση | pH |
|---|---|
| Γαστρικό υγρό | 2,0 |
| Χυμός λεμονιού | 2,2 |
| Ξύδι | 3,0 |
| Καφές | 5,0 |
| Αγελαδινό γάλα | 6,4 |
Βασικές Λύσεις
| Λύση | pH |
|---|---|
| ανθρώπινο αίμα | 7,35 |
| Θαλασσινο νερο | 7,4 |
| Διττανθρακικό νάτριο | 8,4 |
| Γάλα μαγνησίου | 10,5 |
| Λευκαντικό | 12,5 |
Πώς να υπολογίσετε το pH;
Το 1909, ο Δανός χημικός Soren Sörensen (1868-1939) πρότεινε ότι η οξύτητα των διαλυμάτων, μετρούμενη με βάση τις συγκεντρώσεις των ιόντων Η+, οι τιμές του μεταμορφώθηκαν χρησιμοποιώντας λογάριθμους για να διευκολύνουν την κατανόηση.
Σε θερμοκρασία 25 ° C το ιοντικό προϊόν του νερού είναι ίσο με 10–14 mol2/ΜΕΓΑΛΟ2.
Εφαρμόζοντας τον κολογράριθμο στην έκφραση, πρέπει:
Μέσω αυτής της έκφρασης, μπορούμε να αποκτήσουμε την αντίστοιχη τιμή από τη μία κλίμακα στην άλλη μέσω της αφαίρεσης.
Πώς να μετρήσετε το pH;
Ο έλεγχος του pH είναι σημαντικός όχι μόνο για επιστημονικούς σκοπούς, αλλά και για την καθημερινή ζωή.
Το pH της πισίνας πρέπει να ελεγχθεί, καθώς και το pH του ενυδρείου, ακόμη και το pH του εδάφους, ώστε να επιτρέπονται ορισμένοι τύποι καλλιεργειών.
Ακολουθούν οι κύριοι τρόποι μέτρησης του pH.
δείκτης οξέος-βάσης
Οι λεγόμενοι δείκτες οξέος-βάσης χρησιμοποιούνται για τη μέτρηση του pH ενός διαλύματος. Είναι ουσίες που αλλάζουν χρώμα που υποδηλώνουν το χαρακτήρα του διαλύματος. Οι πιο χρησιμοποιούμενοι δείκτες είναι: litmus και phenolphthalein.

Βηματόμετρο
Εκτός από τους δείκτες, το pH ενός διαλύματος μπορεί να μετρηθεί χρησιμοποιώντας ένα όργανο που ονομάζεται peagometer. Αυτή η ηλεκτρονική συσκευή μετρά την ηλεκτρική αγωγιμότητα του διαλύματος και το μετατρέπει στην κλίμακα των τιμών του pH.

Εξετάσεις Ασκήσεις με Ανατροφοδότηση
1. (Enem / 2014) Ένας ερευνητής συνειδητοποιεί ότι η ετικέτα ενός από τα γυαλιά στα οποία διατηρεί συμπύκνωμα πεπτικών ενζύμων είναι δυσανάγνωστη. Δεν ξέρει ποιο ένζυμο περιέχει το γυαλί, αλλά υποψιάζεται ότι είναι μια γαστρική πρωτεάση, η οποία λειτουργεί στο στομάχι χωνεύοντας πρωτεΐνες.
Γνωρίζοντας ότι η πέψη στο στομάχι είναι όξινο και το έντερο είναι βασικό, συγκεντρώνει πέντε δοκιμαστικούς σωλήνες με τροφή διαφορετικά, προσθέστε το συμπύκνωμα ενζύμου σε διαλύματα με καθορισμένο pH και περιμένετε να δείτε εάν το ένζυμο δρα σε κάποιο δικα τους.
Ο δοκιμαστικός σωλήνας στον οποίο το ένζυμο πρέπει να δράσει για να δείξει ότι η υπόθεση του ερευνητή είναι σωστή είναι αυτή που περιέχει:
α) κύβος πατάτας σε διάλυμα με pH = 9
β) κομμάτι κρέατος σε διάλυμα με pH = 5
γ) βρασμένο ασπράδι αυγού σε διάλυμα με pH = 9
δ) μερίδα χυλοπίτες σε διάλυμα με pH = 5
ε) σφαίρα βουτύρου σε διάλυμα με pH = 9
Σωστή εναλλακτική λύση: β) κομμάτι κρέατος σε διάλυμα με pH = 5.
Η πρωτεάση είναι ένα ένζυμο που αφομοιώνει τις πρωτεΐνες και επειδή είναι γαστρικό, δρα στο στομάχι, του οποίου το pH είναι όξινο.
Αναλύοντας τις εναλλακτικές λύσεις, πρέπει:
Α) ΛΑΘΟΣ. Οι πατάτες έχουν υψηλή περιεκτικότητα σε υδατάνθρακες και το pH του συμπυκνώματος είναι βασικό.
β) ΣΩΣΤΗ. Το κρέας περιέχει πρωτεΐνες και τα ένζυμα μπορούν να δράσουν σε αυτό, και το pH του συμπυκνώματος είναι όξινο, όπως το στομάχι.
γ) ΛΑΘΟΣ. Το pH του συμπυκνώματος είναι βασικό.
δ) ΛΑΘΟΣ. Τα ζυμαρικά είναι πλούσια σε υδατάνθρακες.
ε) ΛΑΘΟΣ. Το pH του συμπυκνώματος είναι βασικό.
2. (Udesc / 2009) "Όξινη βροχή" είναι ένας όρος που αναφέρεται σε βροχόπτωση από την ατμόσφαιρα της βροχής με μεγαλύτερες από τις κανονικές ποσότητες νιτρικών και θειικών οξέων.
Οι πρόδρομοι της όξινης βροχής προέρχονται τόσο από φυσικές πηγές, όπως ηφαίστεια όσο και από φθίνουσα βλάστηση, και από διεργασίες βιομηχανικές εκπομπές, κυρίως διοξείδιο του θείου και οξείδια του αζώτου από καύσιμα απολιθώματα
Το pH του βρόχινου νερού που θεωρείται φυσιολογικό είναι 5,5 (λόγω της παρουσίας ανθρακικού οξέος από τη διαλυτοποίηση του διοξειδίου του άνθρακα). Ένας φαρμακοποιός που παρακολουθούσε μια ιδιαίτερα βιομηχανική περιοχή σημείωσε ότι το pH του βρόχινου νερού ήταν 4,5.
Λαμβάνοντας υπόψη ότι η οξύτητα σχετίζεται με τη συγκέντρωση του Η3Ο+, είναι σωστό να πούμε ότι το νερό με pH 4,5 ήταν:
α) δύο φορές πιο απλό από το κανονικό.
β) δύο φορές όξινο από το κανονικό.
γ) δέκα φορές πιο βασικό από το κανονικό.
δ) δέκα φορές πιο όξινο από το κανονικό.
ε) εκατό φορές πιο όξινο από το κανονικό.
Σωστή εναλλακτική λύση: δ) δέκα φορές πιο όξινο από το κανονικό.
Σύμφωνα με τις εκφράσεις pH = - log [H+] και [Η+] = 10-ΡΗ, Πρεπει να:
pH = 5.5
[Χ+] = 10-5,5
pH = 4,5
[Χ+] = 10-4,5
Η διαφορά μεταξύ των τιμών είναι: 10- 5,5 - ( - 4,5) = 10 -1
Καθώς η κλίμακα pH είναι λογαριθμική κλίμακα, η αλλαγή μιας μονάδας ισοδυναμεί με 10 φορές περισσότερο όξινο διάλυμα.
3. (UFMG / 2009) Εξετάστε μια ορισμένη ποσότητα νερού και χυμού λεμονιού, αναμεμιγμένα, που περιέχονται σε ένα ποτήρι. Ελέγξτε αυτές τις τρεις δηλώσεις σχετικά με αυτό το σύστημα:
ΕΓΩ. Το σύστημα είναι όξινο.
ΙΙ. Το pH του συστήματος είναι μεγαλύτερο από 7.
III. Στο σύστημα, η συγκέντρωση των ιόντων Η+ είναι μεγαλύτερο από το OH–.
Με βάση αυτήν την ανάλυση, είναι σωστό να δηλώνεται ότι:
α) μόνο οι δηλώσεις I και II είναι σωστές.
β) μόνο οι δηλώσεις I και III είναι σωστές.
γ) μόνο οι δηλώσεις II και III είναι σωστές.
δ) Και οι τρεις δηλώσεις είναι σωστές.
Σωστή εναλλακτική λύση: β) μόνο οι δηλώσεις I και III είναι σωστές.
ΕΓΩ. ΣΩΣΤΟΣ Το λεμόνι περιέχει κιτρικό οξύ, το οποίο σε διάλυμα απελευθερώνει ιόντα Η+ και έτσι το σύστημα είναι όξινο.
ΙΙ. ΛΑΝΘΑΣΜΕΝΟΣ. Το pH είναι μικρότερο από 7, χαρακτηρίζοντας ένα όξινο σύστημα: όσο πιο κοντά στο 0 το διάλυμα διαλύματος, τόσο πιο όξινο είναι.
III. ΣΩΣΤΟΣ Το όξινο ρΗ είναι αποτέλεσμα της υψηλής συγκέντρωσης ιόντων Η+ σε διάλυμα, αφού το pH = - log [H+].
Για περισσότερες ερωτήσεις, με ανάλυση σχολίων, φροντίστε να ελέγξετε:Ασκήσεις σε pH και pOH.