Ο επίπεδος ή συνταγματικός ισομερισμός είναι μία στην οποία δύο ή περισσότερες ενώσεις έχουν τον ίδιο μοριακό τύπο, αλλά διαφέρουν από κάποια άποψη στη δομή τους. Μία από αυτές τις πτυχές είναι το θέση ακορεσμού, λειτουργίας και διακλάδωσης.
Έτσι, μπορούμε να πούμε ότι α ισομερισμός θέσης ή θέσης συμβαίνει όταν τα ισομερή έχουν την ίδια αλυσίδα άνθρακα, αλλά διαφέρουν από τη θέση ενός από τους προαναφερθέντες παράγοντες.
1ο Παράδειγμα:θέση κορεσμού
Σημειώστε ότι οι δύο παρακάτω ενώσεις έχουν τον ίδιο μοριακό τύπο, C5Η10, αλλά ο κορεσμός του (διπλός δεσμός) βρίσκεται ανάμεσα σε διαφορετικούς άνθρακες σε κάθε περίπτωση. Στο πρώτο μόριο, ο διπλός δεσμός βρίσκεται μεταξύ του άνθρακα 1 και 2, στο δεύτερο, είναι μεταξύ του άνθρακα 2 και 3.
Η2ΝΤΟ ═Χ.Χ. ─CH2Χ.Χ.2Χ.Χ.3 Η3ΝΤΟ ─CH2Χ.Χ. ═Χ.Χ. Χ.Χ.3
έγκλειστος-1-όχι pent-2-όχι
2ο Παράδειγμα:θέση λειτουργίας
Στη συνέχεια έχουμε δύο ισομερή που έχουν την ίδια λειτουργία (κετόνη), με τον ίδιο μοριακό τύπο, C6Η12Η θέση αλλά η λειτουργική ομάδα (καρβονύλιο) είναι διαφορετική. Στην πρώτη, το καρβονύλιο αφήνει άνθρακα 2. Στην άλλη ένωση, αφήνει άνθρακα 3.
ΟΟ
║║
Η3ΝΤΟ ─ ΝΤΟΧ.Χ.2Χ.Χ.2Χ.Χ.2─CH3 Η3ΝΤΟ Χ.Χ.2─ ΝΤΟΧ.Χ.2Χ.Χ.2Χ.Χ.3
εξαν-2-ένα εξάνιο-3-ένας
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση;)
Είναι σημαντικό να θυμόμαστε ότι στη θέση ισομερισμού όλα τα ισομερή ανήκουν στην ίδια χημική λειτουργία.
3ο Παράδειγμα:θέση κλάδου
Και οι δύο ενώσεις παρακάτω έχουν τον μοριακό τύπο C7Η16, αλλά ο κλάδος (μεθυλ) της πρώτης ένωσης βγαίνει από τον άνθρακα 2. Στη δεύτερη ένωση, βρίσκεται στον άνθρακα 3.
Η3Γ ─ Χ.Χ. Χ.Χ.2 Χ.Χ.2 Χ.Χ.2 ─CH3 Η3Γ CH2 ─ Χ.Χ. Χ.Χ.2 Χ.Χ.2 ─CH3
||
Χ.Χ.3Χ.Χ.3
2-μεθυλ-εξάνιο 3-μεθυλ-εξάνιο
Σημείωση: Υπάρχει επίσης ένας ειδικός τύπος ισομερισμού θέσης, αλλά αυτό εξετάζεται ξεχωριστά. ονομάζεται Εγώποσό αποζημίωσης ή μεταμέρεια, επειδή η διαφορά είναι στη θέση του ετεροάτομου (άτομο που εμφανίζεται σε μια αλυσίδα άνθρακα μεταξύ των ανθράκων).
Παράδειγμα: Η3Γ ─ Ο Χ.Χ.2 Χ.Χ.2 Χ.Χ.2 ─CH3 Η3Γ CH2 ─ Ο Χ.Χ.2 Χ.Χ.2 ─CH3
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Θα θέλατε να αναφέρετε αυτό το κείμενο σε σχολείο ή ακαδημαϊκό έργο; Κοίτα:
FOGAÇA, Jennifer Rocha Vargas. "Ισομερισμός θέσης". Σχολείο της Βραζιλίας. Διαθέσιμο σε: https://brasilescola.uol.com.br/quimica/isomeria-posicao.htm. Πρόσβαση στις 27 Ιουνίου 2021.
Χημεία
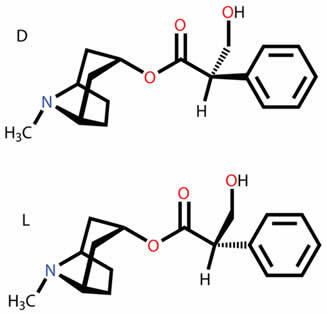
Μάθετε ποιοι είναι οι διάφοροι τύποι επίπεδων και χωρικών ισομερών, όπως λειτουργία, θέση, αλυσίδα, ταυτομερισμός, μεταμερισμός, γεωμετρικός και οπτικός ισομερισμός cis-trans.