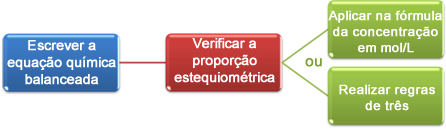
Ο υπολογισμός του ατομική μάζα ενός στοιχείου είναι ο μαθηματικός πόρος που χρησιμοποιείται για τον προσδιορισμό της τιμής μάζας που υπάρχει στον Περιοδικό Πίνακα καθενός από τα υπάρχοντα χημικά στοιχεία. Σε γενικές γραμμές, για την εκτέλεση του υπολογισμός ατομικής μάζας, πρέπει να γνωρίζουμε τις ακόλουθες μεταβλητές του χημικό στοιχείο:
Ισότοπα στοιχείου;
Αριθμός μάζας κάθε ισότοπου του στοιχείου.
Ποσοστό κάθε ισότοπου του στοιχείου στη φύση.
Ο υπολογισμός της ατομικής μάζας του υδρογόνου, για παράδειγμα, πραγματοποιήθηκε με βάση τα ακόλουθα δεδομένα:
Παρουσιάζει τα ισότοπα πρωτίου (Η1), δευτέριο (Η2) και τρίτιο (Η3);
Οι μάζες αυτών των ισοτόπων είναι 1, 2 και 3 αντίστοιχα.
Το ποσοστό Protium στη φύση είναι 98,9%.
Το ποσοστό του δευτερίου στη φύση είναι 0,09%.
Το ποσοστό του τριτίου στη φύση είναι 0,01%.
Μαθηματικό πρότυπο για τον υπολογισμό της ατομικής μάζας
Για την εκτέλεση του υπολογισμός ατομικής μάζας οποιουδήποτε χημικού στοιχείου, πρέπει να χρησιμοποιήσουμε το ακόλουθο μαθηματικό μοτίβο:
1Ο: πολλαπλασιάστε τον αριθμό μάζας κάθε ισοτόπου με το ποσοστό του.
2Ο: προσθέστε όλα τα αποτελέσματα που βρέθηκαν στους πολλαπλασιασμούς του πρώτου βήματος.
3Ο: διαιρέστε το ποσό που βρέθηκε με 100.
Μ.Α. = αριθμός μάζας. ποσοστό + αριθμός μάζας. ποσοστό
100
Χάρτης μυαλού: Ατομική μάζα
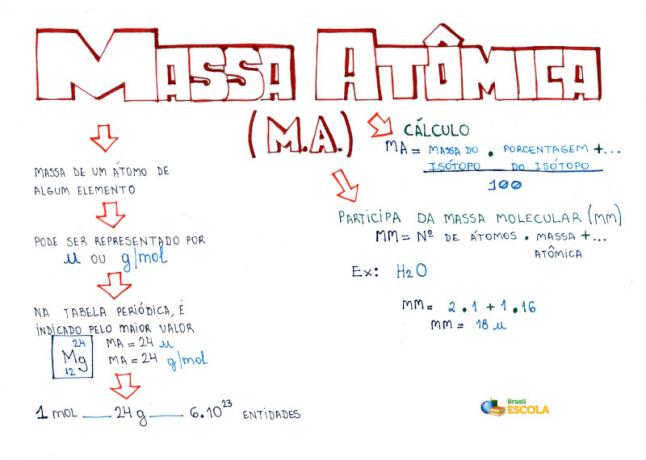
* Για να κατεβάσετε τον χάρτη μυαλού σε PDF, Κάντε κλικ ΕΔΩ!
Παραδείγματα υπολογισμού ατομικής μάζας
⇒ 1ο παράδειγμα: Υπολογισμός της ατομικής μάζας του θείου.
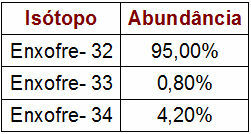
Ποσοστά και δεδομένα μάζας των ισοτόπων θείου
Ο πίνακας που παρέχεται δείχνει τον αριθμό μάζας και το ποσοστό κάθε ισότοπου θείου στη φύση. Για να εκτελέσετε τον υπολογισμό της ατομικής μάζας, απλώς εκτελέστε τα ακόλουθα βήματα:
1Ο Βήμα: πολλαπλασιάστε τον αριθμό μάζας κάθε ισότοπου με την τιμή της αφθονίας του.
Θείο - 32 (Ν32)
μικρό32 = 32.95
μικρό32 = 3040
Θείο - 33 (Ν33)
μικρό33 = 33.0,8
μικρό33 = 26,4
Θείο - 34 (Ν34)
μικρό34 = 34.4,2
μικρό34 = 142,8
2Ο Βήμα: Προσθέστε τις τιμές που βρίσκονται στους πολλαπλασιασμούς του αριθμού μάζας και της αφθονίας του ισοτόπου.
Άθροισμα = S32 + Δ33 + Δ34
Άθροισμα = 3040 + 26,4 + 142,8
Άθροισμα = 3209,2
3Ο Βήμα: υπολογίστε την ατομική μάζα διαιρώντας το άθροισμα των αποτελεσμάτων που βρέθηκαν με 100:
Μ.Α. = Αθροισμα
100
Μ.Α. = 3209,2
100
Μ.Α. = 32.092 u
⇒ 2ο παράδειγμα: Ένα δεδομένο χημικό στοιχείο (D) έχει τρία ισότοπα, των οποίων οι αριθμοί μάζας είναι:
30ρε 32ρε 34ρε
Γνωρίζοντας ότι η ατομική μάζα αυτού του στοιχείου είναι 32,20 u και ότι υπάρχει το 20% του ισοτόπου 32D στη φύση, ποια είναι η αξία των ποσοστών των άλλων ισοτόπων;
Η δήλωση δίνει τους αριθμούς μάζας, την ατομική μάζα και το ποσοστό ενός από τα ισότοπα. Για να προσδιορίσουμε τα ποσοστά άλλων ισοτόπων, πρέπει να ακολουθήσουμε τα ακόλουθα βήματα:
1Ο Βήμα: προσδιορίστε το ποσοστό κάθε ισότοπου.
Ισότοπο - 30 (DS30)
DS30 = 30.χ
DS30 = 30χ
Ισότοπο - 32 (DS32)
DS32 = 32.20
DS32 = 640
Ισότοπο - 34 (Δ34)
DS34 = 34. ε
DS34 = 34ε
2Ο Βήμα: Χρησιμοποιήστε όλα τα δεδομένα που βρέθηκαν στη μαθηματική έκφραση για να υπολογίσετε την ατομική μάζα.
Μ.Α. = αριθμός μάζας. ποσοστό + αριθμός μάζας. ποσοστό
100
32,2 = 30x + 640 + 34ε
100
32,2.100 = 30x + 640 + 34ε
100
3220 - 640 = 30x + 34y
30x + 34y = 2580
x = 2580 - 34ε
30
3Ο Βήμα: χρησιμοποιήστε την έκφραση που βρέθηκε παραπάνω από τον ακόλουθο συλλογισμό:
Ποσοστό ισότοπου 1 + Ποσοστό ισότοπου 2 + Ποσοστό ισότοπου 3 = 100%
x + 20 + y = 100
x + y = 100 - 20
x + y = 80
x = 80 - ε
2580 - 34ε = 80-ε
30
2580 - 34y = 30. (80-ε)
2580-34 y = 2400 - 30y
2580 - 2400 = 34y-30y
4y = 180
y = 80
4
y = 45%
4Ο Βήμα: υπολογίστε την ποσοστιαία τιμή του x στην έκφραση που κατασκευάστηκε στο τρίτο βήμα.
x + y = 80
x + 45 = 80
x = 80 - 45
x = 35%
Από μένα. Diogo Lopes Dias
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm