Verwendung einer Crookes-Ampulle, dh geschlossener Glasröhrchen mit einer positiven und einer negativen Elektrode, die Gase bei extrem niedrigen Drücken enthalten; der englische wissenschaftler Joseph John Thomson (1856-1940) machte eine wesentliche Entdeckung für die Entwicklung des Atommodells.
Er setzte diese Gase extrem hohen Spannungen aus, dadurch konnte das Auftreten von Emissionen beobachtet werden, die sog. Kathodenstrahlen. Dann wurde ein externes elektrisches Feld angelegt und schließlich wurde verifiziert, dass der Kathodenstrahl abgelenkt wurde, wobei er immer in Richtung und Richtung der positiv geladenen Platte ging. Daher wurden diese Emissionen negativ geladen.
Ein weiterer wichtiger Punkt ist, dass, egal welches Gas verwendet wurde, es immer dasselbe war; so kam Thomson zu dem logischen Schluss, dass diese negativen Ladungen in jeder Materie vorhanden waren, ein wesentlicher Bestandteil davon waren. Damit war bewiesen, dass das Atom im Gegensatz zu Daltons Aussage nicht unteilbar war, da es ein negatives subatomares Teilchen hatte, das genannt wurde
Nacheinander, im Jahr 1886, entdeckte ein anderer Wissenschaftler namens Eugen Goldstein die Anodenstrahlen oder Kanäle, die positiv geladene Strahlen waren, die von den Resten der Atome des Gases gebildet wurden, deren Elektronen durch die elektrische Entladung abgerissen wurden. Es war bekannt, dass diese Strahlen besaßen positive Ladung weil sie in die entgegengesetzte Richtung der Kathodenstrahlen abgelenkt wurden, dh sie wurden von der negativen Platte angezogen.
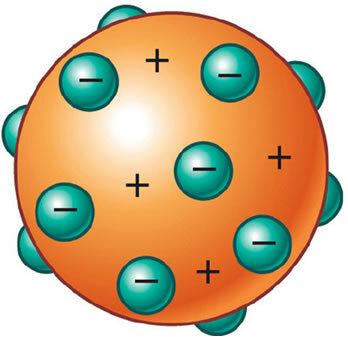
Dann stellte sich heraus, dass das Atom auch einen positiven Anteil hatte, der sogar notwendig war, um seine elektrische Neutralität zu erhalten. So hat J. J. Thomson schlug ein neues Modell für das Atom vor, das "Rosinenpudding" oder "Pflaumenpudding". Es wäre eine positiv geladene, nicht-massive Kugel, die mit (negativen) Elektronen verkrustet ist, so dass ihre elektrische Gesamtladung null ist.
Von Jennifer Fogaça
Abschluss in Chemie
Brasilianisches Schulteam
Allgemeine Chemie - Chemie - Brasilien Schule
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/o-experimento-thomson-com-descargas-eletricas.htm

