Ebenso wie Sulfonsäuren und die Amine, die Isonitrile sind organische Verbindungen, die aus anorganischen Substanzen stammen, genauer gesagt aus einer anorganischen Säure namens Isocyansäure.
Sie Isonitrile finden breite Anwendung bei verschiedenen organischen Synthesen (Herstellung neuer organischer Stoffe) und bei der Herstellung von Pflanzenschutzmitteln und Pflanzenschutzmitteln. Diese Verbindungen entstehen, wenn Isocyansäure mit a. reagiert Alkohol, beispielsweise. Bei dieser Reaktion wird das Wasserstoffatom der Säure durch den Alkoholrest ersetzt. Wasserstoff verbindet sich mit dem Hydroxyl von Alkohol und bildet ein Wassermolekül.
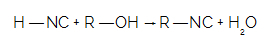
Wenn HNC mit einem Alkohol reagiert, haben wir die Bildung von Isonitril und einem Wassermolekül
Die Isocyanwasserstoffsäure, aus der Isonitrile entstehen, hat folgende Strukturformel:
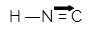
Zwischen dem Kohlenstoffatom und dem Stickstoffatom gibt es eine Doppelbindung und eine dative Bindung. Diese Region von Isonitril ist aufgrund des Resonanzphänomens zwischen den Doppelbindungselektronen und den dativen Bindungselektronen extrem polar.
Aufgrund des Resonanzeffekts zwischen dem Kohlenstoff- und Stickstoffatom haben Isonitrile eine geringere Stabilität gegenüber Nitrilen, d. h. sie können sich zersetzen (in eine andere Substanz umwandeln) leicht. Wenn ein Isonitril erhitzt wird, wandelt es sich leicht in a. um Nitril.
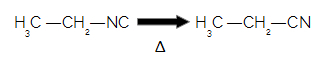
Beim Erhitzen eines Isonitrils wird es zu Nitril
Was die physikalischen Eigenschaften betrifft, Isonitrile:
sind weniger dicht als Wasser;
haben hohe Schmelz- und Siedepunkte im Vergleich zu Stoffen mit ungefährer Molmasse;
Sein physikalischer Zustand hängt von der Größe der Molmasse ab. Isonitrile mit höherer Molmasse sind fest;
Sie sind in Wasser schlecht löslich.
Um die Nomenklatur eines Isonitrils, die Regel der IUPAC (International Union of Pure and Applied Chemistry) lautet wie folgt:
Filialname + Carbylamin
HINWEIS: Der Name Carbylamin bezieht sich auf die NC-Gruppe. Daher wird jede mit dem NC verknüpfte Gruppe in der Nomenklatur als Radikal betrachtet.
Sehen Sie einige Beispiele:
Ethylcarbylamin: Isonitril mit dem Ethylradikal

Vinylcarbylamin: Isonitril mit dem Vinylradikal
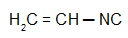
Isobutylcarbylamin: Isonitril mit dem Isobutylrest
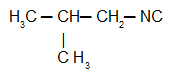
Neben der IUPAC-Nomenklatur Isonitrile haben noch die übliche Nomenklatur, geleitet von der folgenden Regel:
Isocyanid + de + Radikalname + a
Ethylisocyanid: Isonitril mit dem Ethylradikal

Vinylisocyanid: Isonitril mit dem Vinylradikal
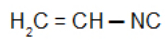
Isobutylisocyanid: Isonitril mit dem Isobutylrest:
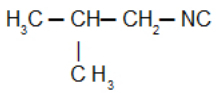
Von mir. Diogo Lopes Dias
