Sie Ester sind mit Sauerstoff angereicherte organische Verbindungen, die durch die chemische Reaktion zwischen a Carbonsäure es ist ein Alkohol. Präsentieren Sie die funktionelle Gruppe (bestehend aus zwei Sauerstoffatomen und zwei Radikale R) unten dargestellt:
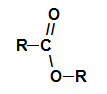
Allgemeine funktionelle Gruppe eines Esters
Was zeichnet die strukturell Ester es ist das Vorhandensein eines direkt an das Sauerstoffatom gebundenen Alkylrests. Dabei kann das am Kohlenstoff – der wiederum doppelt an Sauerstoff gebundene – Radikal (R) entweder ein Alkylrest oder ein Wasserstoffatom sein.
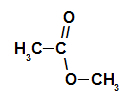
Kohlensäurekette eines Esters
Veresterungsreaktion
es geht um die chemische Reaktion, bei der aus der Wechselwirkung zwischen einer Carbonsäure und einem beliebigen Alkohol ein Ester- und ein Wassermolekül entsteht, wie in der folgenden Gleichung:
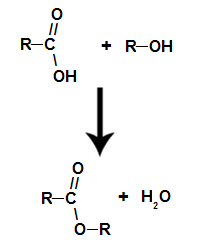
Chemische Gleichung, die die Bildung eines Esters repräsentiert
Bei der Veresterung interagiert die Hydroxylgruppe (OH) des Alkohols mit der Wasserstoff (H) ionisierbar aus dem Hydroxyl der Säure und bildet die Wassermolekül.
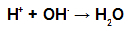
Wassermolekülbildende Gruppen bei der Veresterung
schon die Ester es entsteht durch die Verknüpfung des Restes (R) des Alkohols mit Sauerstoff, der nach der Wasserbildung vom Hydroxyl der Säure übrig bleibt.
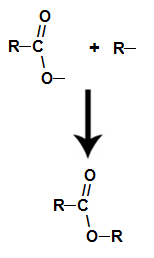
Bildung des Estermoleküls
Eigenschaften von Estern
Wichtigste physikalische Eigenschaften präsentiert von Ester:
Sie haben Frucht- und Blumenaromen;
niedrige Ester Molmasse sie sind bei Raumtemperatur flüssig und solche mit einer hohen Molmasse sind fest;
Im Vergleich zu Alkoholen und Carbonsäuren haben Ester niedrigere Schmelz- und Siedepunkte;
Im Vergleich zu Wasser sind Ester mit niedrigerer Molmasse weniger dicht;
Die Ester mit niedrigerer Molmasse sind polar und diejenigen mit höherer Molmasse sind unpolar;
In polaren Estern überwiegen die Kräfte permanenter Dipol; im Unpolaren überwiegen die Kräfte induzierten Dipol;
Ester mit niedrigerer Molmasse sind in Wasser schlecht löslich und solche mit größerer Masse sind in Wasser unlöslich.
Eine Ester-Namensregel
Vor der Verwendung der Namensregel von a Ester, ist es wichtig, sich daran zu erinnern, dass diese Verbindung durch die Vereinigung von zwei Teilen gebildet wird, von denen einer aus von Carbonsäure (in Rot) und die andere von Alkohol (in Blau), dargestellt durch Bild a Folgen:
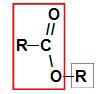
Identifizierung der Teile, aus denen der Ester entsteht
Laut der International Union of Pure and Applied Chemistry (IUPAC), lautet die offizielle Regel für die Benennung eines Esters:
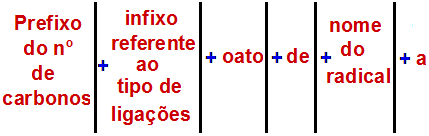
Eine Ester-Namensregel
Hinweis: Präfix und Infix entsprechen immer dem Carbonsäureteil, der Rest dem Alkoholteil.
Nachfolgend finden Sie einige Anwendungsbeispiele der Namensregel für Ester:
1. Beispiel: Himbeeressenz
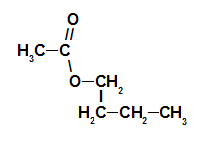
Strukturformel von Himbeeressenz-Ester
Um diesen Ester zu benennen, verwenden wir:
Nr. PräfixÖ von Kohlenstoffen: et, da die sich bildende Säure zwei Kohlenstoffe hat;
Infix zur Art der Links: ein, da die sich bildende Säure nur Einfachbindungen zwischen den Kohlenstoffen aufweist;
Der Akt;
im;
Radikale: Butyl, indem sie vier Kohlenstoffatome hintereinander aufweist;
Das.
Der Name des Esters, der der Himbeeressenz entspricht, lautet also Butylethanolat.
2. Beispiel: Tannenzapfen-Essenz
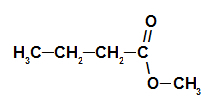
Strukturformel des Tannenzapfenesters
Um den Namen dieses Esters zu bilden, verwenden wir:
Nr. PräfixÖ von Kohlenstoffen: aber, da die bildende Säure vier Kohlenstoffe hat;
Infix zur Art der Links: ein, da die sich bildende Säure nur Einfachbindungen zwischen den Kohlenstoffen aufweist;
Der Akt;
im;
Radikale: Methyl, da der sich bildende Alkohol nur einen Kohlenstoff hat;
Das.
Der Name des Esters, der der Tannenzapfenessenz entspricht, lautet also Methylbutanoat.
3. Beispiel: Erdbeeressenz
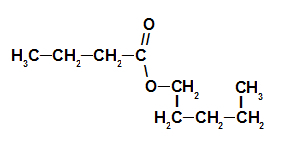
Erdbeeressenz-Ester-Strukturformel
Um diesen Ester zu benennen, verwenden wir:
Nr. PräfixÖ von Kohlenstoffen: aber, da die sich bildende Säure vier Kohlenstoffatome hat;
Infix zur Art der Links: ein, da die sich bildende Säure nur Einfachbindungen zwischen den Kohlenstoffen aufweist;
Der Akt;
im;
Radikale: Penty, da der sich bildende Alkohol fünf Kohlenstoffatome nacheinander aufweist;
Das.
Der Name des Esters, der der Erdbeeressenz entspricht, lautet also Pentylbutanoat.
Verwendung von Estern
Ester sind bekannt für ihre Verwendung als Aroma in verarbeiteten Lebensmitteln, d. h. Substanzen, die den charakteristischen Geschmack und das Aroma natürlicher Lebensmittel, wie beispielsweise Früchte, nachahmen. Außerdem, die Ester werden noch immer zur Herstellung von Arzneimitteln, Kosmetika, Parfüms und Wachsen verwendet.
Von mir. Diogo Lopes Dias
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm
