1786 sezierte der italienische Anatom Luigi Galvani (1737-1798) auf seinem Tisch einen Frosch, auf dem sich eine elektrostatische Maschine befand. Galvani beobachtete, wie sich die Muskeln des Tieres zusammenzogen, als sein Assistent versehentlich mit der Spitze seines Skalpells den inneren Nerv des Froschschenkels berührte. Mit anderen Worten, dies geschah, als das Gewebe des Frosches von zwei verschiedenen Metallen berührt wurde.
Galvani begann von diesem Moment an, eine Theorie zu verteidigen, die diese Tatsache zu erklären versuchte: die Theorie der „tierischen Elektrizität“. Laut Galvani waren Metalle nur Leiter von Elektrizität, die in Wirklichkeit in den Muskeln des Frosches enthalten wäre.
Seine Theorie war jedoch falsch und dies wurde von dem italienischen Physiker Alessandro Volta (1745-1827) gesehen, der mehrere Experimente durchführte und bemerkte, dass, wenn die Platte und der Draht aus demselben Metall waren, die Krämpfe nicht auftraten, was darauf hindeutet, dass kein Fluss von Elektrizität. So verteidigte er weiterhin die (richtige) Vorstellung, dass Elektrizität nicht aus den Muskeln des Frosches, sondern aus Metallen stammt und dass das Gewebe des Tieres diese Elektrizität leitet.
Um zu beweisen, dass er Recht hatte, machte Volta einen Stromkreis, der aus einer elektrolytischen Lösung besteht, dh einer Lösung mit Ionen gelöst, was er nassen Leiter oder Leiter zweiter Klasse nannte, in Kontakt mit zwei Elektroden gebracht metallisch. Diese letzteren nannte Alessandro Volta trockene Dirigenten oder Dirigenten erster Klasse.
Er tat dies, indem er einen nassen Leiter (der eine wässrige Salzlösung war) zwischen zwei trockene Leiter (die Metalle waren, die durch einen leitenden Draht verbunden waren) platzierte. In diesem Moment beobachtete er, dass der elektrische Fluss erwachte. Er erkannte auch, dass der Stromfluss je nach den von ihm verwendeten Metallen größer oder geringer sein konnte. Somit können wir zugeben, dass die Idee, was ein Haufen ist, bereits von Volta verstanden und erklärt wurde.
Im Jahr 1800 stellte Volta die erste elektrische Zelle her, die den Namen erhielt hinterer Stapel, galvanischer Stapel oder Voltaische Zelle und weiterhin, "Rosenkranz". Eine schematische Darstellung dieses Stapels ist unten gezeigt: Er legte eine Kupferscheibe auf eine in Schwefelsäurelösung getränkte Filzscheibe und schließlich eine Zinkscheibe; und so weiter, indem Sie diese Serien zu einer großen Spalte stapeln. Kupfer, Filz und Zink hatten ein Loch in der Mitte und wurden auf einen waagerechten Stab gefädelt und so durch einen leitenden Draht verbunden.
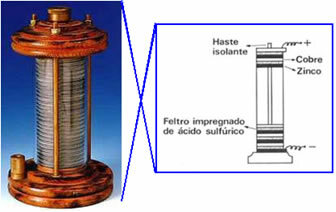
Dieses Experiment sorgte für Umwälzungen in der wissenschaftlichen Welt und fortan bei allen Geräten, die Strom aus Prozessen erzeugten Chemikalien (das heißt, die chemische Energie in elektrische Energie umwandelten) wurden als voltaische Zellen, galvanische Zellen oder einfach Batterien.
Volta führte das gleiche Experiment mit verschiedenen Metallen und Elektrolytlösungen durch, wie z. B. Silber- und Zinkscheiben, die durch in Salzlake getränkte Flanellscheiben getrennt waren. Er demonstrierte diese Entdeckung sogar für Napoleon Bonaparte, wie in der Abbildung unten zu sehen, an der Akademie der Wissenschaften in Paris.

Alessandro Volta demonstriert Napoleon seine Entdeckung
Ein weiteres Volta-Experiment mit Batterien war das Kranz aus Gläsern, in dem er zwei Platten aus verschiedenen Metallen platzierte, die durch einen leitenden Draht miteinander verbunden, aber durch Elektrolytlösungen getrennt waren.
Wir wissen jetzt, dass in einer Zelle, wie sie von Volta geschaffen wurde, Strom vom Pol fließt. negativ, Anode genannt, die oxidiert, Elektronen an den positiven Pol verliert, Kathode genannt, die reduziert, gewinnt Elektronen.
Diese in wässriger Lösung hergestellten Batterien werden heutzutage nicht viel verwendet; nur in der Forschung, aber sie waren das Prinzip, das die modernen Batterien entwickelt hat, die wir heute als Batterien kennen trocken und die viel praktischer zu verwenden und zu tragen sind und einen zufriedenstellenden elektrischen Strom für vieles mehr liefern. Zeit.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/historia-das-pilhas.htm

