DAS Gesetz der Reaktionsgeschwindigkeit setzt die Geschwindigkeit einer chemischen Umwandlung mit den Konzentrationen der Reagenzien in Stoffmenge (mol/L) in Beziehung, die wie folgt angegeben werden kann:

Betrachten Sie beispielsweise die folgende allgemeine Reaktion:
aA + bB → cC + dD
Nehmen wir an, wir erhöhen die Konzentration der Reaktanten A und B, was passiert mit der Reaktionsgeschwindigkeit? Nun, da die Menge der Reaktantenteilchen im gleichen Raum zunimmt, wird es effektivere Kollisionen zwischen ihnen geben, was zu einer Erhöhung der Reaktionsentwicklungsgeschwindigkeit führt. Das bedeutet, dass es Ihre Geschwindigkeit erhöht.
Daher ist die Reaktionsgeschwindigkeit direkt proportional zur Konzentration der Reaktanten. Es kommt aber auch auf die Temperatur an. Daher haben wir die folgende mathematische Gleichung, die das Gesetz der Reaktionsgeschwindigkeit darstellt:

Auf was:
v = Reaktionsgeschwindigkeit;
k = Konstante, die nur vom Temperaturwert abhängt;
α und β = experimentell bestimmte Exponenten.
Nur wenn die Reaktion elementar ist, also in einem einzigen Schritt abläuft, sind die Exponenten genau gleich den Koeffizienten der ausgeglichenen chemischen Gleichung: v = k. [DAS]Das. [B]B. In anderen Fällen muss jedoch die geeignete Potenz, auf die die Konzentration jedes Reagens erhöht werden muss, experimentell bestimmt werden.
Das Gesetz der Reaktionsgeschwindigkeit hat viele Namen, hier sind einige: Massenwirkungsgesetz, Schnelligkeitsgleichung, kinetisches Reaktionsgesetz und Guldberg-Waage-Gesetz.
Betrachten Sie ein Beispiel für die Anwendung dieses Gesetzes:
Betrachten Sie die folgende Elementarreaktion:
2 HCl (G) → H2(g) + Cl2(g)
a) Schreiben Sie die Gleichung für die Geschwindigkeit dieser Reaktion auf;
b) Durch Experimente wurden die Geschwindigkeit dieser Chlorwasserstoffgas-Zersetzungsreaktion und die Konzentration dieses Reagenzes bei einer konstanten Temperatur von 25 °C in der folgenden Tabelle festgehalten:
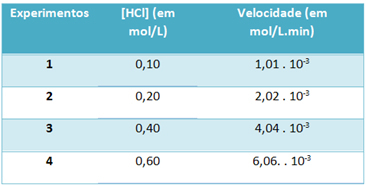
Bestimmen Sie auf dieser Grundlage die charakteristische Geschwindigkeitskonstante dieser Reaktion bei der genannten Temperatur.
Auflösung:
Das) v = k. [HCl]2
b) v = k. [HCl]2
k = __v___
[HCl]2
k = 1,01. 10-3 mol. L-1. Mindest-1
0,01 mol. L-1
k = 1,01. 10-1 Mindest-1
Um den Buchstaben „b“ zu lösen, können Sie die Daten eines der Experimente verwenden, damit der erhaltene Wert derselbe ist.
Aber was ist, wenn die Reaktion nicht elementar ist? Wie lassen sich solche Fragen in nichtelementaren Reaktionen lösen? Um herauszufinden, wie das geht, lesen Sie das Geschwindigkeitsgesetz für nichtelementare Reaktionen.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/lei-velocidade-das-reacoes-quimicas.htm

