DAS oganesson, Symbol Og, Ordnungszahl 118, ist das chemische Element mit der bisher höchsten Ordnungszahl im Periodensystem. Es kommt in der Natur nicht vor und seine Herstellung ist künstlich, daher wird es als synthetisches Element betrachtet. Trotzdem ist seine Herstellung sehr schwierig und es gilt als ein sehr seltenes Element, da es nur sehr wenige Male synthetisiert wurde.
Obwohl sie in derselben Gruppe sind wie die Edelgase, Oganesson hat laut den Berechnungen nicht viele Eigenschaften, die sich auf diese Elemente beziehen Mathematiker demonstrieren als Folge der relativistischen Effekte, dass superschwere Elemente leiden.
Element 118 wurde erstmals 2002 durch die Reaktion von Ionen synthetisiert 48Ca mit Atomen von 249Sehen Sein Name ist eine Hommage an den russischen Wissenschaftler Yuri Oganessian, einen der angesehensten und anerkanntesten auf dem Gebiet der superschweren Elemente.
Auch sehen: Rutherfordium – das synthetische chemische Element, benannt nach dem Wissenschaftler Ernest Rutherford
Zusammenfassung zu oganesson
Oganesson ist ein synthetisches chemisches Element, das in Gruppe 18 der enthalten ist Periodensystem.
Es wurde erstmals 2002 in einer gemeinsamen Arbeit russischer und amerikanischer Wissenschaftler synthetisiert.
Es bildet die Gruppe der Elemente, die zuletzt 2016 in das Periodensystem aufgenommen wurden.
Es ist ein sehr seltenes Element, das nur sehr wenige Male synthetisiert wurde.
Ihre Studien sind noch sehr jung, wobei grundlegende Eigenschaften noch durch Berechnungen und mathematische Modelle bestimmt werden.
Vorläufige theoretische Untersuchungen zeigen, dass Og trotz seiner Zugehörigkeit zur Gruppe der Edelgase einige Eigenschaften von den anderen Elementen entfernt.
Die Produktion von Oganesson erfolgt durch Kernfusion, unter Verwendung von Ionen von 48Ca und Atome von 249Sehen
Sein Name ist eine Hommage an den russischen Wissenschaftler Yuri Oganessian, einen der bedeutendsten auf dem Gebiet der Erforschung superschwerer Elemente.
Eigenschaften von Oganesson
Symbol: oh
Ordnungszahl: 118.
Atommasse: 294 cu (inoffiziell von Iupac).
Elektronische Konfiguration: [Rn] 7s2 5f14 6d10 19 Uhr6.
Stabilstes Isotop: 294Og (0,69 Millisekunden Halbwertszeit, die um 0,64 Millisekunden erhöht oder um 0,22 Millisekunden verringert werden kann).
Chemische Reihe: Gruppe 18, superschwere Elemente, Edelgase.
Eigenschaften von Oganesson
Oganesson ist der Element mit der höchsten Ordnungszahl (118), das bisher offiziell gemacht wurde von der International Union of Pure and Applied Chemistry (IUPAC). Obwohl es erstmals im Jahr 2002 produziert wurde, über ihn ist wenig bekannt. Es wird noch viel spekuliert, da dieses Element in der Natur nicht vorkommt. Seine Herstellung erfolgt im Labor, das es als synthetisches Element konfiguriert.
Außerdem, dein Halbwertzeit ist weniger als eine Millisekunde (10-3 zweitens) – Denken Sie daran, dass die Halbwertszeit die Zeit ist, die erforderlich ist, damit sich die Menge halbiert. Daher sind die Eigenschaften, die für dieses Element festgelegt werden, nichts anderes als die Ergebnisse von theoretische Berechnungen auf Basis mathematischer Modelle, denn in der Region des Periodensystems, in der es sich befindet findet die relativistische Effekte (die Diskrepanz zwischen erwarteten und beobachteten Effekten als Ergebnis der Relativitätstheorie) signifikant sind.
Relativistische Effekte nehmen Og von dem ab, was von ihm erwartet wurde. Das Element bspw. hat kein ähnliches Verhalten wie Edelgase. Berechnungen zeigen, dass Oganesson bei Raumtemperatur ein Feststoff mit einem Schmelzpunkt wäre im Bereich von 325 ± 15 K (etwa 52 °C) und einem Siedepunkt im Bereich von 450 ± 10 K (etwa 177 °C). °C).
Es ist auch bekannt, dass Og reaktiver sein kann als andere Edelgase, da es aufgrund relativistischer Effekte leichter Elektronen der p-Unterebene abgeben kann. Ein weiterer Streitpunkt mit den Edelgasen ist, dass Oganesson a Halbleiter, während die anderen Isolatoren sind.
Lesen Sie auch: Wasserstoff – das chemische Element mit der niedrigsten Ordnungszahl im Periodensystem
Oganesson erhalten
Wie andere superschwere Elemente wird Oganesson durch eine Technik namens The gewonnen heiße Schmelze, wo Ionen des Isotops 48Ca, das natürlich vorkommt, aber sehr wenig verfügbar ist, reagiert mit viel schwereren Isotopen, um die superschweren Elemente zu erzeugen.
Og ist ein so seltenes und schwer zu beschaffendes Element, dass In zehn Jahren nur vier Atome kam um produziert zu werden. Grundsätzlich ist die Herstellung von 294Og, das einzige bekannte Isotop, entsteht durch Beschuss mit Ionen 48Ca zu einem Kern von 249Vgl. mit Freisetzung von 3 Neutronen.
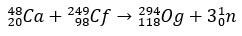
Mit wenigen Millisekunden Halbwertszeit ist der Og wurde anhand seines Zerfallsmusters identifiziert, etwas sehr häufiges für superschwere Elemente. In diesem Fall traten 3-Alpha-Zerfälle auf, wodurch Element 118 zu Copernicium, Cn, wurde, das schließlich einer spontanen Spaltung unterzogen wurde.
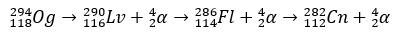
Geschichte von Oganesson
Die erste Synthese von Oganesson fand 2002 statt., in der Stadt Livermore, Kalifornien, USA, im Lawrence Livermore National Laboratory, wo eine Gruppe amerikanischer Wissenschaftler arbeitete mit russischen Forschern zusammen des berühmten Joint Institute for Nuclear Research (JINR) unter der Leitung des russischen Wissenschaftlers Yuri Oganessian.
In einem Zeitraum von zehn Jahren seit der ersten Synthese wurden aufgrund der Seltenheit und Schwierigkeit der Reaktionsparameter nur vier Atome Oganesson synthetisiert. Das vierte und letzte Atom präsentierte jedoch eine unglaubliche Entdeckung.
Wissenschaftler versuchten, Element 117 durch die Reaktion von zu synthetisieren 48Ca mit dem 249Bk, jedoch wurde festgestellt, dass 28 % des Berkelium-Targets einen β-Zerfall durchmachten, der sich in umwandelte 249Cf und somit Element 118 erzeugen. Bemerkenswert ist das Der Name des Elements 118 ehrt den russischen Wissenschaftler Yuri Oganessian, eine Hommage an lebende Chemiker, die es in der Geschichte der Chemie nur zweimal gegeben hat, die erste an Glenn Seaborg, mit der Seaborgium.
Gelöste Übungen zu Oganesson
Frage 1
Oganesson, Element mit der Ordnungszahl 118 und dem Symbol Og, wurde in die siebte Periode des Periodensystems in die Gruppe der Edelgase eingeordnet. Infolgedessen wurde viel darüber spekuliert, ob ein solches Element eine große Stabilität aufweisen würde, eine Eigenschaft, die den anderen Elementen dieser Gruppe bekannt ist. Die Zuordnung von Og in Gruppe 18 erfolgte aufgrund von:
A) Dieses Element ist sehr stabil.
B) Dieses Element hat acht Elektronen in seiner Valenzschale.
C) Dieses Element ist bei Raumtemperatur nachweislich ein Gas.
D) dieses Element hat die gleichen chemischen Eigenschaften wie die anderen Edelgase.
E) Dieses Element hat eine hohe Ionisierungsenergie.
Auflösung:
AlternativeB
Die Zuteilung des Og erfolgt einzig und allein aufgrund dessen elektronische Verteilung. Die Tatsache, dass es acht Elektronen enthält Valenzschicht, 7s2 19 Uhr6, bringt es in diese Position. Studien mit diesem Element sind noch vorläufig, aber aufgrund mathematischer Ergebnisse wird bereits spekuliert, dass beispielsweise Og bei Raumtemperatur kein Gas ist. Ein weiterer hervorzuhebender Punkt ist, dass Og überhaupt nicht stabil ist, nicht einmal in der Natur existiert.
Frage 2
Die große Schwierigkeit bei der Herstellung von Element 118 lässt vermuten, dass sich Wissenschaftler auf einer wahren Odyssee befanden, um es nachweisen zu können. Kein Wunder, nach zehn Jahren seiner ersten Synthese wurde Oganesson nur drei weitere Male synthetisiert. Und bisher ist nur ein Isotop bekannt, das 294oh Wie viele Neutronen hat das bekannte Isotop von Oganesson?
A) 294.
b) 118.
c) 176.
D) 412.
E) 166.
Auflösung:
Alternative C
Die Zahl der Neutronen von Og kann wie folgt berechnet werden:
A = Z + n
A ist die Zahl der Pasta atomar, Z ist die Anzahl der Protonen (oder Ordnungszahl) und n ist die Anzahl der Neutronen. Durch Einsetzen der Werte erhalten wir:
294 = 118 + n
n = 294 - 118
n = 176
Von Stefano Araújo Novais
Chemielehrer
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/oganessonio-og.htm


