Die periodischen Eigenschaften chemischer Elemente sind die Eigenschaften, die sie besitzen.
Beachten Sie, dass die chemischen Elemente im Periodensystem eine bestimmte Position haben, die je nach den periodischen Eigenschaften, die sie aufweisen, variiert. Sie sind nach der Ordnungszahl aufsteigend sortiert.
Nach Moseleys Gesetz:
“Viele physikalische und chemische Eigenschaften von Elementen variieren periodisch in der Reihenfolge der Ordnungszahlen der Elemente..”
Periodische Haupteigenschaften
Atomradius
Bezogen auf die Größe von Atomen wird diese Eigenschaft durch den Abstand zwischen den Zentren der Kerne zweier Atome desselben Elements definiert.
deshalb, die Atomstrahl entspricht dem halben Abstand zwischen den Kernen zweier benachbarter Atome, ausgedrückt wie folgt:
r = d/2
Wo:
r: Blitz
d: internuklearer Abstand
Es wird gemessen in Pikometer (pm). Diese Messung ist ein Teiler des Meters:
13 Uhr = 10-12 ich
Im Periodensystem nimmt der Atomradius in vertikaler Position von oben nach unten zu. In der Horizontalen nehmen sie von rechts nach links zu.
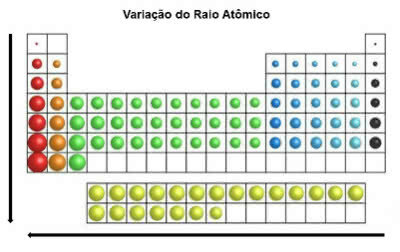
Variation des Atomradius
Das chemische Element mit dem größten Atomradius ist Cäsium (Cs).
Atomvolumen
Diese periodische Eigenschaft gibt das Volumen an, das 1 Mol des Elements im festen Zustand einnimmt.
Es ist erwähnenswert, dass das Atomvolumen nicht das Volumen von 1 Atom ist, sondern ein Satz von 6,02. 1023 Atome (1 Molwert)
Das Atomvolumen eines Atoms wird nicht nur durch das Volumen jedes Atoms definiert, sondern auch durch den Abstand zwischen diesen Atomen.
Im Periodensystem nehmen die atomaren Volumenwerte von oben nach unten (vertikal) und von der Mitte zum Rand (horizontal) zu.

Variation des Atomvolumens
Um das Atomvolumen zu berechnen, wird die folgende Formel verwendet:
V = m/d
Wo:
V: Atomvolumen
ich: Masse von 6.02. 1023 Elementatome
d: Festkörperelementdichte
Absolute Dichte
DAS Dichte absolut, auch „spezifische Masse“ genannt, ist eine periodische Eigenschaft, die das Verhältnis zwischen der Masse (m) eines Stoffes und dem von dieser Masse eingenommenen Volumen (v) bestimmt.
Es wird nach folgender Formel berechnet:
d = m/v
Wo:
d: Dichte
ich: Pasta
v: Lautstärke
Im Periodensystem nehmen die Dichtewerte von oben nach unten (vertikal) und von den Kanten zur Mitte (horizontal) zu.
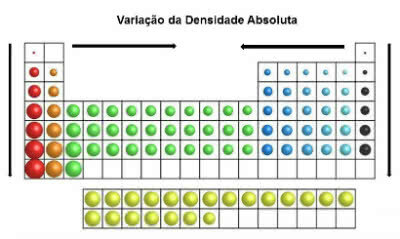
Absolute Dichtevariation
Somit befinden sich die dichtesten Elemente in der Mitte und am unteren Rand der Tabelle:
Osmium (Os): d= 22,5 g/cm3
Iridium (Ir): d = 22,4 g/cm3
Schmelzpunkt und Siedepunkt
Eine weitere wichtige periodische Eigenschaft hängt mit den Temperaturen zusammen, bei denen Elemente in schmelzen und kochen.
Der Schmelzpunkt (MP) ist die Temperatur, bei der Materie von der festen in die flüssige Phase übergeht. Der Siedepunkt (PE) ist die Temperatur, bei der Materie von der flüssigen in die gasförmige Phase übergeht.
Im Periodensystem variieren die Werte von PF und PE je nachdem, welche Seiten in der Tabelle positioniert sind.
Vertikal und auf der linken Seite der Tabelle nehmen sie von unten nach oben zu. Auf der rechten Seite nehmen sie von oben nach unten zu. In horizontaler Richtung erstrecken sie sich von den Enden zur Mitte.

Schmelz- und Siedepunktvariation
Elektronische Affinität
Auch „Elektroaffinität“ genannt, ist die Mindestenergie, die ein chemisches Element benötigt, um einem Anion ein Elektron zu entziehen.
Das heißt, die elektronische Affinität gibt an, wie viel Energie freigesetzt wird, wenn ein Elektron von einem Atom aufgenommen wird.
Beachten Sie, dass dieses instabile Atom allein und in einem gasförmigen Zustand ist. Mit dieser Eigenschaft erhält es Stabilität, wenn es das Elektron aufnimmt.
Im Gegensatz zum Atomradius wächst die Elektroaffinität der Elemente im Periodensystem horizontal von links nach rechts. In vertikaler Richtung nimmt sie von unten nach oben zu.
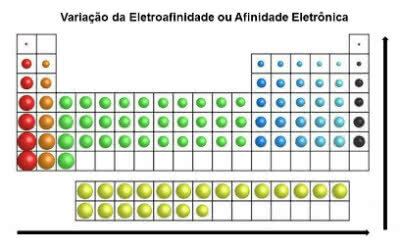
Elektronische Affinitätsvariation
Das chemische Element mit der größten Elektronenaffinität ist Chlor (Cl) mit einem Wert von 349 KJ/mol.
Ionisationsenergie
Auch genannt "Ionisationspotential“, steht diese Eigenschaft im Gegensatz zu der der elektronischen Affinität.
Es ist die minimale Energie, die ein chemisches Element benötigt, um einem neutralen Atom ein Elektron zu entziehen.
Somit gibt diese periodische Eigenschaft an, wie viel Energie benötigt wird, um das Elektron von einem Atom in einen Grundzustand zu übertragen.
Der sogenannte „Grundzustand eines Atoms“ bedeutet, dass seine Protonenzahl gleich seiner Elektronenzahl ist (p+ = und-).
Nachdem ein Elektron aus dem Atom entfernt wurde, wird es also ionisiert. Das heißt, es bekommt mehr Protonen als Elektronen und wird daher zu einem Kation.
Im Periodensystem ist die Ionisationsenergie der des Atomradius entgegengesetzt. Er nimmt also von links nach rechts und von unten nach oben zu.
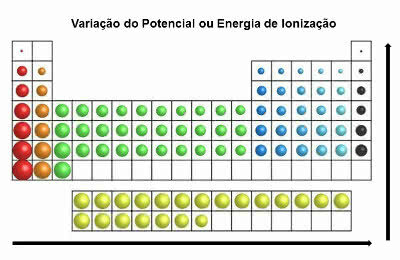
Variation der Ionisationsenergie
Die Elemente mit dem größten Ionisationspotential sind Fluor (F) und Chlor (Cl).
Elektronegativität
Eigenschaft von Atomen von Elementen, die dazu neigen, Elektronen in einer chemischen Bindung aufzunehmen.
Es tritt in kovalenten Bindungen zum Zeitpunkt der gemeinsamen Elektronenpaare auf. Beim Empfangen von Elektronen bleiben Atome mit einer negativen Ladung (Anion) zurück.
Denken Sie daran, dass dies als die wichtigste Eigenschaft des Periodensystems gilt. Dies liegt daran, dass die Elektronegativität das Verhalten von Atomen induziert, aus denen Moleküle gebildet werden.
Im Periodensystem ist die Elektronegativität nimmt von links nach rechts (horizontal) und von unten nach oben (vertikal) zu
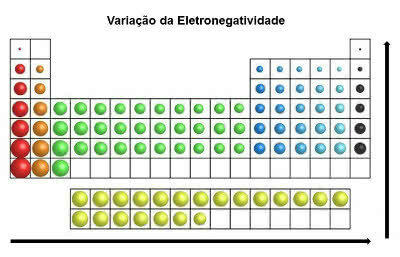
Elektronegativitätsvariation
Somit ist Fluor (F) das elektronegativste Element im Periodensystem. Auf der anderen Seite sind Cäsium (Cs) und Francium (Fr) die am wenigsten elektronegativen Elemente.
Elektropositiv
Im Gegensatz zur Elektronegativität weist diese Eigenschaft von Elementaratomen auf Tendenzen hin, Elektronen in einer chemischen Bindung zu verlieren (oder abzugeben).
Beim Elektronenverlust werden die Atome der Elemente positiv geladen und bilden so ein Kation.
In gleicher Richtung wie der Atomradius und entgegen der Elektronegativität im Periodensystem a Elektropositiv nimmt von rechts nach links (horizontal) und von oben nach unten (vertikal) zu.
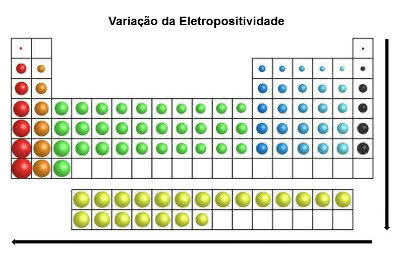
Variation der Elektropositivität
Die chemischen Elemente mit der höchsten Elektropositivität sind Metalle, daher wird diese Eigenschaft auch „metallischer Charakter“ genannt. Das elektropositivste Element ist Francium (Fr) mit maximaler Oxidationsneigung.
Beachtung!
Sie "Edelgase“ sind inerte Elemente, da sie keine chemischen Bindungen eingehen und kaum Elektronen abgeben oder aufnehmen. Außerdem haben sie Schwierigkeiten, mit anderen Elementen zu reagieren.
Daher werden die Elektronegativität und Elektropositivität dieser Elemente nicht berücksichtigt.
Lesen Sie auch:
- Chemische Bindungen
- Geschichte des Periodensystems
- Periodensystem-Familien
Aperiodische Eigenschaften
Neben periodischen Eigenschaften haben wir aperiodische Eigenschaften. In diesem Fall erhöhen oder verringern sich die Werte mit der Ordnungszahl der Elemente.
Sie erhalten diesen Namen, da sie ihrer Position im Periodensystem nicht wie periodische gehorchen. Das heißt, sie werden nicht zu regelmäßigen Zeiten wiederholt.
Die wichtigsten aperiodischen Eigenschaften sind:
- Atommasse: Diese Eigenschaft nimmt mit zunehmender Ordnungszahl zu.
- Spezifische Wärme: diese Eigenschaft nimmt mit steigender Ordnungszahl ab. Denken Sie daran, dass die spezifische Wärme die Wärmemenge ist, die benötigt wird, um die Temperatur von 1 g des Elements um 1 °C zu erhöhen.
Aufnahmeprüfungsübungen mit Feedback
1. (PUC-RJ) Betrachten Sie die Aussagen über Elemente der Gruppe IA im Periodensystem
ICH. Sie werden Alkalimetalle genannt.
II. Seine Atomstrahlen wachsen mit der Ordnungszahl.
III. Sein Ionisationspotential steigt mit der Ordnungszahl.
IV: Sein metallischer Charakter nimmt mit der Ordnungszahl zu.
Unter den Aussagen sind wahr:
a) I und II
b) III und IV
c) I, II und IV
d) II, III und IV
e) I, II, III und IV
Alternative c
2. (UFMG) Vergleicht man Chlor und Natrium, die beiden chemischen Elemente, die Speisesalz bilden, kann man sagen, dass Chlor:
a) ist dichter.
b) ist weniger flüchtig.
c) hat einen stärkeren metallischen Charakter.
d) hat eine niedrigere Ionisierungsenergie.
e) hat einen kleineren Atomradius.
Alternativ und
3. (UFC-CE) Der photoelektrische Effekt besteht in der Emission von Elektronen von metallischen Oberflächen durch den Einfall von Licht geeigneter Frequenz. Dieses Phänomen wird direkt durch das Ionisationspotential von Metallen beeinflusst, die weitgehend Verwendung bei der Herstellung von photoelektronischen Geräten, wie: Lichtschranken für die öffentliche Beleuchtung, Kameras fotografisch usw. Markieren Sie basierend auf der Variation des Ionisationspotentials der Elemente im Periodensystem die Alternative, die das Metall enthält, das am wahrscheinlichsten den photoelektrischen Effekt zeigt.
a) Fe
b) Hg
c) Cs
d) Mg
e) Ca
Alternative c
Prüfen Sie die Prüfungsfragen mit einer kommentierten Auflösung in Übungen zum Periodensystem und unveröffentlichte Fragen zum Thema in Übungen zur Organisation des Periodensystems.
Lesen Sie auch:
- Periodensystem
- Elektronische Verteilung
- Chemische Elemente
- Intermolekularen Kräfte