Empfindliche Wärme oder empfindliche spezifische Wärme ist eine physikalische Größe, die sich auf die Temperaturänderung eines Körpers bezieht.
Beispiel: Erhitzen einer Metallstange
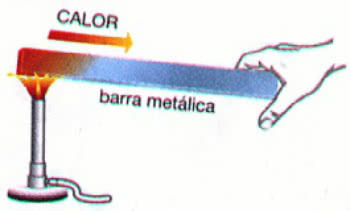
Im obigen Beispiel breitet sich die Wärme durch die Wärmeleitung. Dieser Vorgang führt zu einer Temperaturerhöhung des Materials, sein physikalischer Zustand bleibt jedoch gleich (fest).
Formel
Um die fühlbare Wärme zu berechnen, verwenden Sie die folgende Formel:
Q = m. ç. Δθ
Q: fühlbare Wärmemenge (Kalk oder J)
ich: Körpermasse (g oder kg)
ç: spezifische Wärme des Stoffes (cal/g°C oder J/Kg°C)
Δθ: Temperaturschwankung (°C oder K)
Hinweis: Um die fühlbare Wärme zu berechnen, müssen wir die spezifische Wärme kennen, die in jedem Stoff variiert.
Lesen Sie mehr unter: Spezifische Wärme.
Empfindliche Hitze und latente Hitze
Bei der latente Wärme (L) ändert sich der physikalische Zustand des Stoffes, während er bei fühlbarer Wärme gleich bleibt.
Ein weiterer Unterschied zwischen den beiden ist die Temperatur. Das heißt, latente Wärme ist unabhängig von der Körpertemperatur, während sensible Wärme sie berücksichtigt.
Ein Beispiel für latente Wärme ist das Schmelzen eines Eiswürfels oder die Verdunstung von Wasser. In beiden Fällen bleibt die Temperatur in den beiden physikalischen Zuständen gleich.
Um die latente Wärme zu berechnen, verwenden Sie die folgende Formel:
Q = m. L
Wo,
Q: Wärmemenge (Kalk oder J)
ich: Masse (g oder kg)
L: latente Wärme (cal/g oder J/Kg)
Lesen Sie auch:
- Hitze und Temperatur
- Kalorimetrie
- Wärmebilanz
- Wärmekapazität
- Physikalische Formeln
Aufnahmeprüfungsübungen mit Feedback
1. (Mackenzie) Eine Wärmequelle liefert kontinuierlich Wärme mit einer Geschwindigkeit von 150 cal/s an eine gegebene Wassermasse. Wenn die Wassertemperatur in 4 Minuten von 20 °C auf 60 °C ansteigt, wobei die spezifische Wärmeempfindlichkeit des Wassers 1,0 cal/g °C beträgt, kann geschlossen werden, dass die Masse des erhitzten Wassers in Gramm beträgt:
a) 500
b) 600
c) 700
d) 800
e) 900
Alternativ und
2. (UFSM-RS) Ein 400 g Körper und eine empfindliche spezifische Wärme von 0,20 cal/g °C, bei einer Temperatur von 10 °C, wird platziert in thermischem Kontakt mit einem weiteren 200 g Körper und sensibler spezifischer Wärme von 0,10 cal/g° C, bei einer Temperatur von 60°C. Die Endtemperatur, sobald das Wärmegleichgewicht zwischen den beiden Körpern hergestellt ist, beträgt:
a) 14°C
b) 15 °C
c) 20°C
d) 30°C
e) 40°C
Alternative c
3. (UFPR) Während der Sonnenfinsternis gab es in einer der Städte der Totalitätszone, Criciúma - SC, einen Temperaturabfall von 8,0 °C. (Null Stunden – 11.04.1994)
Wenn man weiß, dass die empfindliche spezifische Wärme von Wasser 1,0 cal/g °C beträgt, beträgt die Wärmemenge, die von 1000 g Wasser bei der Reduzierung seiner Temperatur von 8,0 °C in Kalk freigesetzt wird:
a) 8,0
b) 125
c) 4000
d) 8000
e) 64000
Alternative