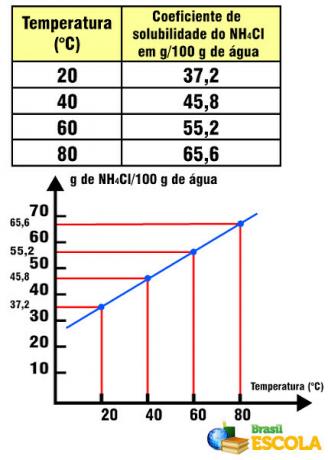
pH stellt das Wasserstoffionenpotential dar und pOH ist das Hydroxyionenpotential der Lösungen.
Dies sind logarithmische Skalen, die verwendet werden, um den sauren und basischen Charakter einer Probe zu messen.
Die Werte, aus denen sie bestehen, reichen von 0 bis 14 und wurden aus dem Ionengleichgewicht von Wasser erhalten.
Eine neutrale Lösung hat einen pH-Wert von 7. Werte unter 7 klassifizieren die Lösungen als sauer, während nach 7 die Lösungen basisch sind.
Mit dem pH-Wert ist es möglich, den entsprechenden pH-Wert auf der pOH-Skala einfach durch Subtraktion zu finden.
Ionischer Wasserhaushalt
Ein Wassermolekül hat die Fähigkeit, nach folgender Gleichung zu ionisieren:
Hier haben wir ein Ionengleichgewicht, denn der Vorgang ist reversibel und die Ionen können auch wieder zusammenkommen und wieder ein Wassermolekül bilden.
Eine andere Möglichkeit, das auftretende Gleichgewicht zu demonstrieren, ist durch die Autoionisierung.
Ein Wassermolekül erzeugte Hydroniumionen (H3Ö+) und Hydroxyl (OH-) durch die Zerstörung eines zweiten Moleküls.
Ionisches Produkt von Wasser (Kw)
Die Konstante für das Ionengleichgewicht von Wasser ist:
Da Wasser eine reine Flüssigkeit ist, wird seine Konzentration als 1 angenommen und stört den konstanten Wert nicht. Daher wird der Ausdruck:
Ö ionisches Produkt von Wasser é .
Dieser Ausdruck erhält das Symbol Kw (W kommt vom englischen Wort Wasser - Wasser) und variiert wie die Gleichgewichtskonstante mit der Temperatur.

Bestimmung von pH und pOH
Bei einer Temperatur von 25°C ist das ionische Produkt von Wasser:
Bei der Ionisierung von reinem Wasser wird 1 mol H3Ö+ entsteht mit 1 mol OH- .
Bald,
Da diese Werte extrem niedrig sind, hat man sich entschieden, die Werte von Kologarithmen zu verwenden, die dem Logarithmus mit vertauschtem Vorzeichen entsprechen.
Wenden wir den Kologarithmus auf das ionische Produkt von Wasser an, müssen wir:
Wir können Folgendes beobachten: Wenn wir den pH-Wert einer Lösung kennen, können Sie den pOH-Wert ermitteln, indem Sie den ersten Wert von 14 subtrahieren.
Säure und Basizität der Lösungen
Neutrale Lösung: Die Konzentration der Hydroniumionen ist gleich der der Hydroxyle.
| [H3Ö+] = 1,0. 10-7 mol/L | pH = 7 |
| [Oh-] = 1,0. 10-7 mol/L | pOH = 7 |
Beispiel: reines Wasser.
Säurelösung: Die Konzentration von Hydroniumionen ist höher als die von Hydroxylen.
| [H3Ö+] |
pH |
| [Oh-] |
pOH |
Beispiel: Soda, Zitrone und Tomate.
Grundlösung: Die Konzentration an Hydroxylen ist höher als die der Hydroniumionen.
| [H3Ö+] |
pH |
| [Oh-] |
pOH |
Beispiel: Ei, Seife und Bleichmittel.
pH-Berechnung
Das Konzept des Wasserstoffpotentials wurde von dem dänischen Chemiker Peter Lauritz Sorensen (1868-1939) entwickelt, um den Säuregehalt einer Lösung durch die Konzentration von H. auszudrücken+.
Siehe die folgende Tabelle, die die Ionisierung von a. zeigt Acid:
| Anfangsmolarität | 0,020 | 0 | 0 |
| Ionisation | 0,001 | 0,001 | 0,001 |
| Molarität im Gleichgewicht | 0,019 | 0,001 | 0,001 |
Im Beispiel haben wir, dass die Konzentration von H-Ionen+ é 0,001. Daher ist der pH-Wert der Lösung:
[H+] = 0,001 = 10-3
pH = - log 10-3 = 3
Da der pH-Wert der Lösung weniger als 7 beträgt, ist diese Lösung sauer.
Zusammenfassung zu pH und pOH
| Definitionen | pH: Wasserstoffionenpotential der Lösung. | |
|---|---|---|
| pOH: Hydroxylionisches Potential der Lösung. | ||
| allgemeine Formel | pH + pOH = 14 | |
| Lösungen | Neutral | pH = pOH = 7 |
| sauer |
pH pOH > 7 |
|
| Grundlagen |
pOH pH-Wert > 7 |
|
| pH-Berechnung | pH = -log [H+] | |
| Berechnung von pOH | pOH = -log[OH-] |
Übungen zu pH und pOH
1. (FMTM) Der pH-Wert von Magensaft, einer wässrigen Salzsäurelösung (HCℓ), beträgt ungefähr 2. Daher beträgt die in jedem Liter Magensaft vorhandene Masse an HCℓ in Gramm
Daten: Molmassen (g/mol) H = 1, Cℓ = 35,5
a) 7,3 · 10-2
b) 3,65 · 10-1
c) 10-2
d) 2
e) 10
Richtige Alternative: b) 3,65 · 10-1.
1. Schritt: Berechnen Sie die Konzentration der H-Ionen+.
2. Schritt: Berechnen Sie die Molmasse von HCl.
3. Schritt: Berechnen Sie die Salzsäuremasse in jedem Liter Magensaft.
2. (UEMG) Mehrere Reinigungsmittel enthalten Ammoniak in ihrer Zusammensetzung. Das Etikett eines dieser Produkte zeigt pH = 11 an. Dies bedeutet, dass die Konzentration von Hydroxon-Kationen und Hydroxyl-Anionen in diesem Produkt jeweils beträgt:
bis 1. 10-3 und 1. 10-11
b) 1. 10-11 und 1. 10-7
c) 1. 10-11 und 1. 10-3
d) 1. 10-11 und 1. 10-11
Richtige Alternative: c) 1. 10-11 und 1. 10-3.
eine falsche. Diese Konzentrationen entsprechen einer Lösung mit pH = 3.
b) FALSCH. Obwohl die Konzentration von H+ geben an, dass der pH-Wert der Lösung 11 beträgt, die Konzentration der OH-Ionen- ist falsch, da es 3 sein sollte, denn: pOH = 14 - pH.
c) RICHTIG. pH = 11 und pOH = 3, da pH + pOH = 14.
d) FALSCH. Obwohl die Konzentration von H+ geben an, dass der pH-Wert der Lösung 11 beträgt, die Konzentration der OH-Ionen- ist falsch, da es 3 sein sollte, denn: pOH = 14 - pH.
a) 0,1 mol/L NaOH
b) NaCl 0,5 mol/L
CH2NUR4 1,0 mol/l
d) 1,0 mol/l HCl
e) 0,2 mol/L KOH
Richtige Alternative: e) KOH 0,2 mol/L.
eine falsche. Die Lösung ist basisch, da ihr pH-Wert über 7 liegt, sie hat jedoch nicht den höheren pH-Wert der Alternativen.
b) FALSCH. NaCl ist ein Salz, da es das Produkt einer starken Säure-Base-Reaktion ist. Daher ist sein pH-Wert neutral.
c) FALSCH. Schwefelsäure ist eine starke Säure, daher ist ihr pH-Wert niedrig.
d) FALSCH. Salzsäure ist eine starke Säure, daher ist ihr pH-Wert niedrig.
e) RICHTIG. Die Lösung ist basisch, da ihr pH-Wert über 7 liegt.