Wie im Text „Arten intermolekularer Kräfte“ erläutert, werden die Moleküle von Stoffen in den drei Aggregatzuständen (fest, flüssig und gasförmig) von einer der intermolekularen Kräfte angezogen.
Die drei bekannten intermolekularen Kräfte sind: induzierter Dipol - induzierter Dipol, permanenter Dipol - permanenter Dipol und Wasserstoffbrückenbindung. Unter ihnen ist die Wasserstoffbrücke die stärkste. Einige Autoren bezeichneten diese intermolekulare Kraft als Wasserstoffbrückenbindungen; der korrekte von der IUPAC akzeptierte Begriff ist jedoch „Wasserstoffbrücken“.
Diese Art von Wechselwirkung tritt auf, wenn das Molekül Wasserstoff an Fluor, Stickstoff oder Sauerstoff gebunden hat, die stark elektronegative Atome sind.

Die Wasserstoffbrücke ist ein extremes Beispiel für die permanente Dipol-permanente Dipolbindung. Denn der Wasserstoff eines Moleküls bildet einen positiven Pol, der an eines der Fluor-, Sauerstoff- oder Stickstoffatome eines anderen Moleküls bindet, die seinen negativen Pol bilden.
Normalerweise treten intermolekulare Bindungen mit Stoffen im flüssigen und festen Zustand auf. Da es sich um eine sehr starke Anziehungskraft handelt, ist außerdem eine sehr hohe Energie erforderlich, um sie zu brechen.
Eine Substanz, die diese intermolekulare Kraft besitzt, ist Wasser selbst. Beachten Sie, wie dies in der folgenden Abbildung geschieht:
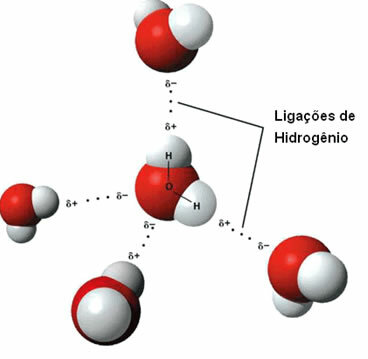
Beachten Sie, dass jedes Wassermolekül räumlich von vier anderen Wassermolekülen umgeben ist, wobei die Bindungen von Wasserstoff entstehen durch die Bindung zwischen dem Wasserstoff eines Moleküls (positiver Pol) mit dem Sauerstoff eines anderen (Pol Negativ).
Wasserstoffbrückenbindungen erklären verschiedene Phänomene in der Natur, siehe folgende Beispiele:
- Dass Eis auf Wasser schwimmt: Eis ist weniger dicht als Wasser und schwimmt folglich darauf. Denn während im flüssigen Zustand die zwischen Wassermolekülen auftretenden Wasserstoffbrückenbindungen desorganisiert sind, sind die Wasserstoffbrückenbindungen im Eismoleküle sind in größerem Abstand und organisierter und bilden eine starre hexagonale Struktur, wodurch die Moleküle einen viel größeren Raum einnehmen, als sie es in diesem Zustand tun würden. Flüssigkeit.

Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Das ist auch der Grund, warum sich das Volumen einer Flasche ausdehnt und die Flasche bricht, wenn wir das volle Volumen einer Flasche und später in einen Kühler füllen.
Somit gibt es die gleiche Menge an Molekülen pro Volumeneinheit, was die Dichte nach der Dichteformel verringert: d = m/v. Zwischen den gebildeten Sechsecken entstehen Leerräume, die die Dichte dieser Substanz verringern.
- Säureionisation: Obwohl Wasserstoffbrücken etwa zehnmal schwächer sind als kovalente Bindungen; unter Umständen gelingt es ihnen, die kovalenten Bindungen aufzubrechen. Im unten gezeigten Fall wird beispielsweise Salzsäure in Wasser gelöst. Der Sauerstoff im Wasser zieht den an das Chlor der Säure gebundenen Wasserstoff stärker an als das Chlor selbst, wodurch Hydroniumionen (H3Ö+) und Chlorid (Cl-). Dieses Phänomen wird Ionisation genannt:
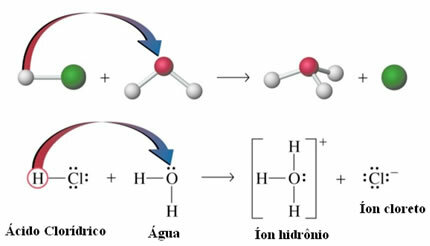
- Oberflächenspannung von Wasser: die Moleküle auf der Flüssigkeitsoberfläche werden von Wasserstoffbrücken nur mit den Molekülen daneben und darunter angezogen, da sich darüber keine Moleküle befinden. Die unter der Oberfläche befindlichen Moleküle hingegen führen diese Art der Bindung mit Molekülen in allen durch in Richtungen entsteht eine Art Film oder dünne Schicht auf der Wasseroberfläche, die beinhaltet.
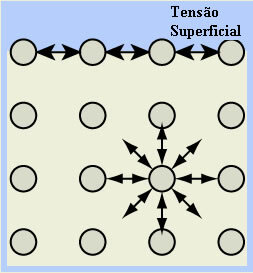
Dies erklärt die Tatsache, dass Insekten darauf verbleiben können und auch das Phänomen der Kugelform von Wassertropfen.

Von Jennifer Fogaça
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Wasserstoffbrücken"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/ligacoes-hidrogenio.htm. Zugriff am 27. Juni 2021.
Chemie

Wasserverschmutzung, physikalische Aspekte des Wassers, chemische Aspekte des Wassers, biologische Aspekte des Wassers, Industrieabfälle, Schwermetalle, Trinkwasser, organische Stoffe, Wassertrübung, Abwasser.


