DAS Enthalpie (H) sie kann als Energieinhalt jedes Materials oder als Gesamtenergie eines Systems definiert werden. In der Praxis ist es jedoch nicht möglich, die Enthalpie eines Stoffes zu bestimmen. Was normalerweise gemessen wird, ist also die Enthalpievariation 

Wir werden hier die Variation der Enthalpie bei exothermen Reaktionen analysieren (das Wort „exo“ kommt aus dem Griechischen und bedeutet „aus, aus, aus“), also Reaktionen, bei denen Wärme freigesetzt wird. Im Alltag gibt es viele Beispiele für diese Reaktionen, wie die Verbrennung und die Mischung von Branntkalk mit Wasser.
In diesen Fällen ist die Enthalpievariation 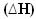 ist genau die freigesetzte Wärmemenge, gegeben durch den Wert der Endenthalpie minus der Anfangsenthalpie (Hf - Hich) oder, da es sich um eine Reaktion handelt, der Enthalpiewert der Produkte minus dem der Reaktionspartner (HP - HR).
ist genau die freigesetzte Wärmemenge, gegeben durch den Wert der Endenthalpie minus der Anfangsenthalpie (Hf - Hich) oder, da es sich um eine Reaktion handelt, der Enthalpiewert der Produkte minus dem der Reaktionspartner (HP - HR).
Da Wärme freigesetzt wird, geht Energie verloren. Dadurch sinkt die Gesamtenergie des Systems, so dass die Enthalpie der Produkte immer kleiner ist als die der Reagenzien, so dass die Enthalpieänderung bei exothermen Reaktionen immer negativ ist, kleiner als Null
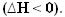
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
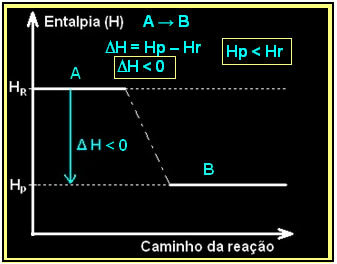
Betrachtet man eine generische exotherme Reaktion:
| A → B + Wärme |
Dies kann mit einem Enthalpiediagramm wie dem folgenden ausgedrückt werden:
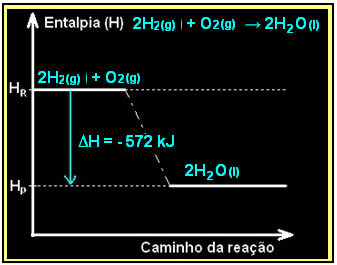
Die Verbrennung von Wasserstoffgas unter Bildung von flüssigem Wasser erfolgt unter Energiefreisetzung. Der Wert der Enthalpieänderung des Systems bei dieser Reaktion ist gegeben durch:
2h2(g) + Aus2(g) → 2H2Ö(1)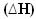 = - 572 kJ
= - 572 kJ
Ihr Diagramm würde wie folgt dargestellt:
Von Jennifer Fogaça
Abschluss in Chemie
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Variation der Enthalpie in exothermen Reaktionen"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/variacao-entalpia-reacoes-exotermicas.htm. Zugriff am 28. Juni 2021.
Chemie

Thermochemie, Enthalpie, freigesetzte Wärme, exotherme Reaktion, Verbrennungsreaktion, äußere Umgebung, endotherme Reaktion, Reaktion Chemie, Energieaustausch, Reagenzien, Lichtemission, Lichtabsorption, Wärme, Strom, Komponenten, Aggregatzustand, Produkte.


