En blanding af opløsninger af samme opløste stof uden kemisk reaktion den består i at samle to opløsninger i den samme beholder med for eksempel kaliumchlorid (Kcl). I denne type blanding vil der aldrig være en kemisk reaktion på grund af tilstedeværelsen af lige opløste stoffer, dvs. begge har den samme kation og den samme anion. Således kan vi sige, at når vi udfører en blanding med disse egenskaber, tilføjer vi bare de mængder opløst stof og opløsningsmiddel, der udgør begge opløsninger.
Hvis vi for eksempel blander en opløsning af 1 liter vand og 4 gram KI (kaliumiodid) med en anden opløsning af 2 liter vand og 6 gram KI, har vi en ny opløsning af 3 liter vand og 10 gram KI .
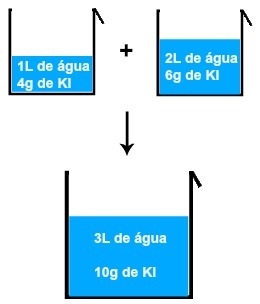
Resultat af blanding af to kaliumiodidopløsninger
Når vi analyserer billedet, kan vi konkludere det massen af det opløste stof (m1') af den første opløsning tilsættes til massen af det opløste stof (m1'') af den anden løsning, hvilket resulterer i massen af det opløste stof (mF) i den endelige løsning (Blande):
m1'+ m1'' = mF
I eksemplet:
4 + 6 = 10 gram
Det samme sker med det volumen vand, der er til stede i hver opløsning, dvs. volumenet af den første (V ') tilsat til volumenet af den anden (V' ') resulterer i det endelige volumen (V'F):
V '+ V' '= VF
I eksemplet:
1 + 2 = 3 l
Da hver opløsning har en mængde opløst opløst stof, og her har vi en blanding af opløsninger af samme opløste stof, fra ovenstående kan vi derefter bestemme koncentrationen (fælles, molaritet) for hver af de blandede opløsninger og også for den endelige opløsning.
Derfor skal vi huske formlerne for at beregne disse koncentrationer:
Almindelig koncentration:
C = m1
V
m1 = opløsning af opløst opløsning
V = opløsningsvolumen
BEMÆRK: isolering af m1 i formlen har vi: m1 = CV
Molarity:
M = m1
M1.V
M1 = molær masse af det opløste stof.
BEMÆRK: isolering af m1 i formlen har vi: m1 = M.M1.V
Da blandingen af opløsninger af samme opløselige adresserer summen af massen af opløsningen af opløsningen, kan vi erstatte hver af observationerne i følgende udtryk:
m1'+ m1'' = mF
C'.V '+ C' '. V' '= CF.VF
Stop ikke nu... Der er mere efter reklamen;)
C '= fælles koncentration af opløsning 1
C '' = fælles koncentration af opløsning 2
Hvis beregningen af blandingen af opløsninger involverer molaritet:
m1'+ m1'' = mF
M'.V '+ M' '. V' '= MF.VF
BEMÆRK: Da den opløste stof er den samme, er den molære masse den samme i hver af opløsningerne; derfor forsømmes det i beregningen.
se nu eksempler, der dækker beregninger i en blanding af opløsninger af samme opløste stof uden kemisk reaktion:
Eksempel 1: (Mackenzie-SP-Adaptada) Tilsætning af 600 ml af en 14 g / L KOH-opløsning til et bestemt volumen (v) af 84 g / L opløsning af den samme base opnås en 67,2 g / L-opløsning. Det tilsatte volumen (v) af 84 g / L-opløsningen er:
a) 0100 ml
b) 3000 ml
c) 2700 ml
d) 1500 ml
e) 1900 ml
Dataene fra øvelsen var:
V '= 600 ml
C '= 14 g / l
V '' =?
C '' = 84 g / l
VF = ?
CF = 67,2 g / l
Før vi bestemmer det tilsatte volumen af opløsning 1, skal vi først bestemme det endelige volumen ved hjælp af følgende udtryk:
V '+ V' '= VF
600 + V '' = VF
Ved at erstatte værdierne i det matematiske udtryk nedenfor har vi:
C'.V '+ C' '. V' '= CF.VF
14. 600 + 84.V '' = 67,2. (600 + V '')
8400 + 84.V '' = 67,2. 600 + 67,2.V ''
8400 + 84.V '' = 40320 + 67.2.V ''
84.V '' - 67.2.V '' = 40320 - 8400
16.8.V '' = 31920
V '' = 31920
16,8
V '' = 1900 ml
Eksempel 2: (UFOP) I en 1000 ml målekolbe blev 250 ml af en 2M svovlsyreopløsning tilsat 300 ml af en 1M opløsning af den samme syre, og volumenet blev fyldt op til 1000 ml med destilleret vand. Bestem molariteten af den resulterende opløsning.
Dataene fra øvelsen var:
V '= 250 ml
M '= 2 M
V '' = 300 ml
M '' = 1 M
VF = 1000 ml
MF = ?
For at bestemme molariteten af den endelige løsning skal du bare bruge det matematiske udtryk, der repræsenterer processen:
M'.V '+ M' '. V' '= MF.VF
2. 250 + 1. 300 = MF.1000
500 + 300 = MF. 1000
800 = MF
1000
MF = 0,8 mol / l
Af mig Diogo Lopes Dias
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
DAGE, Diogo Lopes. "Blanding af opløsninger af samme opløste stof uden kemisk reaktion"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/mistura-solucoes-mesmo-soluto-sem-reacao-quimica.htm. Adgang til 27. juni 2021.

