entalpi er mængden af energi i en given reaktion, variationen af Enthalpy refererer til oprindelsen af denne energi. For eksempel, hvis energien kommer fra en fusionsreaktion (passage af et stof fra fast tilstand til væsken), har vi fusionsentalpien. Der er flere typer entalpier, se nedenfor:
Dannelse entalpi: er entalpi-variationen verificeret i dannelsen af 1 mol molekyler af et givet stof i standardtilstand (under omgivelsesbetingelser (25 ° C og 1 atm) og i en mere stabil allotrop tilstand). Lad os betragte vand som dette stof:
H2 (g) + ½ O2 (g) → 1 H2O (l) ∆Hf = -68,3 Kcal / mol
Vandhalens entalpi (H2O) er -68,3 Kcal / mol, denne værdi svarer til opnåelse af 1 mol H2O (l) gennem elementer i standardtilstand.
Neutraliserings entalpi: værdi som følge af varmen absorberet i neutraliseringen af 1 mol OH- (aq) med 1 mol H + (aq), idet de er i fortyndede vandige opløsninger.
H+ (aq) + OH- (aq) → H2(1) ∆H = -13,8 Kcal / mol
opløsning entalpi: er varmen, der findes i opløsningen af 1 mol opløst stof i opløsningsmiddel, i tilstrækkelig mængde til at opnå en fortyndet opløsning.
HCI (g) + H2O (1) → H30+(aq) + Cl- (aq) ∆H = -18,0 Kcal / mol
Ligningen ovenfor repræsenterer entalpi af opløsning af saltholdig gas.
Stop ikke nu... Der er mere efter reklamen;)
Forbrændingshalppi: er den varme, der absorberes i den samlede forbrænding af 1 mol af stoffet under omgivende forhold (25 ° C og 1 atm). Forbrænding frigiver varme, den finder sted mellem et brændstof og en oxidator, brændstoffet kan være et hvilket som helst stof, den vigtigste oxidator er ilt.
1 CH4(g) + 202(g) → CO2(g) + 2 H2O (1) ∆H = - 212,8 Kcal / mol
Værdien - 212,8 Kcal / mol refererer til forbrændingen af 1 mol CH-methan4(g) ved omgivelsesbetingelser på 25 ° C og et tryk på 1 atm.
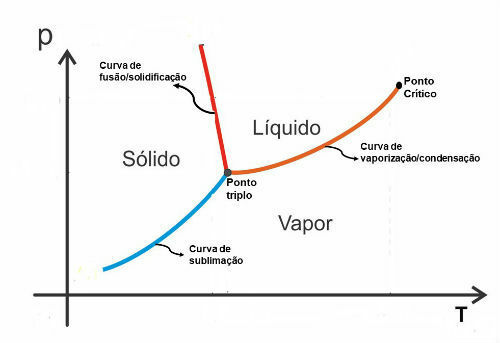
Enthalpi af størkning: svarer til entalpiændringen i den totale størkning af 1 mol af stoffet ved et tryk på 1 atm.
H2O (1) → H2O (s) AH = - 1,7 Kcal / mol
Enthalpi af kondens: henviser til entalpi-variationen i den samlede kondensation af 1 mol af stoffet ved et tryk på 1 atm.
H2O (v) → H2O (l) AH = - 10,5 Kcal / mol
Fusions entalpi: ændring af entalpi i den samlede fusion af 1 mol af stoffet ved et tryk på 1 atm.
H2O (s) → H2O (l) AH = + 1,7 Kcal / mol
fordampning entalpi: svarer til entalpiændringen i den samlede fordampning af 1 mol af stoffet ved et tryk på 1 atm.
H2O (1) → H2O (v) AH = + 10,5 Kcal / mol
Af Líria Alves
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
SOUZA, Líria Alves de. "Enthalpy variation i reaktioner"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/variacao-entalpia-nas-reacoes.htm. Adgang til 28. juni 2021.