For at en kemisk reaktion skal forekomme, er det nødvendigt at opfylde fire grundlæggende betingelser, som er:
1. Reagenser skal kontakte;
2. Der skal være kemisk affinitet mellem reagenserne;
3. Kollisioner mellem reagenspartikler skal være effektive;
4. Aktiveringsenergi skal nås.
Se kort hvert enkelt tilfælde:
1.Kontakt mellem reagenser:
Denne tilstand er åbenbar, for selvom reaktanterne har meget affinitet for hinanden, som i tilfældet med syrer og baser, hvis de adskilles, vil reaktionen ikke forekomme. De har brug for at komme i kontakt, så deres partikler kan kollidere, bryde reaktanternes bindinger og danne produkterne.

2.Kemisk affinitet:
Som vi har set, er det nødvendigt at bringe reagenserne i kontakt, men ikke nok. For eksempel, hvis vi sætter natrium i kontakt med vand, vil der opstå en ekstremt voldsom reaktion, men hvis vi lægger guld, ser vi ingen forskel. Dette skyldes, at forskellige stoffer har forskellige kemiske affiniteter med hinanden, eller måske har de slet ingen affinitet. Jo større den kemiske affinitet, jo hurtigere er reaktionen.
I de nævnte eksempler har natrium en stor affinitet med vand, så meget at for ikke at komme i kontakt med fugtigheden i luften lagres metallisk natrium i petroleum. Guld er inaktivt, hvorfor guldmonumenter holder så længe som Egyptens sarkofager.

3.Kollisionsteori:
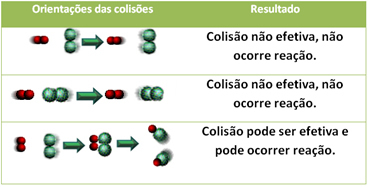
Selv i forbindelser, der har kemisk affinitet, for at reaktionen kan finde sted, er det nødvendigt, at deres partikler, atomer eller molekyler kolliderer effektivt. Ikke alle partikler, der kolliderer, gør dette effektivt, men stød, der resulterer i at bryde reagensbindinger og dannelse af nye bindinger er de, der forekommer i den rigtige retning og med energien nok.
Nedenfor er tilfældet med to ineffektive kollisioner og en effektiv kollision, der resulterer i reaktionen.
4.Aktiveringsenergi og aktiveret kompleks:
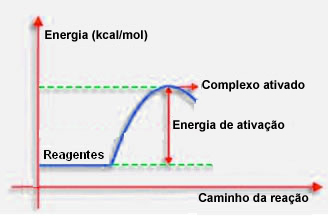
Som anført i det foregående punkt, kræver effektiv kollision ud over gunstig vejledning også tilstrækkelig energi. Den mindste energimængde, der er nødvendig for at hver reaktion skal finde sted, kaldes aktiveringsenergien.
Hvis reaktanterne har en energi lig med eller større end aktiveringsenergien under det velorienterede chok, der dannes et oprindeligt aktiveret kompleks, som er en mellemstruktur mellem reaktanterne og Produkter. I det aktiverede kompleks er der svækkede reagensbindinger og nye produktbindinger dannet.
Således fungerer aktiveringsenergien som en slags barriere for reaktionen, fordi jo større den er, jo sværere bliver det for reaktionen at forekomme. I nogle tilfælde er det nødvendigt at levere energi til reagenserne. For eksempel har kogegas en affinitet til at interagere med ilt i luften, men vi er nødt til at levere energi, når vi bringer kampen sammen, ellers finder reaktionen ikke sted. Men når den er startet, frigiver selve reaktionen nok energi til at aktivere de andre molekyler og holde reaktionen i gang.
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/condicoes-para-ocorrencia-reacoes-quimicas.htm


