En energisk oxidationsreaktion i alkener opstår, når der er et brud på molekylet, dvs. samtidig brydning af de to dobbeltbindinger og iltindløb i det organiske molekyle.
Det er muligt at udføre denne type reaktion med alkener, når der anvendes kaliumpermanganat (KMnO4) eller kaliumdichromat (K2Cr2O7koncentreret i et surt medium, mens det er varmt.
I det sure medium er der H-ioner3O+ forårsager KMnO at nedbrydes4 og frigive 5 atomer af spirende ilt [O] for hver 2 KMnO4. Bemærk denne nedbrydning nedenfor:

Denne reaktion kaldes "energisk", fordi den bryder de to dobbeltbindinger (i mild oxidation er kun bindingen brudt pi), en anden faktor er, at denne reduktion af mangan i et surt medium er meget mere intens end i et basisk medium, som det gøres i mild oxidation.
Det frigivne ilt, der frigøres, reagerer derefter med en alken, men det endelige produkt afhænger af, hvad typer kulstof, der laver dobbeltbinding, dvs. hvis de er primære, sekundære eller tertiære. Se hvad der sker i hvert enkelt tilfælde:
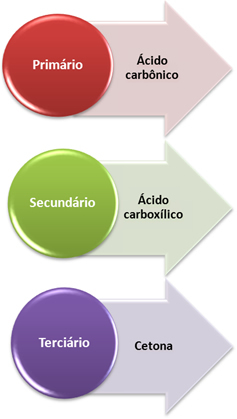
- Primært kulstof: Hvis umættelsen er mellem to primære carbonatomer, vil de dannede produkter være to kulsyre (H2CO3). Hvis kun et af kulstofferne i dobbeltbindingen er primært, er kun en af de dannede molekyler kulsyre. Denne forbindelse er imidlertid ustabil og er aldrig blevet isoleret, den bryder ned i vand og kuldioxid.
- Sekundært kulstof: Hvis umættelsen er mellem to sekundære carbonatomer, vil de to dannede produkter være carboxylsyrer. Hvis kun et af kulstofferne er sekundært, vil det give anledning til et carboxylsyremolekyle, mens det andet afhænger af det andet kulstof.
- Tertiært kulstof: Giver stiger til keton.
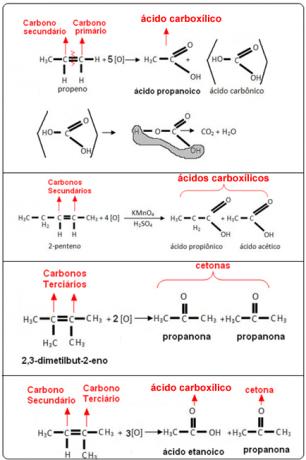
Se eksemplerne nedenfor:
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcenos.htm
