Aminer er organiske forbindelser, der er resultatet af erstatning af et eller flere hydrogener fra ammoniak (NH3) af organiske grupper. Ved at symbolisere disse radikaler med R har vi, at deres funktionelle gruppe kan identificeres på de tre måder nedenfor:
R ─ NH2 eller R ─ NH ─ R ’ eller R─N─R ’
│
R "
Forbindelserne, der hører til denne organiske funktion, er meget vigtige i vores daglige liv og i vores egen organisme, udføre meget vigtige biologiske funktioner, da de vises i aminosyrer, der danner de grundlæggende proteiner til levende væsner.
Industrielt anvendes de også i vid udstrækning, som ved vulkanisering af gummi, til produktion af sæber, medicin og i utallige organiske synteser. Mange bruges desværre som stoffer.
Som sådan er mange aminer ofte kendt under almindelige navne. Se nogle eksempler:
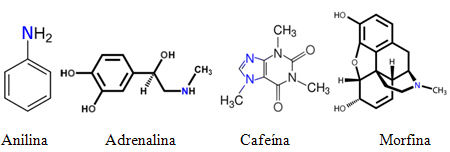
Det er imidlertid ikke muligt for alle kendte aminer at blive kaldt bare ved almindelige navne svarende til de nævnte. Navngivningsregler er nødvendige, så alle i verden kan udføre eksperimenter med det samme stof, at dets struktur let kan identificeres gennem dets navn og omvendt.
Således fastslog IUPAC, at nomenklaturen for aminer skal overholde følgende regel:
Denne regel gælder kun for primære aminer, det vil sige, hvor kun ét ammoniakhydrogenatom er blevet erstattet af en gruppe, der har følgende funktionelle gruppe: R - NH2.
Eksempler:
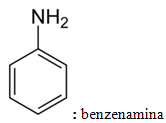
H3C NH2: methanamin
H3C CH2 NH2: ethanamin
H3C CH2 CH2 CH2 NH2: butan-1-amin
Når der er grene eller umættetheder i kæden, er det nødvendigt at nummerere kæden startende fra den nærmeste ende af NH-gruppen2 og vis i hvilket kulstof det forekommer:
NH2
│
H3C - CH - CH2 CH2 CH2 CH3: hexan-2-amin
NH2
│
H3C CH2 CH2 ─ C ═ CH ─ CH3: hex-2-en-3-amin
CH3 NH2
│ │
H3C CH CH ─ CH2 CH3: 2-methyl-pentan-3-amin
CH3 NH2
│ │
H3C - CH - CH2 ─ CH─CH3: 4-methyl-pentan-2-amin
I tilfælde af sekundære og tertiære aminer (som har henholdsvis to og tre hydrogener af den substituerede ammoniakgruppe), er reglen forskellig:

Navnet på disse aminer er forud for bogstavet N for at indikere, at substituenten er bundet til et nitrogenatom, og substituenterne i carbonkæden er normalt angivet med tal.
Eksempler:
H3C CH2 CH2 ─ NH ─ CH2: N-methyl-propanamin
CH3 CH3
│ │
H3C - CH - CH2 - NEJ - CH2 CH3: N-ethyl-2, N-dimethyl-propanamin
H3C─N─CH2 CH3: N-dimethyl-ethanamin
│
CH3
H3C─N─CH2 CH3: N-methyl-ethan-1-amin
│
H
Der er to typer sædvanlige nomenklatur for aminer. Den første følger følgende ordning:

Eksempler:
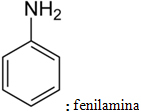
H3C NH2: methylamin
H3C CH2 NH2: ethylamin
H3C CH2 CH2 CH2 NH2: butylamin
H3C─N─CH2 CH3: ethyl-dimethylamin
│
CH3
H3C─N─CH2 CH3: ethylmethylamin
│
H
H3C─N─CH3: trimethylamin
│
CH3
Trimethylamin er hovedkomponenten i den dårlige lugt fra rådne fisk.
Den anden sædvanlige nomenklatur overvej NH-gruppen2 som en gren af carbonkæden og er angivet med præfikset “amino”. Den længste kæde er den vigtigste, og resten er grenen. Se eksemplerne:
CH3 CH3
│ │
H3Ç1 ─C2 ─C3H ─C4H2 ─C5H3: 2-amino-2,3-dimethyl-pentan
│
NH2
CH2 CH2 CH2 CH2 : 1,4-diamino-butan
│ │
NH2 NH2
CH2 CH2 CH2 CH2 CH2 : 1,5-diaminopentan
│ │
NH2 NH2
Disse sidste to forbindelser er kendt i henholdsvis hverdagen som putrescin og kadaverin, aminer, der dannes i nedbrydningen af menneskelige lig.
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/nomenclatura-das-aminas.htm
