Der er tre typer alkadiene eller diener, som er:
1-akkumuleret: Dobbeltbindingerne er placeret på samme kulstof og vises successivt:
─C ═ Ç ═ C ─
│ │
2- Isoleret: Dobbeltbindingerne er på forskellige kulstoffer og adskilles af mindst to på hinanden følgende enkeltbindinger:
│
─C ═ C C - C ═ C ─
│ │ │ │ │
3- Konjugater: Dobbeltbindinger vises skiftevis og adskilles af en enkelt enkeltbinding:
─C ═ C C ═ C ─
│ │ │ │
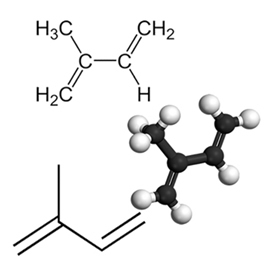
Et eksempel på en vigtig konjugeret dien er isopren, som er en basisk enhed af terpengruppen, en klasse af organiske forbindelser. meget vigtigt, nogle eksempler på produkter dannet af isoprener er gummi, beta-caroten (ansvarlig for den orange farve på gulerødder), vitamin A og olier, der findes i frugtskaller, frø, blomster, blade, rødder, grøntsager og træ, såsom limonen og myrcene.
Til akkumulerede og isolerede diener, tilføjelsesreaktioner forekommer ligesom i tilfælde af alkener, hvad du kan forstå ved at læse teksten Tilføjelsesreaktioner. Den eneste forskel er, at diener gennemgår denne type dobbeltreaktion, fordi de har to dobbeltbindinger, mens alkener kun har en dobbeltbinding.
I tilfælde af konjugerede diener, additionsreaktionen har en særlig egenskab, da disse forbindelser kan gennemgå resonans, så tilsætningen kan finde sted på to måder:
1- Tilføjelse 1.2:
Dette betragtes som normal tilsætning, da tilsætningen sker på de to carbonatomer, der danner den samme dobbeltbinding, det vil sige på kulstof 1 og 2:
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH─ CH ═ CH2
│ │
HBr
Se, at denne type reaktion følger Markovnikovs styrebringer hydrogenet sig til det mere hydrogenerede carbon (med flere hydrogenatomer bundet).
Tilsætning 1,2 behandles ved lave temperaturer (-60 ° C).
2- Tilføjelse 1.4:
I dette tilfælde fortsætter reaktionen ved høje temperaturer. Det er vigtigt at understrege, at både produktet af tilsætning 1.2 og tilsætning af 1.4 altid dannes, men temperaturen indikerer, hvilken der vil blive dannet i større mængde.
Følgende er et eksempel på tilføjelse af type 1.4:
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH ═ CH─CH2
│ │
HBr
Bemærk, at følgende forekommer, en af de delte elektroner i pi-bindingen af hver af de dobbelte carbonatomer deles med substituenten, og de andre danner en ny dobbeltbinding mellem andre carbonatomer:
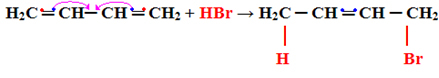
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/reacoes-adicao-dienos.htm
