Amerikansk kemiker Gilbert N. Lewis (1875-1946) foreslog oktetreglen, der siger:
"Atomer med forskellige grundstoffer etablerer kemiske bindinger, donerer, modtager eller deler elektroner for at erhverve den elektroniske konfiguration af ædelgas, det vil sige med 8 elektroner i den sidste skal (eller med 2 elektroner i tilfælde af de atomer, der kun har en elektronskal, som det sker med hydrogen). "
I 1916 foreslog Lewis, at for at forblive stabil og nå oktetten eller duetten, de elementer, der udgør molekylære stoffer udføre deling af elektronpar. Disse stoffer dannes kun af atomer af brint, ikke-metaller og halvmetaller, alt sammen med tendens til at modtage elektroner. Derfor er der ingen måde for nogen af dem at donere nogen elektron (som det forekommer med metaller i ionbindinger), men alle har brug for at modtage, så de deler deres elektroner gennem en kovalent binding eller molekylær.
Således foreslog Gilbert Lewis en måde at repræsentere den kovalente eller molekylære binding, som blev kendt som
Lewis formel. Hun kaldes også elektronisk formel eller endnu, Lewis 'elektroniske formel, fordi dens vigtigste funktion er, at det viser elektronerne i hvert atoms valensskal og dannelsen af elektroniske par.Hver elektron er repræsenteret af en prik., som omgiver symbolet for det tilsvarende kemiske element. Kun valensskalelektronerne er omkring elementet.
Som vist i tabellen nedenfor, skal du bare kende den periodiske systemfamilie for at kende mængden af elektroner i valensskallen:

I Lewis-formlen hvert fælles elektronpar repræsenterer en kemisk (kovalent) binding, hvor elektroner mødes i det område af elektrosfæren, der er fælles for hvert par atomer, der er forbundet sammen. Derfor er de i repræsentationen placeret side om side.
Lad os for eksempel finde ud af, hvad Lewis-formlen er for hydrogengas, hvis molekylformel er: H2.
Hvert brintatom har kun en elektron i valensskallen, da dette element hører til familie 1 i det periodiske system. Hver skal modtage endnu en elektron for at være stabil med to elektroner i K-elektronskallen. Så de deler deres elektroner, og begge får to. Se:
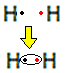
Dette er Lewis-formlen for hydrogengasmolekylet.
Oxygen har seks elektroner i sin elektronskal, så hver har brug for at modtage yderligere to elektroner for at være stabile med otte elektroner. Derfor er Lewis-formlen for iltgasmolekylet:

Bemærk, at der er to links, da der er to delte par.
Se andre eksempler på elektroniske formler af molekylære stoffer nedenfor:
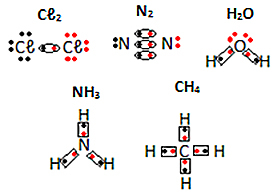
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/formula-eletronica-lewis.htm

