DET optisk isomerisme er en slags rumisomerisme, eller stereoisomerisme, der studerer stoffers opførsel, når de udsættes for en stråle af polariseret lys. For bedre at forstå, skal du læse teksten "Polariseret lys”.
Som i alle former for isomerisme, optiske isomerer har den samme molekylformel, men er differentieret ved deres optiske aktivitet.
Overvej f.eks. Mælkesyremolekylet vist nedenfor. Da det ikke er symmetrisk, kan det give anledning til to typer mælkesyrer:
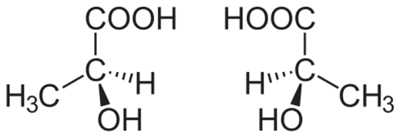
Når vi sender disse to molekyler til en polariseret lysstråle, bemærker vi, at en af dem afbøjer den polariserede lysstråle til højre, kaldet højrehåndet (syre d-laktisk); og den anden afviger til venstre, kaldet levogyro (syre ℓ-laktisk). Dextrorotatorisk mælkesyre opnås ved indvirkning af bakterier i kødekstrakten, og levorotær mælkesyre fra fermenteringen af saccharose ved hjælp af Bacillus acidi levolactiti.
Så disse to forbindelser er optiske isomerer.
En måde at kontrollere, om et molekyle af en bestemt forbindelse udfører optisk aktivitet, er at se, om molekylet har nogen
asymmetrisk kulstof (C *), dvs. det har 4 forskellige ligander.Bemærk, at dette sker i strukturen af mælkesyre, og denne type kulstof kaldes chiral, der stammer fra et græsk ord, der betyder "hånd". Så som vores hånd er optiske stereoisomerer spejlbilledet af hinanden og kaldes på grund af dette enantiomerer.
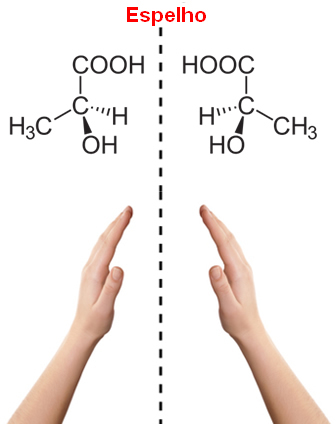
Derudover skal det også bemærkes, at strukturerne af deres molekyler ikke overlapper hinanden, fordi strukturen af et givet molekyle og dets billede overlapper uden forandring, så de er det samme molekyle og ikke optiske isomerer.
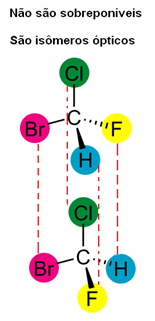
Imidlertid er det kun ved hjælp af et polarimeter, at det er muligt med sikkerhed at vide, om en optisk isomer er højrehåndet eller venstrehåndet.
Disse to forbindelser har, til trods for at de er kemisk og fysisk ens, helt forskellige egenskaber. En blanding af dem er optisk inaktiv, det vil sige, den afviger ikke fra det polariserede lysplan og kaldes racemisk blanding.
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/isomeria-Optica.htm
