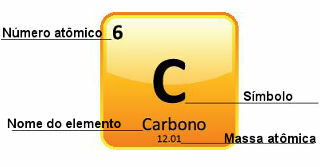
DET sp-type kulstofhybridisering det sker kun, når det danner to pi-bindinger (π) og to sigma-bindinger (σ). I dette tilfælde er der så to muligheder: kulstof kan danne to dobbeltbindinger eller en enkelt og en tredobbelt binding som vist nedenfor:
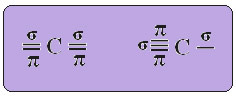
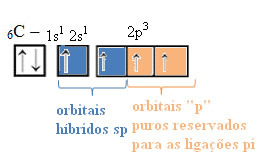
Teksten "sp-type hybridisering3”Viser detaljeret, hvordan kulstofhybridisering finder sted. Husk: hybridisering er "blanding" af rene atomorbitaler, der stammer fra hybridatomorbitaler svarende til hinanden, men forskellig fra de oprindelige rene orbitaler. Så dette sker i kulstoforbitaler, der oprindeligt var repræsenteret sådan:
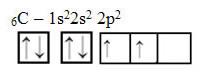
Men med modtagelse af energi fremmes en elektron (repræsenteret af en pil) fra 2s-orbitalen til 2p-orbitalen:
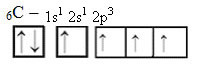
På denne måde har kulstoffet fire ikke-parrede orbitaler, der er i stand til at danne fire kovalente bindinger, ikke kun to.
I tilfælde af hybridisering af sp-typen ved vi, at to obligationer vil være pi; disse forekommer i de rene ”p” orbitaler, mens de to andre orbitaler, som er sp hybrider, vil danne de resterende sigma-bindinger.
Den rumlige repræsentation af denne hybridisering mellem en s og en p orbital, der giver anledning til en hybrid sp orbital, kan repræsenteres som følger:
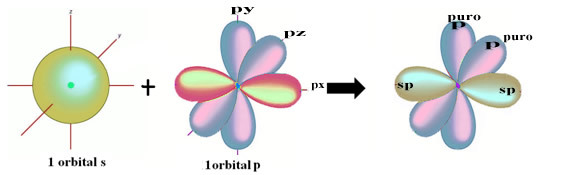
I figuren ovenfor er det meget klart, at der er to rene orbitaler, der vil gøre pi-bindingerne.
For at du kan forstå, hvordan dette sker, lad os tage et eksempel på et molekyle cyanidgas (HCN), der bruges i USA i gaskamre til fanger, der er idømt dødsstraf. Dens strukturformel er givet ved:
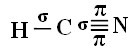
Med hensyn til kulstof er dets atomorbitaler allerede blevet vist, se nu på hydrogen- og nitrogenorbitalerne:
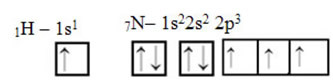
Bemærk, at den uparrede hydrogenbane, der udfører sigma-bindingen, er "s", som er rumligt repræsenteret af en cirkel; og nitrogenorbitaler er af "p" -typen, repræsenteret af tre dobbelte æggestokke (hver i et rumligt felt: x, y, z). Således er strukturen af HCN-molekylet repræsenteret som følger:
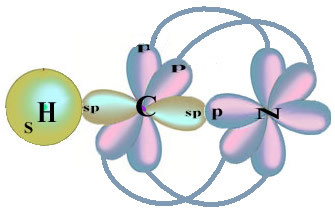
Hvad angår typen af obligationer, der findes i denne formaldehydstruktur, har vi:
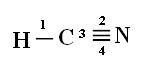
Forbindelser: 1 = σs-sp
2 = σp-sp
3 = 4 = πp-p
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm