Du estere er iltede organiske forbindelser, der dannes ved den kemiske reaktion mellem a carboxylsyre det er en alkohol. Præsenter den funktionelle gruppe (sammensat af to iltatomer og to radikaler R) repræsenteret nedenfor:
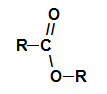
Generel funktionel gruppe af en ester
Strukturelt, hvad der karakteriserer ester det er tilstedeværelsen af en eller anden alkylradikal bundet direkte til oxygenatomet. I dette tilfælde kan gruppen (R), der er bundet til kulstof - som igen er dobbeltbundet til ilt - være enten en alkylgruppe eller et hydrogenatom.
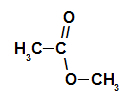
Kulstofkæde af en ester
forestringsreaktion
det handler om kemisk reaktion, der stammer fra en ester og et vandmolekyle fra interaktionen mellem en carboxylsyre og enhver alkohol, som i ligningen nedenfor:
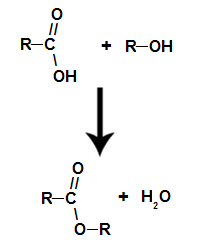
Kemisk ligning, der repræsenterer dannelsen af en ester
Under forestring interagerer alkoholens hydroxylgruppe (OH) med hydrogen (H) ioniserbar ud fra hydroxyl af syren og danner vandmolekyle.
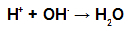
Vandmolekyledannende grupper i forestring
allerede den ester den dannes ved at forbinde alkoholen (R) med alkoholen, som er tilbage fra syrehydroxylen efter dannelsen af vand.
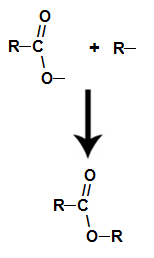
Dannelse af estermolekylet
Kendetegn ved estere
Vigtigste fysiske egenskaber præsenteret af estere:
De har frugt- og blomsteraromaer;
lave estere Molar masse de er flydende ved stuetemperatur, og de med en høj molær masse er faste;
Sammenlignet med alkoholer og carboxylsyrer har estere lavere smelte- og kogepunkter;
Sammenlignet med vand er estere med lavere molær masse mindre tætte;
De lavere molære massestere er polære, og de med højere molære masser er ikke-polære;
I polære estere dominerer kræfter permanent dipol; i det ikke-polære dominerer kræfter induceret dipol;
Estere med lavere molær masse er dårligt opløselige i vand, og dem med større masse er uopløselige i vand.
En Ester-navngivningsregel
Før du bruger navngivningsreglen for a ester, er det vigtigt at huske, at denne forbindelse er dannet af foreningen af to dele, den ene kommer fra af carboxylsyre (i rødt) og den anden af alkohol (i blå), som repræsenteret ved billede a følge efter:
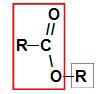
Identifikation af de dele, der stammer fra esteren
Ifølge International Union of Pure and Applied Chemistry (IUPAC), den officielle regel for navngivning af en ester er:
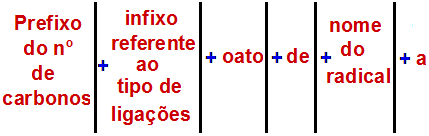
En Ester-navngivningsregel
Bemærk: Præfikset og infikset svarer altid til carboxylsyredelen, og radikalet svarer til alkoholdelen.
Se nedenfor nogle eksempler på anvendelse af navngivningsreglen for estere:
1. eksempel: hindbær essens
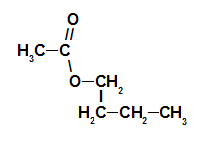
Strukturel formel af hindbær essensester
For at navngive denne ester bruger vi:
Nej. PræfiksO af kulhydrater: et, da den dannende syre har to carbonatomer;
Infix om typen af links: en, da den dannende syre kun har enkeltbindinger mellem carbonatomer;
akten;
i;
Radikal: butylved at have fire carbonatomer i rækkefølge;
Det.
Således er navnet på esteren svarende til hindbæressensen butylethanoat.
2. eksempel: fyrretræs kerne essens
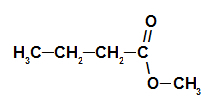
Strukturformel af fyrkegleesteren
For at danne navnet på denne ester bruger vi:
Nej. PræfiksO af kulhydrater: men, da dannelse af syre har fire carbonatomer;
Infix om typen af links: en, da den dannende syre kun har enkeltbindinger mellem carbonatomer;
akten;
i;
Radikal: methyl, da den dannende alkohol kun har et kulstof;
Det.
Således er navnet på esteren, der svarer til fyrretræets essens methylbutanoat.
3. eksempel: jordbær essens
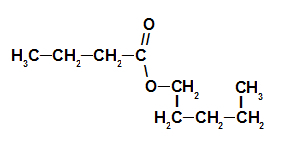
Strawberry Essence Ester Structural Formula
For at navngive denne ester bruger vi:
Nej. PræfiksO af kulhydrater: men, da den dannende syre har fire carbonatomer;
Infix om typen af links: en, da den dannende syre kun har enkeltbindinger mellem carbonatomer;
akten;
i;
Radikal: pentyl, da den dannende alkohol har fem carbonatomer i rækkefølge;
Det.
Således er navnet på esteren svarende til jordbæressensen pentylbutanoat.
Anvendelse af estere
Estere er velkendte for deres anvendelse som aromastof i forarbejdede fødevarer, dvs. stoffer, der simulerer den karakteristiske smag og aroma af naturlige fødevarer, såsom frugt. Desuden, estrene bruges stadig til fremstilling af medicin, kosmetik, parfume og voks.
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm
