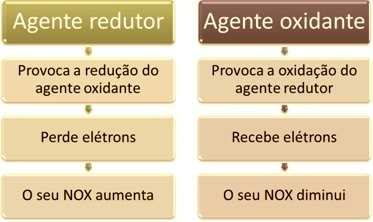
Et af de vigtigste træk, der skelner mellem en oxidationsreduktionsreaktion (eller redox) af de andre er tilstedeværelsen af et oxidationsmiddel og et reduktionsmiddel, som kan defineres som følger:
Se for eksempel på den kemiske reaktion nedenfor, hvor aluminium (Al) korroderer i vandig saltsyreopløsning (HCI). Aluminiumatomer overfører elektroner til H-kationer+(her) og producere Al-kationen3+(her):
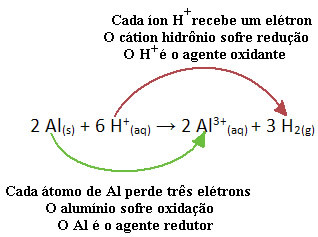
Bemærk, at da Al overførte elektroner, betyder det, at han forårsagede reduktionen af H-kationerne+(her); det er derfor, han kaldes reduktionsmiddel. Allerede kationen H+(her) fjernede elektronerne fra aluminiumet, forårsager oxidation af det metal; derfor fungerer han som en oxidationsmiddel.
I hverdagen er der mange eksempler på ydeevnen af oxidationsmidler og reduktionsmidler. Se på nogle af dem og husk dog, at reduktionen i alle tilfælde sker samtidig med oxidationen; derfor, hvis der er et reduktionsmiddel, er der også et oxidationsmiddel.
- Eksempler på reduktionsmidler:
- I fotografiske film: fotografiske film indeholder lysfølsomme sølvsalte. På punkter, hvor der er forekomst af lys, er der en reduktion af Ag-ioner+, hvilket resulterer i kontrasten observeret i negativerne.

- C-vitamin: C-vitamin (L-ascorbinsyre) er et stærkt reduktionsmiddel i vandig opløsning. Det har en enestående facilitet, der skal oxideres, og det er derfor, det er meget brugt, især i fødevarer som f.eks antioxidant, dvs. det tilsættes til andre fødevarer og beskytter dem mod mulig oxidation på grund af dets egne ofre. Et eksempel er frugter som æbler og pærer, der mørkner i kontakt med ilt i luften, fordi de oxiderer. Men når du tilføjer en lille mængde appelsin- eller citronsaft (som indeholder C-vitamin) til frugten skåret forhindrer dette, at denne reaktion opstår, fordi C-vitamin fungerer som et reduktionsmiddel og oxiderer før frugten.

- Brintgas: brintgassen (H2) anvendes i raketfremdrift og betragtes som et af de vigtigste energialternativer, da dets forbrænding frigiver en stor mængde energi og ingen forurenende stoffer. I denne reaktion fungerer brint som et reduktionsmiddel, der oxideres af ilt.
- Eksempler på oxidationsmidler:
- Ved produktion af eddike: når vin udsættes for luft, bliver den til eddike, hvis hovedbestanddel er eddikesyre. Dette skyldes, at den ethylalkohol eller ethanol, der findes i vin, oxiderer ved kontakt med atmosfærisk ilt, hvilket resulterer i eddikesyre. Således er ilt et oxidationsmiddel. Selv oprindelsen af udtrykket "oxidation" er relateret til reaktionen med ilt.

- I rusten: som anført i det foregående eksempel fungerer ilt som et oxidationsmiddel for alkohol; og det gør det også i kontakt med forskellige metaller, såsom jern, der forårsager rustprocessen. Ud over ilt i luften er andre oxidationsmidler i dette tilfælde vand eller en sur opløsning.
- I blegemidler: blegemidlets blegningseffekt skyldes tilstedeværelsen af følgende to reduktionsmidler: o hypochloritanion (generelt i form af natriumsalt - NaOCl), fx til stede i blegemiddel; og hydrogenperoxid (H2O2), markedsført som hydrogenperoxid. Disse to forbindelser har en meget stærk tendens til at oxidere og forårsage reduktion af andre kemiske arter. Derfor er de ansvarlige for oxiderende stoffer, der giver produkter mørk farve. For eksempel nedbrydes lignin i cellulose og bliver lettere og mere formbart. I tilfælde af pletfjerning og stofblegning forårsager disse oxidationsmidler oxidation af organiske molekyler såsom fedtstoffer og farvestoffer.

- I åndedrætsværn: en simpel engangs åndedrætsværn består af et klart rør indeholdende en vandig opløsning af dichromatsaltet af kalium og silica, fugtet med svovlsyre; blandet med orange farve. Dette salt, i kontakt med den alkoholdamp, der er inde i den berusede førers ånde, reagerer og ændrer farven til grøn. Dette betyder, at oxidation af ethanol (alkohol) til ethanal er forårsaget.

Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm


