Til nitrogen funktioner er en gruppe af organiske forbindelser der har atomer af nitrogen knyttet til kulstofkæden. De er kendetegnet ved deres respektive funktionelle grupper, som er sæt af atomer forbundet i en bestemt konfiguration, og som definerer de karakteristiske egenskaber for hver funktion.
Nitrogenfunktionerne er:
aminer;
amider;
nitroforbindelser;
nitriler;
isonitriler.
Læs også:Hvad er iltfunktionerne?
Sammenfatning af nitrogenfunktioner
Nitrogenfunktioner er organiske forbindelser, der indeholder atomer af nitrogen.
Aminer, amider, nitroforbindelser, nitriler og isonitriler er nitrogenfunktionerne.
Uorganiske funktioner er kendetegnet ved deres funktionelle gruppe.
Aminer er afledt af substitution af hydrogener af ammoniak ved alkylradikaler.
Amider har det samme kulstofatom forbundet med nitrogen og kulstof. ilt.
Nitroforbindelser indeholder -NO-gruppen.2.
Nitriler er karakteriseret ved tilstedeværelsen af en tredobbelt binding mellem kulstof og nitrogen.
Isonitriler har en tredobbelt binding mellem nitrogen og kulstofmed nitrogen bundet til kulstofkæden.
Video lektion om nitrogenholdige funktioner
Hvad er nitrogenfunktioner?
Nitrogenfunktioner er et sæt af organiske funktioner, der har nitrogenatomet i deres struktur, foruden kulstof- og brintatomer. De er: aminer, amider, nitroforbindelser, nitriler og isonitriler,
Det, der adskiller de nitrogenholdige funktioner, er de respektive funktionelle grupper, som er det strukturelle arrangement af atomer, der er ansvarlige for stoffets egenskaber.
Hvad er nitrogenfunktionerne?
aminer
Den organiske funktion minen er karakteriseret ved at binde mindst én kulstofkæde til nitrogenatomet. Den funktionelle gruppe af aminer er -N-R1R2R3 (R-grupperne er carbonkæder eller hydrogenatomer, hvoraf mindst én er en carbonkæde).

aminerne er afledt af ammoniak (NH3), med et eller flere hydrogenatomer erstattet af carbonatomer eller alkylligander. De er grundlæggende stoffer, der forlader pH større end 7 i vandig opløsning.
De er klassificeret efter mængden af hydrogenatomer erstattet af carbonligander (alkyl- eller arylgrupper), som kaldes substituenter.
- Primære aminer: har en enkelt carbonsubstituent.
- Sekundære aminer: har to carbonsubstituenter.
- Tertiære aminer: har tre kulstofsubstituenter, det vil sige, at nitrogenatomet ikke længere er bundet til noget brintatom, hvilket etablerer tre Forbindelser simpelt med kulstofatomer.
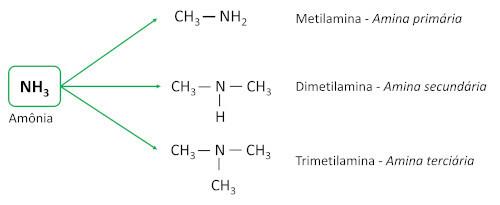
EN nomenklatur for aminer følger retningslinjerne for IUPAC (International Union of Pure and Applied Chemistry). I tilfælde af primære aminer tager konstruktionen af navnet hensyn til antallet af carbonatomer (præfiks), arten af bindingen mellem carboner (infix) og udtrykket bruges minen for suffikset (ordets slutning).

Se eksemplet:
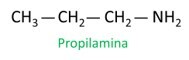
Når du tildeler numre til carbonatomer for placeringen af radikaler, skal du tildele det lavest mulige tal til det atom, der er tættest på NH-gruppen.2.
For sekundære og tertiære aminer betragter nomenklaturen den længste substituentgruppe knyttet til nitrogenet som hovedkæden, og de andre ligander er skrevet med præfikset, der henviser til antallet af carbonatomer og suffikset -il, med bogstavet N foran dem.

Eksempel:
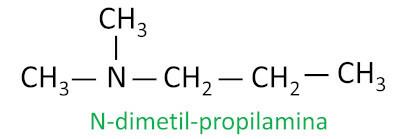
Amider
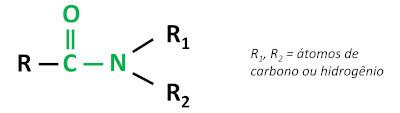
Den organiske funktion amid er præget af binding af en carbonylgruppe (C=O) til nitrogenatomet, hvor nitrogen kan bindes til carbon- eller hydrogenatomer.
Amider er grundstofferEfterlader pH over 7 i vandig opløsning. Stoffet urinstof tilhører gruppen af amider og er en naturligt forekommende forbindelse i urinen, der stammer fra nedbrydningsprocesser, der sker i levende organismer.
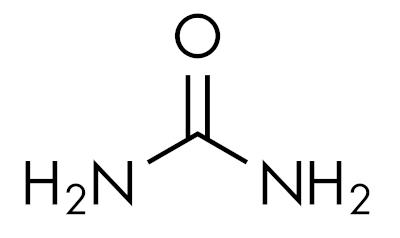
Amider er karakteristiske afhængigt af niveauet af nitrogensubstitution. Sådan her:
- Primære amider: holder to brintatomer sammen med nitrogen.
- Sekundære amidereller monosubstitueret: en af brinterne er blevet erstattet af kulstofkæde, så nitrogen opretholder en enkeltbinding med brint.
- tertiære amidereller fortrængt: Nitrogen har ikke længere hydrogenbindinger, som alle er erstattet af kulstof.

Amider er Navngivet ifølge IUPAC, molekylerne er navngivet af sekvensen:

I forgrenet amid deltager amidgruppens kulstofatom i hovedkæden, og kulstoftallet skal starte med det. Se:
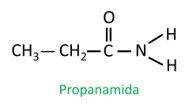 |
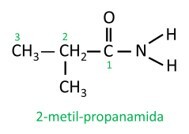 |
I monosubstituerede eller disubstituerede amider er de bogstavet N angiver grenens position som er knyttet til nitrogenatomet. Hvis der er en anden radikal i kæden, vil den blive skrevet efter at have identificeret den radikal, der refererer til N.
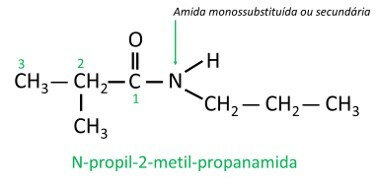
nitroforbindelser
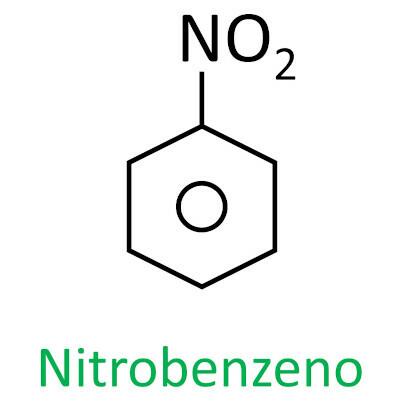
Du nitroforbindelser er organiske forbindelser, der indeholder en nitrogruppe (-NO2) bundet til en kulstofkæde, som kan være alifatisk (åben eller lineær) eller aromatisk.
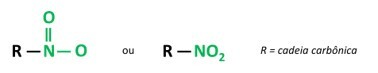
EN hovedkarakteristika ved disse stoffer er deres eksplosive kraft. Den eksplosive kapacitet er forbundet med aromatiske nitroforbindelser, og jo større antal nitrogrupper, jo større er eksplosionen. Alifatiske nitroforbindelser bruges i laboratorier som organiske opløsningsmidler.
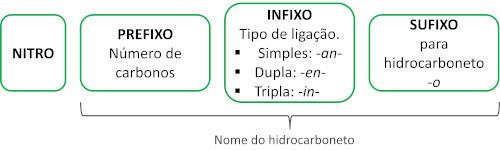
Nomenklaturen for disse forbindelser er dannet af ordet nitro efterfulgt af navnet på kulbrinte (præfiks + infix + slutning -O).
Se nogle eksempler:
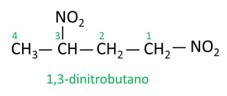 |
 |
nitriler
Nitriler er organiske forbindelser karakteriseret ved tredobbelt binding mellem et carbonatom og et nitrogenatom, der præsenterer den funktionelle gruppe – C ≡ N. I nitriler er nitrogenet i enden, og kulstoffet er bundet direkte til kulstofkæden.

nitrilerne Også kendt som cyanider, da de stammer fra reaktioner med blåsyre (HCN).
de er stoffer giftig for mennesker, fordi de i kroppen kan danne blåsyre i kontakt med mavesyre, hvilket forhindrer processer af cellulær respiration af cellerne.
I naturen kan nitriler findes i nogle stenfrugter, men i en meget lav koncentration, der ikke udgør en risiko, og i bladene af vild kassava.

Iupac-reglen for nomenklaturen af nitriler definerer dette udtryk nitril tilføjes som et suffiks:

Se nogle eksempler:
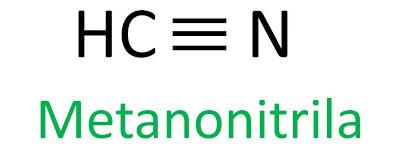 |
 |
Den sædvanlige form for nomenklatur for nitriler er cyanid + radikalt navn.
isonitriler
Isonitriler eller isonitriler er forbindelser dannet af tredobbelt binding mellem et carbonatom og et nitrogenatom, der præsenterer den funktionelle gruppe – R ≡ C. I isonitriler er kulstoffet i enden, og nitrogenet er bundet direkte til kulstofkæden.

Isonitrilerne adskiller sig fra nitrilerne på grund af placeringen af nitrogen- og carbonatomerne, og I isonitriler er nitrogen karakteriseret som et heteroatom., da den er placeret mellem to carbonatomer.
De er ustabile arter og kan omdannes til nitriler ved forhøjede temperaturer. Isocyanidinsyrereaktioner giver anledning til isonitriler, hvorfor disse forbindelser også er kendt som isocyanider.
Isonitrilmolekyler følger Iupac-reglen for navngivning:
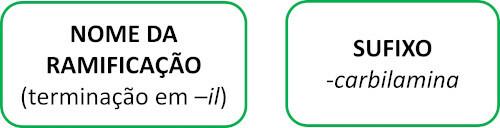
Se nogle eksempler:
 |
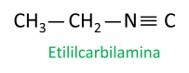 |
Anvendelser af nitrogenfunktioner
De stoffer, der hører til de nitrogenholdige funktioner, har talrige anvendelser, hovedsageligt på industriområdet, til fremstilling af polymerer, gummi, syntetiske fibre, lægemidler, landbrugskemikalier, pesticider og sprængstoffer.
Til aminer bruges til fremstilling af farvestoffer, sæber, stoffer, i gang med gummi vulkanisering, sprængstoffer og andre industrielle processer, og findes også i planter og dannes i organisk stofnedbrydningsprocesser.

Til Amider har bred anvendelse i den industrielle og kemiske sektor, der er til stede i produktionen af polymerer (såsom nylon og polyurethan), harpikser, sprængstoffer, gødning, insektmidler, gødning og lægemidler.

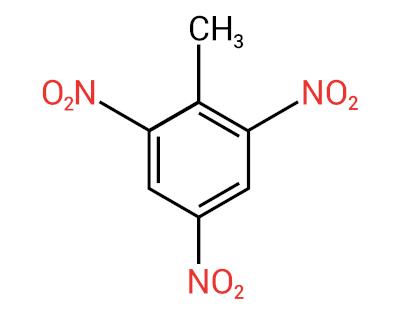
Du nitroforbindelserDens hovedanvendelse er fremstilling af sprængstoffer. der anvendes i den militære, industrielle og metallurgiske sektor (til råvareudvinding). En af de bedst kendte nitroforbindelser er trinitrotoluen, populært kendt som TNT. Andre anvendelser af nitroforbindelser er i produktionen af pesticider, baktericider, farvestoffer, petroleumsraffinering mv.

Til nitriler anvendes som organiske opløsningsmidler i laboratoriet og i industrien, der deltager i udvindings- og fremstillingsprocesserne af nogle syntetiske fibre, plastpolymerer, farvestoffer og gødning.

Til isonitriler anvendes i forskellige processer til fremstilling af organiske forbindelser, såsom opløsningsmidler, og deltager i fremstillingen af landbrugskemikalier, pesticider, gummi og plast.
Læs også:Halogenider - stoffer, der har halogenatomer knyttet til kulstofkæden
Løste øvelser om nitrogenfunktioner
Spørgsmål 1
(FPS-PE-modificeret) Anvendelsen af nitrogenholdige forbindelser i syntetisk organisk kemi er meget diversificeret og involverer fremstilling af lægemidler, farvestoffer, sprængstoffer og vitaminer. Se på forbindelserne nedenfor.
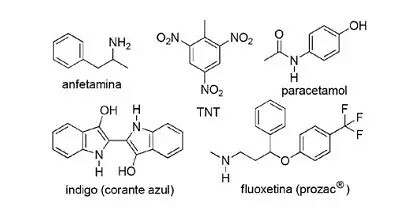
Om disse forbindelser skal du markere den forkerte udsagn.
a) TNT er en nitroforbindelse.
b) Den nitrogenholdige del af fluoxetin er en sekundær amin.
c) Amfetamin er klassificeret som et primært amid.
d) Indigo har heteroaromatiske ringe i sin struktur.
e) Den nitrogenholdige del af paracetamol er et amid.
Løsning:
Bogstav C
Varen Det er korrekt, fordi TNT er en nitroforbindelse, fordi den INGEN grupper har2.
Varen B er korrekt. Den nitrogenholdige del af fluoxetin er en sekundær amin, fordi den er forbundet med to kulstofsegmenter.
Varen w er forkert, da amfetamin er klassificeret som en primær amin, ikke et amid. Bemærk, at den nuværende gruppe er NH2. Så dette er kernen i spørgsmålet.
Varen d er korrekt, da indigo har heteroaromatiske ringe i sin struktur, det vil sige ringe dannet af carbonatomer og et andet grundstof - i dette tilfælde nitrogen.
Varen det er er korrekt, fordi paracetamol er et amid, der præsenterer kulstof knyttet til nitrogen og oxygen.
spørgsmål 2
(UFMS) Yerba mate (Ilex paraguariensis), oprindeligt fra Sydamerika, bruges som en styrkende og stimulerende drik. Produktet opnået ved forarbejdning af yerba mate-blade kan bruges til at forberede chimarrão og tereré, blandt andre drikkevarer, der almindeligvis og kulturelt indtages i regioner i Argentina, Paraguay og Brasilien. Den store interesse for yerba mate skyldes de tilstedeværende kemiske forbindelser på grund af dets antioxidant-, stimulerende og vanddrivende egenskaber.
(Tilgængelig i: http://repositorio.utfpr.edu.br/jspui/bitstream/1/3158/1/PG_PPGEP_Henrique%2C%20 Flavia%20Aparecida_2018.pdf. Tilgået den: 01. nov. 2018. tilpasset).
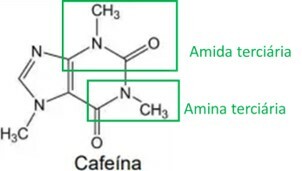
De stimulerende egenskaber af yerba mate er relateret til dets indhold af methylxanthiner, en af de vigtigste er koffein, struktur præsenteret nedenfor:

Når man analyserer koffeins strukturformel, er det korrekt at sige, at det har følgende organiske funktioner og egenskaber:
a) aldehyd og amid, basisk.
b) amin og amid, alkalisk.
c) amin og keton, alkalisk.
d) keton og amid, amfotere.
e) carboxylsyre og amin, basisk.
Løsning:
Bogstav B
Ved at analysere koffeinstrukturen identificeres amin- og amidfunktionelle grupper, som fremhævet på billedet nedenfor. Da disse to grupper har en basisk eller alkalisk karakteristik, har koffein også denne egenskab, hvilket betyder, at vandige koffeinopløsninger har en pH over 7.
Af Ana Luiza Lorenzen Lima
Kemi lærer
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/funcoes-nitrogenadas.htm
