O muscovius, Atom nummer 115, placeret i gruppe 15 i det periodiske system, er et af de sidste elementer, der er inkluderet i det, i 2015, sammen med elementerne 113, 117 og 118. Dens navn er en henvisning til regionen Moskva, russisk hovedstad.
Moscovium blev imidlertid oprindeligt produceret, i 2003, gennem fælles arbejde af russiske og amerikanske videnskabsmænd. Alligevel, næsten 20 år efter dens første syntese, bliver dens grundlæggende egenskaber stadig bestemt. Der er således spekuleret meget, og man ved kun lidt om dets egenskaber.
Få mere at vide: Navne på de nye kemiske elementer - hyldesten til byer, regioner og videnskabsmænd
abstrakt om moscovius
Det er et syntetisk kemisk grundstof placeret i gruppe 15 af Periodiske system.
Det blev syntetiseret for første gang, i 2003, gennem fælles arbejde mellem russiske og amerikanske videnskabsmænd.
Det udgør den gruppe af grundstoffer, der senest er inkluderet i det periodiske system, i 2015.
Deres undersøgelser er meget nye, med grundlæggende egenskaber stadig under fastlæggelse.
Dens produktion foregår ved atomfusion, vha 48Ca og atomer af 243Er.
Moskva ejendomme
Symbol: Mc
Atom nummer: 115
Atommasse: 288 au.m.a (ikke officielt af Iupac)
Elektronisk konfiguration: [Rn] 7s2 5f14 6d10 7 p3
Mest stabile isotop: 288Mc (0,159 sekunders halveringstid)
kemisk serie: gruppe 15, supertunge elementer
Moskusagtige træk
muscovius er et af de sidste elementer inkluderets i det periodiske system. Dets optagelse fandt sted den 30. december 2015, og dets officielle navn blev frigivet den 8. juni 2016.
Indtil den dato var grundstof 115 kendt på portugisisk som ununpentio, fra latin, ununpentium, hvis oversættelse er "en, en, fem". En anden vedtagne nomenklatur var eka-bismuth, som betyder "ligner bismuth", element i den sjette periode i gruppe 15.
Muscovy er en syntetisk element, hvilket betyder, at det kun kan fremstilles i et laboratorium. Dette er meget almindeligt blandt supertunge grundstoffer, fordi deres kerne, med mange protoner og neutroner, ikke kan stabilisere sig, hvilket gør det umuligt at finde dem i naturen.
for at være en ustabilt element, det og de andre supertunge grundstoffer ender med at gennemgå radioaktivt henfald næsten øjeblikkeligt - partikelemissioner nukleare grundstoffer (såsom α- eller β-partikler) - og den deraf følgende transformation til andre lettere grundstoffer, som kan være stabile eller ingen.
Med hensyn til det skal det bemærkes, at dets undersøgelser stadig er meget nye, trods alt står vi over for et element, der blev produceret for knap 20 år siden, og hvis officielle status ikke engang er 10 år gammel. I denne henseende har videnskabsmænd været mere optaget af at bestemme grundlæggende egenskaber, såsom deres atommasse og dets kemiske opførsel i nogle mulige forbindelser.
For eksempel er den mest sandsynlige atommasse, der er påvist indtil videre for moskus, 288 atommasseenheder. For ikke at nævne, at opnåelse af muscovium er meget kompliceret, med en indtægt fra kun én atom Per dag.
Derudover kan det producerede atom ikke altid fanges for at måle massen. I 2018 kunne forskere ved Berkeley Laboratories, Californien, USA, kun måle én masse om ugen. Dermed, undersøgelser om egenskaberne af dets forbindelser er stadig inden for teoretisk kemi, med beregninger og matematiske modeller til bestemmelse af de forventede resultater.
Opnåelse af Muscovy
Indhentning af moscovium sker ved Kernefusion. ioner af 48Her11+ (Z = 20) accelererede hit atomer af 243Am (Z = 95), arrangeret i form af AmO2 på et cirkulært mål titanium på 32 cm², hvilket producerer moscoviet (Z = 115) og tre neutroner.
Efter stød, på omkring et mikrosekund (10-6 sekund), rammer moskusatomet detektoren, som er omkring fire meter væk fra kollisionsstedet. På denne vej går grundstoffet også gennem en separator, så lettere reaktionsprodukter afledes. I detektoren, muscovium detekteres af dets radioaktive henfaldsmønster.
Moscovium, som et radioaktivt atom, gennemgår alfa-henfald (en radioaktiv partikel med to protoner og to neutroner), hvilket producerer grundstof 113 (nihonium, Nh) til grundstof 105 (dubnium, Db). Endelig bliver Db'en til rutherfordium (Rf), som hurtigt opdeles i to fragmenter. Henfaldsmønsteret for moscovium er vist nedenfor.
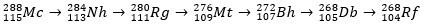
Moskvas historie
muscovius var første gang syntetiseret i 2003, mellem 14. juli og 10. august gennem fælles arbejde af videnskabsmænd fra Joint Institute for atomforskning i Dubna, Rusland og Lawrence Livermore National Laboratory i Livermore, Californien.
Ioner af 48Ca, så de kunne kollidere med atomer af 243Am, som oprindeligt producerede isotopen 291Mc. Under processen blev kernen opvarmet til utrolige 4 x 1011 K, og derefter afkølet ved den meget hurtige emission af tre neutroner og gammastråler.

Denne handling dannede isotopen 288Mc. derefter moscovius blev opdaget og analyseret baseret på dets mønster af radioaktive henfald (alfa-henfald). Navnet Moskow er en hyldest til Moskva-regionen, Rusland.
Læs også:Seaborgium - det syntetiske kemiske grundstof opkaldt efter videnskabsmanden Glenn Seaborg
Løste øvelser på moscovium
Spørgsmål 1
Moscovium, et nyligt opdaget grundstof, blev placeret i gruppe 15 i det periodiske system. Baseret på de andre elementer i denne gruppe ville det forventede hydrid for dette element være:
A) McH
B) McH2
C) McH3
D) McH4
E) Mc2H3
Løsning:
Alternativ C
Andre gruppe 15 elementer, som f.eks nitrogen det er fosfor, præsentere formlerne NH3 og pH3 når de er bundet til brint. Det forventes således, at moscovium præsenterer formlen McH3 også.
spørgsmål 2
I 2003 blev moscovium (Z = 115) syntetiseret for første gang gennem fælles arbejde af russiske og amerikanske videnskabsmænd. På det tidspunkt, isotopen 288Mc blev opdaget, og dets produktion var afgørende for at placere dette grundstof i det periodiske system. Antallet af neutroner i denne isotop er:
A) 115
B) 288
C) 403
D) 173
E) 170
Løsning:
Alternativ D
Antallet af neutroner kan beregnes sådan:
A = Z + n
Hvor A er massetallet, Z er atomnummeret, og n er antallet af neutroner. Ved at erstatte værdierne får vi:
288 = 115 + n
n = 288 – 115
n = 173
Af Stefano Araujo Novais
Kemi lærer
