Reaktionerne af tilføjelse er vigtige handlinger med hensyn til organiske synteser, fordi der gennem dem kan udvikles et interessant antal organiske stoffer.
For at additionsreaktionen kan finde sted, er det nødvendigt at skabe to bindingssteder i kulstofkæden, hvilket simpelthen opstår, når kæden er umættet (tilstedeværelse af pi link). Når pi-linket er brudt, vises webstederne således i kæden.
En gruppe af stoffer, der kan bruges i tillæg synteser er cycloalkaner eller cyklaner, gruppe af kulbrinter med cykliske og mættede kæder. De undslipper den generelle regel om tilføjelse, da de ikke har et pi-link, men afhængigt af nogle forhold (varme, katalysatormetal, surt medium) de kan gennemgå et kædebrud mellem to kulstofatomer, hvilket får to bindingssteder til at opstå, så tilsætningen kan finde sted. Der er dog et faktum, der begrænser brugen af disse forbindelser. Faktum er opkaldet ring stress teori, foreslået af Adolf V. Bayer i 1885.
For at sigmabindingen mellem carbonerne kan brydes, skal der være en vis ustabilitet mellem carbonerne. Denne ustabilitet er relateret til vinklen af bindinger mellem carboner. Ifølge Bayer er den vinkel, der giver en
stor stabilitet til sigma-linket er 109,47O. Således kæder, der har en vinkel mellem kulstofatomer mindre end 109,47O de har en tendens til at have ustabilitet i sigma-bindingerne mellem de kulstoffer, der danner kæderne, hvilket begunstiger deres brud forbundet med en ideel ydre tilstand.De eneste cycloalkaner, der har en vinkel mindre end 109,47O blandt dets kulstof er cyclopropan (60O), cyclobutan (90O) og cyclopentan (108O). Cyclopentan har en vinkel meget tæt på 109,47O den har meget stabile sigma-bindinger, derfor kan den ikke gennemgå nogen additionsreaktion. Nedenfor har vi strukturerne af disse tre cycloalkaner:

Strukturformel for henholdsvis cyclopropan, cyclobutan og cyclopentan
Observation: Enhver cycloalkan, der har mere end 5 carbonatomer i kæden, vil udføre en substitutionsreaktion for eksempel, og aldrig en tilføjelse, fordi sigma-bindingerne mellem deres kulstofatomer er ekstreme stabil.
De additionsreaktioner, der kan ske med cycloalkaner, er stort set alle, men med cyclopentan er de eneste, det kan gennemgå, hydrogenering og halogenering. Nedenfor er eksempler på tilføjelser med cycloalkaner og deres betingelser for forekomst:
a) Hydrogenering
Reaktion af cycloalkanen med brintmolekylet med tilstedeværelsen af pulveriseret metallisk katalysator (zink, nikkel eller platin) i nærvær af opvarmning (omkring 180°COÇ). I denne reaktion vil cycloalkanen give anledning til en alkan. I denne reaktion, efter at cyklussen er brudt, tilføjes et brintatom til hver af carbonatomerne i sigmabindingen, der blev brudt.
Stop ikke nu... Der er mere efter reklamen ;)

Additionsreaktion i cyclobutan under anvendelse af hydrogen
b) Halogenering
Reaktion af cycloalkanen med halogenmolekylet (f.eks. klor, brom, jod) med tilstedeværelsen af jern III chloridkatalysator (FeCl3). I denne reaktion vil cycloalkanen give anledning til en organisk halogenid med to halogenatomer i kæden. Efter at cyklussen er brudt, har vi tilføjelsen af et halogenatom på hver af carbonatomerne i sigmabindingen, der blev brudt.

Additionsreaktion i cyclobutan under anvendelse af brom
c) Reaktion med halogenhydrider (syrehalogenider)
Reaktion af cycloalkanen med det halogenholdige uorganiske hydratmolekyle (HCl. HBr, HI). Da en syre bruges som reaktant, bruges der ikke en katalysator. I denne reaktion vil cycloalkanen give anledning til en organisk halogenid med kun et halogenatom i kæden. Efter cyklussen er brudt har vi tilføjelsen af et brintatom på et af carbonatomerne i sigmabindingen, der blev brudt, og et halogen på det andet carbon. Overhold Markovnikovs regel (H på det mest hydrogenerede kulstof og halogen på det mindst hydrogenerede kulstof).
Bemærk: Det forekommer kun med cyclopropan og cyclobutan.
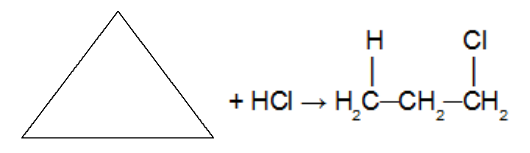
Additionsreaktion i cyclopropan under anvendelse af saltsyre
Bemærk: Det forekommer kun med cyclopropan og cyclobutan.
d) Hydrering
Reaktion af cycloalkan med et vandmolekyle i nærvær af svovlsyre og opvarmning. I denne reaktion vil cycloalkanen give anledning til en mono alkohol (alkohol med kun én OH-gruppe i kæden). Efter cyklussen er brudt har vi tilføjelsen af et hydrogenatom på et af carbonatomerne i sigmabindingen, der blev brudt, og en hydroxyl (OH) på det andet carbon. Overhold Markovnikovs regel (H på det mest hydrogenerede kulstof og hydroxyl på det mindst hydrogenerede kulstof).
Bemærk: Det forekommer kun med cyclopropan og cyclobutan.

Additionsreaktion i cyclopropan under anvendelse af saltsyre
Af mig Diogo Lopes Dias
Vil du referere til denne tekst i et skole- eller akademisk arbejde? Se:
DAGE, Diogo Lopes. "Tilføjelser i cyklaner"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/adicoes-ciclanos.htm. Tilgået den 27. juli 2021.
Kemi

Hydroxyl funktionel gruppe, Primære alkoholer, Sekundære alkoholer, Tertiære alkoholer, Methanol, Glycerol, Ethanol, nitroglycerinpræparat, malingfremstilling, produktion af alkoholholdige drikkevarer, eddikesyre, brændstof biler.