I teksten "Hvordan fungerer katalysatorstoffer?”, Er det blevet vist, at katalysatorer er i stand til at øge reaktionshastigheden, fordi de mindsker aktiveringsenergien, der kræves for at reaktionen skal forekomme. De gør dette ved at ændre reaktionsmekanismen, kombinere med reaktanterne og danne en mellemforbindelse, som igen bliver produkterne og katalysatoren.
En af måderne til, at dette kan ske, kaldes Homogen katalyse, som er når katalysatoren danner et enkeltfasesystem med reaktanterne.
Dette betyder, at reaktanterne, produkterne og katalysatoren alle skal være i samme fase, dvs. i samme fysiske tilstand.
Undersøgelsen af denne type katalyse er vigtig for videnskab og industri, da flere vigtige reaktioner til produktion kan fremskyndes med små mængder katalysatorer.
Et eksempel på homogen katalyse anvendt i industrien er et mellemliggende trin i fremstillingen af svovlsyre (H2KUN4 (aq)), hvor dannelsen af svovltrioxid (SO3 (g)) gennem forbrændingsreaktionen af svovldioxid (SO2 (g)), vist nedenfor:
2 SÅ2 (g) + O2 (g) → 2 OS3 (g)
Denne reaktion forløber for langsomt, så der tilsættes en katalysator, nitrogendioxid (NO).2 (g)). Denne katalysator kombineres med svovldioxid til dannelse af en mellemforbindelse (aktiveret kompleks), som er nitrogenmonoxid (NO(g)).
Denne mellemforbindelse reagerer derefter med iltgas (O2 (g)) til katalysatorregenerering. Se nedenfor, hvordan dette sker, og observer, hvordan de alle er i gasfasen og danner et homogent medium:
katalysatorkompleks aktiveret
Trin 1: 2 OS2 (g) + 2 NEJ2 (g)→ 2 OS3 (g) + 2 NEJ(g)
Trin 2: 2 NEJ(g)+ 1 O2 (g) → 2 NEJ2 (g)
Global reaktion: 2 SO2 (g) + O2 (g) → 2 OS3 (g)
Bemærk, at katalysatoren kun deltager i de mellemliggende trin, men ikke forbruges. I slutningen af reaktionen er han fuldt genoprettet. Reaktionen med denne mekanisme lavet i to trin kræver mindre aktiveringsenergi, og den fortsætter derfor hurtigere.
Grafisk repræsentation:
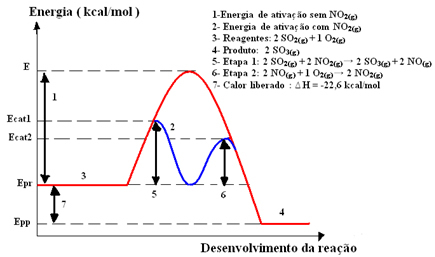
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/catalise-homogenea.htm

