Strukturel formel er skemaet, der angiver strukturen, det vil sige arrangementet af atomer, der udgør de kemiske grundstoffer, samt forbindelsen mellem dem. Det kan repræsenteres på forskellige måder: fladt, kondenseret eller elektronisk.
Blandt de faktorer, der konditionerer de anvendte strukturer, er antallet af elektroner i valensskallen en af dem.
Flad formel
Den flade formel bruger bindestreger til at repræsentere kovalente bindinger, som kan være enkelt, dobbelt eller tredobbelt og repræsenteret på følgende måder:
- enkel forbindelse (når 2 elektroner deles)
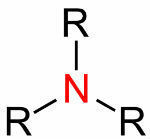
= dobbeltbinding (når 4 elektroner deles)
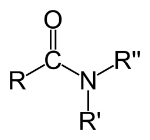
≡ tredobbelt link (når 6 elektroner deles)
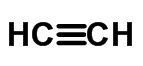
Kondenseret eller forenklet formel
I den kondenserede strukturformel vises bindingerne ikke.
I sin repræsentation er antallet af atomer for hvert element angivet på en kondenseret måde, dvs. forenklet:
H3C CH2 CH2 CH3
Lineær kondenseret formel
Den lineære kondenserede formel bruger zigzag-linjer, i hvis hjørner kulstofferne er repræsenteret:
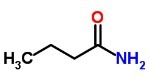
Elektronisk eller Lewis-formel
Den elektroniske formel, også kaldet Lewis-formlen, er repræsenteret af prikker.
Gennem disse punkter vises de mængder elektroner, der er til stede i valenslagene:
H: H
Og den molekylære formel?
DET molekylær formeluden at henvise til dets struktur, angiver antallet af elementer, der udgør a molekyle. Ud over at angive antallet af atomer til stede i hvert element og deres proportioner.
Det kan opnås gennem den minimale eller empiriske formel og procent- eller centesimalformlen.
Læs også Isomerisme og Valencia lag.
Løst øvelser
1. (Vunesp-2000) Skriv strukturformlen, og angiv det officielle navn:
a) en mættet forgrenet carbonketonketon med i alt 7 carbonatomer.
b) en aminosyre med 4 carbonatomer.
Det)

B)
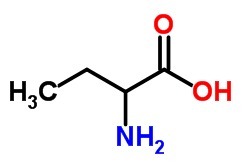
2. (FGV-2005) Aspartam er et kunstigt sødemiddel, der ved et uheld blev opdaget i 1965 af en skødesløs kemiker, der slikkede sine beskidte fingre og følte, at de var søde.
Disse uhygiejniske vaner anbefales ikke, da mange stoffer i små mængder er meget giftige.
Strukturformlen for aspartam er vist nedenfor:

Fra strukturformlen for aspartam ser det ud til, at der er
a) 13 carbonatomer pr. molekyle.
b) 1 etherfunktionel gruppe.
c) 1 dipeptid
d) 2 tertiære carbonatomer
e) kun 1 asymmetrisk carbonatom.
Alternativ c: 1 dipeptid
For at fortsætte med at teste din viden, se også disse øvelseslister:
- Øvelser på kulbrinter
- Øvelser om organisk kemi
- Øvelser på flad isomerisme