Nogle metaller findes ikke frie i naturen og skal opnås ved laboratorieprocedurer. En af de effektive og økonomiske metoder til oprensning af metaller er gennem elektrolyse. Elektrolyse finder sted i elektrolytiske celler med to elektroder forbundet til terminalerne på en jævnstrømsgenerator.
Det er kendt, at der i en elektrolytisk celle er en katode og en anode, se definitionen for hver:
Katode: Det er den negative elektrode, der tiltrækker kationer, og det er her, kationreduktionen opstår.
anode: Den positive elektrode, der tiltrækker anioner, og derfor er det her anionen oxiderer.
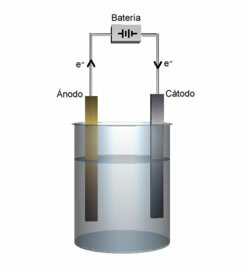
Anode og katode demonstration.
Kobberrensning
Kobber, som findes i naturen, har urenheder som sølv, jern, guld, zink. Gennem elektrolyse er det muligt at isolere dette metal, der opnår det i ren form, følg processen:
- Uren kobber fungerer som en anode, og en vandig opløsning af kobbersulfat fungerer som en elektrolyt, der er inde i den elektrolytiske celle. Cellens katode er kobber i sig selv i en høj grad af renhed.
- Kobber overføres fra anoden til katoden, mens urenhederne forbliver i opløsning. Kobber i ren tilstand akkumuleres ved katoden og kan således bruges.
Af Líria Alves
Uddannet i kemi
Brazil School Team
Se mere!
Elektrolysereaktioner
Elektrolyseprodukter
Elektrolyse - Fysisk-kemisk - Kemi - Brasilien skole
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/purificacao-metais-atraves-eletrolise.htm


