Det periodiske system er et vigtigt undersøgelsesværktøj, der samler information om alle kendte kemiske grundstoffer.
Test din viden med denne liste over 17 spørgsmål med de forskellige tilgange til emnet og løs din tvivl med de beslutninger, der er kommenteret efter feedbacken.
For at hjælpe med at forstå spørgsmålene, brug periodiske system komplet og opdateret.
Periodisk systemorganisation
Spørgsmål 1
(UFU) I begyndelsen af det nittende århundrede med opdagelsen og isoleringen af forskellige kemiske grundstoffer blev det nødvendigt at klassificere dem rationelt for at udføre systematiske undersøgelser. Mange bidrag blev tilføjet, indtil de nåede den nuværende periodiske klassificering af kemiske grundstoffer. Svar på den aktuelle periodiske klassifikation:
a) Hvordan er elementerne anført sekventielt i det periodiske system?
Det periodiske system er organiseret i sekvenser af kemiske grundstoffer i stigende rækkefølge af Atom nummer. Dette antal svarer til antallet af protoner i atomens kerne.
Denne organisationsmetode blev foreslået af Henry Moseley, da han omkonfigurerede bordet foreslået af Dmitri Mendeleiev.
Et element kan placeres i tabellen efter familien og den periode, hvori det indsættes. Denne fordeling sker som følger:
| grupper eller familier | 18 lodrette sekvenser |
| Grupper af elementer, der har lignende egenskaber. |
| Perioder | 7 vandrette sekvenser |
| Antal elektroniske lag, som elementet har. |
b) Hvilke grupper i det periodiske system findes: et halogen, et alkalimetal, et jordalkalimetal, et chalcogen og en ædelgas?
Klassificeringen af elementer i grupper udføres i henhold til egenskaber. Elementer, der er i samme gruppe, har lignende karakteristika, og for klassificeringerne, skal vi:
| Klassifikation | Gruppe | Familie | Elementer |
| halogen | 17 | 7A | F, Cl, Br, I, At og Ts |
| alkalimetal | 1 | 1A | Li, Na, K, Rb, Cs og Fr |
| jordalkalimetal | 2 | 2A | Vær, Mg, Ca, Sr, Ba og Ra |
| kalkogen | 16 | 6A | O, S, Se, Te, Po og Lv |
| ædelgas | 18 | 8A | Han, Ne, Ar, Kr, Xe, Rn og Og |
spørgsmål 2
(PUC-SP) Løs problemet baseret på analysen af udsagnene nedenfor.
I - Det nuværende moderne periodiske system er arrangeret i stigende rækkefølge af atommassen.
II - Alle elementer, der har 1 elektron og 2 elektroner i valensskallen er, henholdsvis alkalimetaller og jordalkalimetaller, forudsat at det vigtigste kvantetal er af dette lag (n 1).
III - I samme periode præsenterer elementerne det samme antal niveauer (lag).
IV - I den samme gruppe (familie) har elementerne det samme antal niveauer (lag).
Det konkluderes, at de er korrekte med hensyn til den nuværende periodiske tabel over kemiske grundstoffer:
a) I og IV (kun).
b) I og II (kun).
c) II og III (kun).
d) II og IV (kun).
e) III og IV (kun).
Korrekt alternativ: c) II og III (kun).
Når vi analyserer hvert alternativ, skal vi:
Jeg - forkert. Elementerne er arrangeret i stigende rækkefølge efter atomnummer.
II - KORREKT. Elektronerne i valensskallen definerer gruppen, elementet er placeret i.
| alkalimetaller | 1 elektron i valensskallen |
| 3Læs | 2-1 |
| 11På | 2-8-1 |
| 19K | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Fr | 2-8-18-32-18-8-1 |
| jordalkalimetaller | 2 elektroner i valensskallen |
| 4være | 2-2 |
| 12mg | 2-8-2 |
| 20Her | 2-8-8-2 |
| 38Hr | 2-8-18-8-2 |
| 56Ba | 2-8-18-18-8-2 |
| 88Frø | 2-8-18-32-18-8-2 |
Hovedkvantantallet svarer til skallen, hvori elektronen er placeret, og er forskellig fra 1, fordi ved den elektroniske distribution bemærker vi, at elektronens placering er fra den anden skal eller n = 2.
III - KORREKT. Placeringen af et element i en bestemt periode skyldes antallet af lag, når man foretager den elektroniske distribution.
| Perioder | 7 vandrette sekvenser |
| 1. periode | 1 lag: K |
| 2. periode | 2 lag: K, L. |
| 3. periode | 3 lag: K, L, M |
| 4. periode | 4 lag: K, L, M, N. |
| 5. periode | 5 lag: K, L, M, N, O |
| 6. periode | 6 lag: K, L, M, N, O, P |
| 7. periode | 7 lag: K, L, M, N, O, P, Q |
Eksempel: kemisk element placeret i den anden periode.
IV - forkert. Elementer, der tilhører den samme gruppe, har lignende egenskaber, og det skyldes, at de har det samme antal elektroner i valensskallen.
Eksempel:
| Beryllium | Magnesium |
|
2 elektroner i valenslag. |
2 elektroner i valenslag. |
Derfor er beryllium og magnesium en del af gruppe 2 i det periodiske system.
spørgsmål 3
(Unitins) Angående den moderne periodiske klassificering af elementer, identificer den sande udsagn:
a) i en familie har elementerne generelt det samme antal elektroner i den sidste skal.
b) i det periodiske system placeres de kemiske grundstoffer i faldende rækkefølge efter atommasserne.
c) i en familie har elementerne meget forskellige kemiske egenskaber.
d) i en periode har elementerne lignende kemiske egenskaber.
e) alle repræsentative elementer hører til gruppe B i det periodiske system.
Korrekt alternativ: a) i en familie har elementerne generelt det samme antal elektroner i den sidste skal.
a) KORREKT. Kemiske elementer i samme familie har det samme antal elektroner i den sidste skal, og det får dem til at have lignende egenskaber.
b) forkert. Atommasserne stiger, når atomets antal stiger.
c) forkert. Elementernes kemiske egenskaber er ens, så de er grupperet i samme familie.
d) forkert. På en gang har elementerne deres elektroner fordelt i det samme antal skaller.
e) forkert. De repræsentative elementer tilhører gruppe A, som svarer til familierne: 1A, 2A, 3A, 4A, 5A, 6A, 7A og 8A. Elementer, der hører til gruppe B, er overgangselementer.
spørgsmål 4
(Vunesp) I betragtning af egenskaberne ved kemiske grundstoffer og det periodiske system er det forkert at angive:
a) et metal er et stof, der leder elektrisk strøm, er duktilt og formbart.
b) et ikke-metal er et stof, der ikke leder elektrisk strøm, hverken er duktilt eller formbart.
c) en semimetal har det fysiske udseende af et metal, men kemisk adfærd svarende til et ikke-metal.
d) de fleste kemiske grundstoffer består af ikke-metaller.
e) ædelgasserne er monoatomiske.
Forkert alternativ: d) de fleste kemiske grundstoffer er ikke-metaller.
Bemærk klassificeringen af kemiske grundstoffer i det periodiske system i metaller, ikke-metaller og semimetaller.

Som vi kan se, er de fleste grundstoffer metaller.
a) KORREKT. Metaller leder elektricitet på grund af elektronskyer dannet af frie elektroner, som er karakteristiske for deres struktur. De er duktile, fordi de kan blive til ledninger eller ark, afhængigt af det område, hvor der påføres tryk. De kan også formes, da der kan produceres meget tynde ark med denne type materiale.
b) KORREKT. Ikke-metaller har de modsatte egenskaber ved metaller. I stedet for ledere er de gode varmeisolatorer, og da de er sprøde, er de ikke støbt i ledninger eller plader, da de ikke har god duktilitet og formbarhed.
c) KORREKT. Halvmetaller har egenskaber, der er mellemliggende til metaller og ikke-metaller. At være halvledere af elektricitet har de en metallisk glans, men er skøre som ikke-metaller.
d) forkert. De fleste grundstoffer er klassificeret som metaller. Klasserne af metaller, der er til stede i det periodiske system, er: alkalisk, jordalkalisk, overgangs intern og ekstern.
e) KORREKT. Ædle gasser er monoatomiske, så de er kun repræsenteret ved deres initialer.
Eksempel:
| ædelgas | kalkogen |
| Helium (He) | Oxygen (O2) |
| monoatomisk: dannet af et atom | diatomisk: dannet af to atomer |
På grund af ædelgassens stabilitet har elementerne i denne familie lav reaktivitet og er også kendt som inaktive.
spørgsmål 5
Om tilrettelæggelsen af det nuværende periodiske system, svar:
a) Hvad er kolonner?
b) Hvad er linjerne?
c) Hvad er metoden til at organisere de kemiske grundstoffer?
Svar:
a) søjlerne er grupperne i det periodiske system, tidligere kaldet familier, der samler kemiske grundstoffer med lignende egenskaber.
b) Linjerne er perioderne i det periodiske system og angiver antallet af elektroniske lag af et atom i jordtilstand.
c) De kemiske grundstoffer i det aktuelle periodiske system er arrangeret i stigende rækkefølge efter atomnummer, hvilket angiver antallet af protoner i atomens kerne.
Periodiske bordfamilier
Spørgsmål 1
(CESGRANRIO) Oprettelse af forbindelsen mellem nedenstående kolonner, der svarer til elementfamilierne i henhold til det periodiske system, vil den numeriske rækkefølge være:
| 1. ædle gasser | • Gruppe 1A |
| 2. alkalimetaller | • Gruppe 2A |
| 3. jordalkalimetaller | • Gruppe 6A |
| 4. Chalcogens | • Gruppe 7A |
| 5. Halogener | • Gruppe 0 |
a) 1, 2, 3, 4, 5.
b) 2, 3, 4, 5, 1.
c) 3, 2, 5, 4, 1.
d) 3, 2, 4, 5, 1.
e) 5, 2, 4, 3, 1.
Korrekt alternativ: b) 2, 3, 4, 5, 1.
| grupper | elektronisk konfiguration |
| • Gruppe 1A: 2. alkalimetaller | os1 (med n |
| • Gruppe 2A: 3. jordalkalimetaller | os2 (med n |
| • Gruppe 6A: 4. Chalcogens | os2np4 |
| • Gruppe 7A: 5. Halogener | os2np5 |
| • Gruppe 0: 1. ædle gasser | 1s2 (Han) eller os2np6 (hvis n> 1) |
spørgsmål 2
(UECE) Det kemiske element med Z = 54 har i sit valenslag 5-konfigurationen2 5p6. Elementerne med Z = 52 og med Z = 56 tilhører familierne af:
a) kalcogener og jordalkalier
b) halogener og baser
c) halogener og jordalkalier
d) chalcogener og baser
Korrekt alternativ: a) kalcogener og jordalkalier.
I betragtning af atomnumrene udførte vi den elektroniske distribution og fandt følgende resultater:
| 54X og | 52Du | 56Ba |
|
8 elektroner i valenslag |
6 elektroner i valenslag |
2 elektroner i valenslag |
| Ædle gasser: 8A familie | Chalcogens: 6A familie | Alkaline Earth: familie 2A |
spørgsmål 3
(F. Ibero-Americana-SP) Den periodiske systemgruppe, der er karakteriseret ved overvejelsen af kunstige elementer, er følgende:
a) lanthanider
b) ædelgasser
c) overgangsmetaller
d) jordalkalimetaller
e) actinider
Korrekt alternativ: e) actinider.
Kunstige elementer er dem, der ikke findes i naturen, og som er blevet syntetiseret i laboratoriet gennem nukleare reaktioner.
De kaldes også transuraniske grundstoffer, da disse radioaktive grundstoffer har et atomnummer større end 92, hvilket svarer til uran.
Generelt er disse elementer kortvarige og varer op til brøkdele af et sekund.
Ifølge disse oplysninger skal vi:
Elementerne findes i naturen er: lanthanider, ædle gasser, overgangsmetaller og jordalkalimetaller. Med undtagelse af technetium og promethium, som er kunstige.
Overvejelsen af kunstige elementer er actinider, klassificeret som interne overgangsmetaller og indsat i det periodiske system under lanthaniderne. Fra denne serie er kun actinium, thorium, protactinium og uran naturlige.
spørgsmål 4
(U. Katolske kirke i Salvador-BA) X-arten2- med 8 elektroner i den yderste skal (valensskal) kan den være fra element X, som i det periodiske system hører til gruppen:
a) 7A
b) 6A
c) 2A
d) 1A
e) 8A
Korrekt alternativ: b) 6A.
Ifølge oktetreglen forudsætter det for et element at opnå stabilitet den elektroniske konfiguration af en ædelgas, som har 8 elektroner i valensskallen.
Opladning 2- på art X2- angiver, at elementet har fået 2 elektroner.
Elektronkonfigurationen for de arter, der har 8 elektroner i den yderste skal, er ns2np6.
Efter at have mistet to elektroner, vender elementet tilbage til sin jordtilstand med ns-elektronkonfiguration2np4.
De 6 elektroner i valensskallen er karakteristiske for chalcogener, elementer i 6A-familien.
For eksempel:
| Element: ilt | elektronisk konfiguration |
| 8O | 1s22s22p4 |
| art O2- | 1s22s22p6 |
Lær mere om Periodiske bordfamilier.
Kemiske grundstoffer
Spørgsmål 1
(CESGRANRIO) I betragtning af elementerne i atomnummer 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 og 75 er indstillingen, der kun indeholder alkalimetaller:
a) 3, 11, 37 og 55
b) 3, 9, 37 og 55
c) 9, 11, 38 og 55
d) 12, 20, 38 og 56
e) 12, 37, 47 og 75
Korrekt alternativ: a) 3, 11, 37 og 55
Alkalimetaller svarer til de kemiske grundstoffer, der afslutter den elektroniske distribution med en elektron i underniveau.
Ved at foretage den elektroniske fordeling af de givne atomnumre har vi følgende alkalimetaller:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| Lithium | Natrium | Rubidium | Cæsium |
De andre atomnumre svarer til elementerne i følgende grupper:
Jordalkalimetaller: afslut elektronisk distribution på underniveau s2.
| Z = 12 | Z = 38 | Z = 56 |
| Magnesium | Strontium | Barium |
Overgangsmetaller: afslut elektronisk distribution på underniveau d.
| Z = 30 | Z = 47 | Z = 75 |
| Zink | Sølv | Rhenium |
Halogener: afslut elektronisk distribution på underniveau s5.
| Z = 9 |
spørgsmål 2
(Unirio) “Det kunstige hjerte, der blev placeret i Eloi, blev udviklet for fire år siden i USA og bruges allerede af omkring 500 mennesker. Sættet, kaldet Heartmate, består af tre hovedstykker. Det vigtigste er en fire-pund rund taske, 12 centimeter i diameter og 3 centimeter tyk, lavet af titanium - et sølv-hvidt metal, let og stærkt. ” Veja Magazine, juli 1999.
Blandt nedenstående metaller er den, der i det sidste lag har et antal elektroner svarende til titanets:
a) C
b) I
c) Ga
d) Mg
e) Xe
Korrekt alternativ: d) mg.
| Titanium | elektronisk konfiguration | Lagfordeling |
| 22Du | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
Fra den elektroniske distribution af titanium ser vi, at dette element har 2 elektroner i den sidste skal.
| Element | elektronisk konfiguration | Lagfordeling |
| 6Ç | 1s2 2s2 2p2 | 2, 4 |
| 11På | 1s2 2s2 2p6 3s1 | 2, 8, 1 |
| 31Ga | 1s2 2s2 2p6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12mg | 1s2 2s2 2p6 3s2 | 2, 8, 2 |
| 54X og | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 | 2, 8, 18, 18, 8 |
Elementet, der også har 2 elektroner i den sidste skal er magnesium.
spørgsmål 3
(UFPA) Overvej et bestemt kemisk element, hvis mest energiske underniveau er 5s2. Dets atomnummer og gruppen, hvor det er placeret på det periodiske system, er henholdsvis:
a) 20; 1A
b) 20; 2A
c) 38; 2A
d) 38; 1A
e) 39; 2A
Korrekt alternativ: c) 38; 2A
Ved at udføre elektronisk distribution fandt vi, at:
- Det kemiske element er placeret i familien 2A, da det har det mest energiske underniveau s2
- Har atomnummer 38, hvilket svarer til det samlede antal distribuerede elektroner.
- Det er placeret i den femte periode, da den elektroniske distribution blev udført op til det femte lag.
Når vi kontrollerer disse oplysninger i det periodiske system, kan vi bekræfte, at det er elementet strontium.
spørgsmål 4
(UFC) Et x-atom har et proton mere end et y-atom. På baggrund af disse oplysninger skal du bestemme den korrekte erklæring.
a) Hvis y er jordalkalisk, er x alkalimetal.
b) Hvis y er en ædelgas, er x et halogen.
c) Hvis y er et overgangsmetal, er x en ædelgas.
d) Hvis y er en ædelgas, er x et alkalimetal.
e) x er placeret i samme periode før y-atomet i det periodiske system.
Korrekt alternativ: d) Hvis y er en ædelgas, er x et alkalimetal.
Det periodiske system er arrangeret i stigende rækkefølge efter atomnummer.
Hvis Y har atomnummer z, og X har en proton mere end det, betyder det, at disse to grundstoffer er i samme periode, og X efterfølger Y.
Eksempel:
| Element | efterfølgende element |
| zY | z + 1x |
| 11På | 12mg |
De to grundstoffer er i 3. periode, og magnesium har en proton mere end natrium.
Ifølge denne begrundelse skal vi:
a) forkert. Et alkalimetal kommer før et jordalkalimetal på det periodiske system. Den korrekte sætning ville være: Hvis y er alkalimetal, er x jordalkalisk jord.
b) forkert. Et halogen kommer før ædelgassen i det periodiske system. Den korrekte sætning ville være: Hvis y er halogen, er x ædelgas.
c) forkert. Overgangsmetaller og ædelgasser adskilles af andre kemiske grundstoffer og er derfor ikke sekventielle.
d) KORREKT. Ædle gasser er den sidste gruppe i det periodiske system, og alkalimetaller er den første, så de er sekventielle.
Eksempel:
| ædelgas | alkalimetal |
| zY | z + 1x |
| 2han | 3Læs |
Lithium, et alkalimetal, har en proton mere end helium, som er en ædelgas.
e) forkert. X er i samme periode som Y først efter det, ikke før som alternativet siger.
spørgsmål 5
Fra et kemisk grundstofs atomnummer er det muligt at vide:
a) antallet af neutroner i kernen
b) antallet af elektroner i elektrosfæren
c) kernemassen
Svar: b) antallet af elektroner i elektrosfæren
Et atom i jordtilstand er elektrisk neutralt. Så ved at kende atomnummeret, der svarer til antallet af protoner (positivt ladede partikler), kender vi antallet af elektroner (negativt ladede partikler) i elektrosfæren.
For eksempel har jern et atomnummer 26, så i jordtilstand har det 26 elektroner omkring kernen.
Lær mere om kemiske grundstoffer Det er Atom nummer.
Periodiske og aperiodiske egenskaber
Spørgsmål 1
(UFSM) Bedøm, om udsagnene relateret til elementernes periodiske egenskaber er sande (T) eller falske (F).
() Afhænger af elementernes atommasser.
() De gentages med mere eller mindre regelmæssige intervaller i forhold til stigningen i atomtal.
() Er ens i den samme gruppe af elementer.
() Er ens i den samme periode med elementer.
() I den samme gruppe stiger de numeriske værdier for de periodiske egenskaber altid, når der er en stigning i det atomare antal elementer.
Den korrekte rækkefølge er:
a) V - F - V - F - F
b) V - F - F - V - V
c) F - V - V - F - F
d) F - V - F - V - V
e) V - F - F - V - F
Korrekt alternativ: c) F - V - V - F - F
(FALSK) Afhænger af elementernes atommasser.
Ifølge Moseleys lov om periodicitet varierer mange fysiske og kemiske egenskaber ved kemiske grundstoffer efter atomnummer.
(RIGTIGT) De gentages med mere eller mindre regelmæssige intervaller i forhold til stigningen i atomtal.
Egenskaber som atomradius, atomvolumen, densitet, smeltepunkt og kogning er eksempler på egenskaber, der gentages regelmæssigt i det periodiske system.
(RIGTIGT) Ligner i samme gruppe af elementer.
De periodiske tabelgrupper er arrangeret med elementer, der har lignende egenskaber.
(FALSK) Ligner i samme periode af elementer.
Ejendomme er ens i familier, ikke perioder. I perioder fordeles elementerne efter antallet af elektroniske lag.
(FALSK) I samme gruppe stiger de numeriske værdier for de periodiske egenskaber altid, når der er en stigning i det atomare antal elementer.
Egenskaber kan stige eller falde afhængigt af atomnummeret. Et eksempel på dette er elektronegativitet, som falder, når atomnummeret stiger i en given gruppe.
Læs også: Periodiske egenskaber
spørgsmål 2
(FAESP) Elementernes aperiodiske egenskaber er:
a) densitet, atomvolumen og atommasse.
b) smeltepunkt, elektronegativitet og specifik varme.
c) atomvolumen, atommasse og smeltepunkt.
d) atommasse, specifik varme og smeltepunkt.
e) atommasse og specifik varme.
Korrekt alternativ: e) atommasse og specifik varme.
De aperiodiske egenskaber gentages med regelmæssige intervaller.
Atommasse er målingen på atomets vægt i atommasseenheder, hvilket svarer til af kulstof-12-massen.
Specifik varme bestemmer den mængde varme, der er nødvendig for at øge temperaturen med 1 ° C på 1 g af elementet.
Disse to egenskaber er ikke relateret til elementets position på det periodiske system.
De andre egenskaber er klassificeret som periodiske, da de stiger eller falder med atomnummeret. Er de:
- Densitet: repræsenterer kvotienten mellem massen og volumenet af et element.
- Atomisk volumen: repræsenterer volumenet af et sæt atomer og påvirker afstanden mellem dem.
- Smeltepunkt: temperatur ved hvilken overgangen fra fast til flydende forekommer.
- Elektronegativitet: atomets evne til at tiltrække sig selv det elektroniske par, som det deler i en kovalent binding.
Læs også: elektronegativitet og Elektronisk affinitet
spørgsmål 3
(PUC-PR) Hvilke er korrekte blandt følgende diagrammer relateret til det periodiske system?
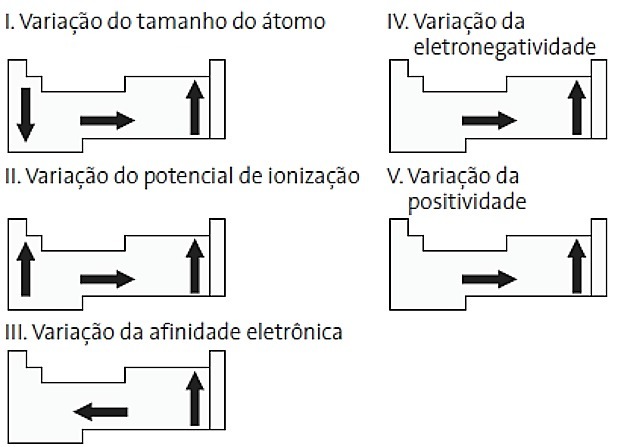
a) II og V
b) II og III
c) I og V
d) II og IV
e) III og IV
Korrekt alternativ: d) II og IV.
JEG. FORKERT. Atomstørrelsesvariation måles ved den gennemsnitlige afstand fra kernen til den yderste elektron. De største atomer er placeret i bunden af tabellen, så stigningen sker i henhold til atomnummeret, og den korrekte repræsentation er:
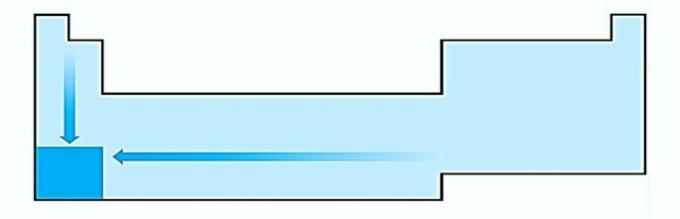
II. KORREKT Den nødvendige energi til at rive en elektron af et isoleret atom i gasform kaldes ioniseringspotentialet. Det øges som vist i sætningen diagram.
III. FORKERT. Elektronisk affinitet udtrykker den frigivne energi, når et neutralt atom i gasformig tilstand modtager en elektron, hvilket er en meget vigtig egenskab ved ikke-metaller. De højeste elektroniske affiniteter observeres i halogener og ilt.
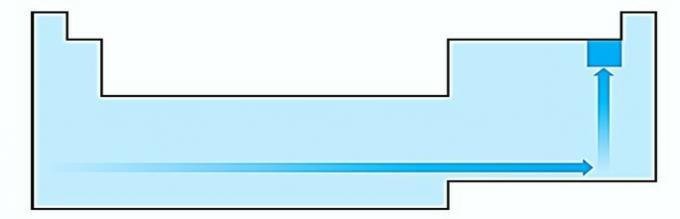
IV. KORREKT Elektronegativitet er relateret til ioniseringspotentiale og elektronaffinitet. Som sådan er halogener de mest elektronegative elementer i det periodiske system.
V. FORKERT. Elektropositivitet forekommer i den modsatte retning af elektronegativitet. Det repræsenterer atomets evne til at opgive elektroner.
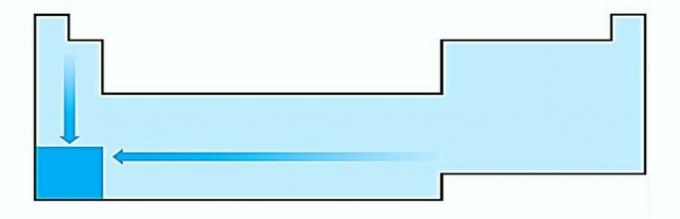
Derfor har alkalimetaller den højeste elektropositivitet.
Bliv ved med at teste din viden med listerne:
- Øvelser på kemiske bindinger
- Øvelser i elektronisk distribution
- Øvelser på atommodeller
- Øvelser på termokemi

